1 . 汽车排气系统中的催化转化器可将汽车尾气中的 转化为无害物质,减少对大气的污染,一种
转化为无害物质,减少对大气的污染,一种 储存-还原(NSR)技术的工作原理如图所示。下列说法中正确的是
储存-还原(NSR)技术的工作原理如图所示。下列说法中正确的是
 转化为无害物质,减少对大气的污染,一种
转化为无害物质,减少对大气的污染,一种 储存-还原(NSR)技术的工作原理如图所示。下列说法中正确的是
储存-还原(NSR)技术的工作原理如图所示。下列说法中正确的是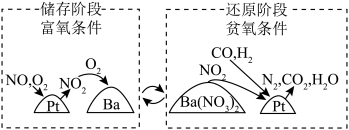
A.该过程可减少 的排放高温 的排放高温 |
B.存储阶段发生反应: |
C. 是催化剂 是催化剂 |
| D.汽车尾气中来自润滑油的磷、锌元素会增强催化效果 |
您最近一年使用:0次
解题方法
2 . 我国研制出一种多功能复合催化剂,能将 转化为烯烃和汽油,转化步骤如下:
转化为烯烃和汽油,转化步骤如下: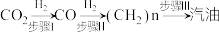 。步骤I除生成
。步骤I除生成 外,还生成另一种氧化物,其电子式为
外,还生成另一种氧化物,其电子式为_______ 。
 转化为烯烃和汽油,转化步骤如下:
转化为烯烃和汽油,转化步骤如下: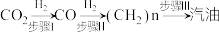 。步骤I除生成
。步骤I除生成 外,还生成另一种氧化物,其电子式为
外,还生成另一种氧化物,其电子式为
您最近一年使用:0次
解题方法
3 . 以碳酸锰矿(主要成分为 、
、 、
、 、
、 )和软锰矿(主要成分为
)和软锰矿(主要成分为 )为原料制取大颗粒的电池
)为原料制取大颗粒的电池 。其工艺主要包括“联合浸锰”、“沉淀除杂”、“溶解转化”、“氧化分解”。
。其工艺主要包括“联合浸锰”、“沉淀除杂”、“溶解转化”、“氧化分解”。
(1)联合浸锰。向反应器中加入一定量稀硫酸,然后依次加入软锰矿、碳酸锰矿,充分反应后过滤得到含 的酸浸液。其中生成单质
的酸浸液。其中生成单质 反应的离子方程式为
反应的离子方程式为___________ 。碳酸锰矿不能先于软锰矿加入的原因是___________ 。
(2)沉淀除杂。向上述酸浸液中加入 调节剂再通入
调节剂再通入 得到
得到 。酸浸液中
。酸浸液中 、
、 、
、 的浓度分别为
的浓度分别为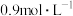 、
、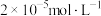 、
、 ,若使酸浸液中
,若使酸浸液中 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )与
)与 、
、 分离,需控制溶液中
分离,需控制溶液中 的范围为
的范围为___________ 。[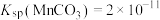 ,
,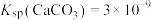 ,
,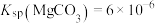 ]
]
(3)若反应过程中,“沉锰”中若产生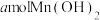 沉淀。现用
沉淀。现用 一定浓度的
一定浓度的 溶液将其全部转化为
溶液将其全部转化为 ,需
,需 溶液的浓度至少为
溶液的浓度至少为___________  (用含
(用含 的表达式表示)。
的表达式表示)。
已知:[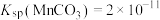 ,
, ]
] 经过溶解、沉淀,得到含少量
经过溶解、沉淀,得到含少量 的
的 沉淀。向该沉淀中加水,边加热边持续通空气可得到
沉淀。向该沉淀中加水,边加热边持续通空气可得到 。沉淀加热通空气过程中溶液
。沉淀加热通空气过程中溶液 随时间的变化如题图所示,其中
随时间的变化如题图所示,其中 先基本不变后迅速下降的原因是
先基本不变后迅速下降的原因是___________ 。
(5) 含量测定:准确称取
含量测定:准确称取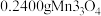 样品于锥形瓶中,加入
样品于锥形瓶中,加入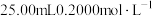 草酸钠溶液和适量硫酸,加热。待样品完全溶解后,冷却,立即用
草酸钠溶液和适量硫酸,加热。待样品完全溶解后,冷却,立即用 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液
溶液 。测定过程中发生下列反应:
。测定过程中发生下列反应:

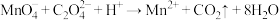
计算 样品的纯度(写出计算过程)
样品的纯度(写出计算过程)___________ 。
 、
、 、
、 、
、 )和软锰矿(主要成分为
)和软锰矿(主要成分为 )为原料制取大颗粒的电池
)为原料制取大颗粒的电池 。其工艺主要包括“联合浸锰”、“沉淀除杂”、“溶解转化”、“氧化分解”。
。其工艺主要包括“联合浸锰”、“沉淀除杂”、“溶解转化”、“氧化分解”。(1)联合浸锰。向反应器中加入一定量稀硫酸,然后依次加入软锰矿、碳酸锰矿,充分反应后过滤得到含
 的酸浸液。其中生成单质
的酸浸液。其中生成单质 反应的离子方程式为
反应的离子方程式为(2)沉淀除杂。向上述酸浸液中加入
 调节剂再通入
调节剂再通入 得到
得到 。酸浸液中
。酸浸液中 、
、 、
、 的浓度分别为
的浓度分别为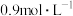 、
、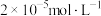 、
、 ,若使酸浸液中
,若使酸浸液中 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )与
)与 、
、 分离,需控制溶液中
分离,需控制溶液中 的范围为
的范围为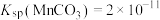 ,
,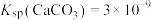 ,
,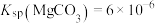 ]
](3)若反应过程中,“沉锰”中若产生
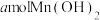 沉淀。现用
沉淀。现用 一定浓度的
一定浓度的 溶液将其全部转化为
溶液将其全部转化为 ,需
,需 溶液的浓度至少为
溶液的浓度至少为 (用含
(用含 的表达式表示)。
的表达式表示)。已知:[
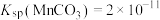 ,
, ]
]
 经过溶解、沉淀,得到含少量
经过溶解、沉淀,得到含少量 的
的 沉淀。向该沉淀中加水,边加热边持续通空气可得到
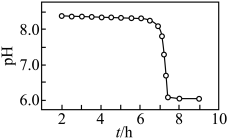
沉淀。向该沉淀中加水,边加热边持续通空气可得到 。沉淀加热通空气过程中溶液
。沉淀加热通空气过程中溶液 随时间的变化如题图所示,其中
随时间的变化如题图所示,其中 先基本不变后迅速下降的原因是
先基本不变后迅速下降的原因是(5)
 含量测定:准确称取
含量测定:准确称取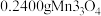 样品于锥形瓶中,加入
样品于锥形瓶中,加入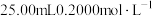 草酸钠溶液和适量硫酸,加热。待样品完全溶解后,冷却,立即用
草酸钠溶液和适量硫酸,加热。待样品完全溶解后,冷却,立即用 溶液进行滴定,消耗
溶液进行滴定,消耗 溶液
溶液 。测定过程中发生下列反应:
。测定过程中发生下列反应:
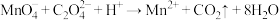
计算
 样品的纯度(写出计算过程)
样品的纯度(写出计算过程)
您最近一年使用:0次
解题方法
4 . 一定条件下,O2得电子转化为超氧自由基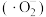 ,并实现如下转化,下列说法错误的是
,并实现如下转化,下列说法错误的是
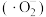 ,并实现如下转化,下列说法错误的是
,并实现如下转化,下列说法错误的是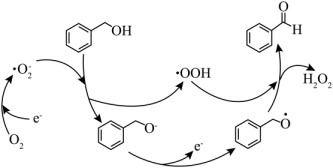
A.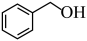 有5种不同化学环境的氢原子 有5种不同化学环境的氢原子 | B.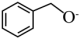 转化为 转化为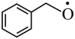 发生了还原反应 发生了还原反应 |
C.总反应为: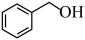 +O2 +O2 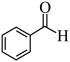 +H2O2 +H2O2 | D.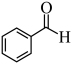 具有还原性,能被氧气氧化 具有还原性,能被氧气氧化 |
您最近一年使用:0次
5 . 有效氯是指含氯消毒剂与浓盐酸反应生成的氯气的质量与含氯消毒剂质量的比值,可用于衡量含氯消毒剂的效能。
(1)NaClO与HCl反应生成氯气的化学方程式为 ,请用单线桥法标出该反应的电子转移情况
,请用单线桥法标出该反应的电子转移情况_______ 。
(2)上述反应中氧化剂与还原剂的物质的量之比为:________ 。
(3)某品牌含氯消毒剂中含有质量分数为10%的NaClO,该消毒液的有效氯为_______ (结果保留3位小数)。
(1)NaClO与HCl反应生成氯气的化学方程式为
 ,请用单线桥法标出该反应的电子转移情况
,请用单线桥法标出该反应的电子转移情况(2)上述反应中氧化剂与还原剂的物质的量之比为:
(3)某品牌含氯消毒剂中含有质量分数为10%的NaClO,该消毒液的有效氯为
您最近一年使用:0次
6 . 五种短周期主族元素在周期表中的相对位置如图所示。
已知:在周期表中Z元素的非金属性最强。请回答下列问题:
(1)Y、W的氢化物有 、
、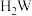 ,它们的分子含电子数均为
,它们的分子含电子数均为_____ ;二者反应的化学方程式为_____ 。
(2)基态R原子的电子排布式为_____ 。
(3)X、Y、Z、W的气态氢化物的热稳定性强弱排序为_____ (用化学式表示)。
(4)XY_2与Z的氢化物反应的化学方程式为_____ 。
(5)在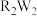 中滴加W的最高价氧化物对应的水化物稀溶液,发生剧烈反应的化学方程式为
中滴加W的最高价氧化物对应的水化物稀溶液,发生剧烈反应的化学方程式为_____ ;W所在周期所有元素中第一电离能比W大的元素种类一共有_____ 种。
| Y | Z | |||||
| R | X | W |
(1)Y、W的氢化物有
 、
、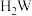 ,它们的分子含电子数均为
,它们的分子含电子数均为(2)基态R原子的电子排布式为
(3)X、Y、Z、W的气态氢化物的热稳定性强弱排序为
(4)XY_2与Z的氢化物反应的化学方程式为
(5)在
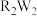 中滴加W的最高价氧化物对应的水化物稀溶液,发生剧烈反应的化学方程式为
中滴加W的最高价氧化物对应的水化物稀溶液,发生剧烈反应的化学方程式为
您最近一年使用:0次
7 . 人体缺铁会造成贫血。补铁剂中含有 ,长期放置会变质。检验它是否变质的方法:
,长期放置会变质。检验它是否变质的方法:______ 。 可以用酸性高锰酸钾溶液来检验,补齐产物并配平相关反应方程式
可以用酸性高锰酸钾溶液来检验,补齐产物并配平相关反应方程式______ :
______ ______
______ ______
______ ______
______ ______
______ ______。
______。
 ,长期放置会变质。检验它是否变质的方法:
,长期放置会变质。检验它是否变质的方法: 可以用酸性高锰酸钾溶液来检验,补齐产物并配平相关反应方程式
可以用酸性高锰酸钾溶液来检验,补齐产物并配平相关反应方程式______
 ______
______ ______
______ ______
______ ______
______ ______。
______。
您最近一年使用:0次
8 . 下图为硫循环示意图,请回答以下问题
(1)下列不能由单质直接化合生成的物质是___________。
(2)硫磺和过氧化钠都是淡黄色固体,如何鉴别某固体物质为硫磺或过氧化钠:___________ 。硫单质有多种结构,例如S2、S4、S6和S8等,它们互称___________ ,已知S8中S原子最外层满足8电子稳定结构,且S8结构中仅有硫硫单键,计算16gS8固体中共价键的数目为___________ 。
Ⅱ.火山喷发产生的气体中含有H2S,经过一系列化学反应最终能转变为硫磺。
(3)写出H2S的结构式___________ ,写出H2S在水溶液中的电离方程式___________ 。
(4)H2S从火山口喷出后在空气中转变化SO2,写出有关化学反应方程式___________ ,之后生成的SO2与剩余H2S继续反应形成硫磺,SO2与H2S反应产物中氧化产物与还原产物的比例为___________ 。
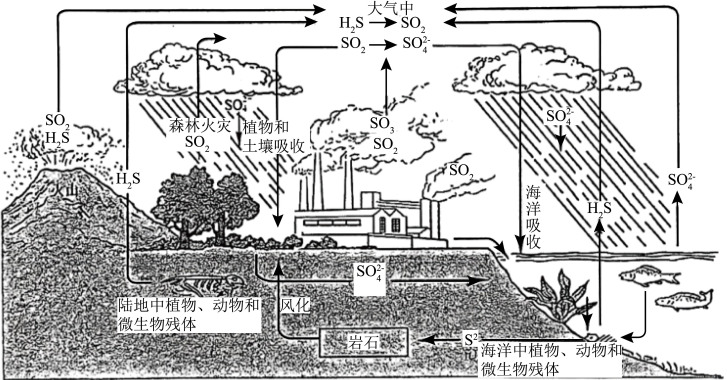
(1)下列不能由单质直接化合生成的物质是___________。
| A.CuS | B.SO3 | C.FeS | D.Na2S |
(2)硫磺和过氧化钠都是淡黄色固体,如何鉴别某固体物质为硫磺或过氧化钠:
Ⅱ.火山喷发产生的气体中含有H2S,经过一系列化学反应最终能转变为硫磺。
(3)写出H2S的结构式
(4)H2S从火山口喷出后在空气中转变化SO2,写出有关化学反应方程式
您最近一年使用:0次
解题方法
9 . 为提高农作物产量,现代农业生产中需要大量含氮化合物作肥料。
(1)下列固氮方法中,属于人工固氮的是______(填字母)。
(2)植物的根瘤菌能把空气中的氮气转化为氨,被植物吸收,这种过程被称为氮的固定。此过程可简单地用化学方程式表示为:____N2+____C+____H2O ____NH3+____CO2,配平以上化学方程式
____NH3+____CO2,配平以上化学方程式____ ,若转移3 mol电子则会生成______ mol NH3。
(1)下列固氮方法中,属于人工固氮的是______(填字母)。
| A.合成氨 | B.闪电固氮 |
| C.根瘤菌固氮 | D.用氨气合成尿素 |
 ____NH3+____CO2,配平以上化学方程式
____NH3+____CO2,配平以上化学方程式
您最近一年使用:0次
解题方法
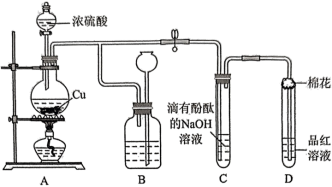
10 . 鲁能巴蜀中学化学学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:_____ ,圆底烧瓶中发生反应的化学方程式为_____ 。
(2)装置 的作用是贮存多余的气体,
的作用是贮存多余的气体, 中广口瓶内应盛放的液体是
中广口瓶内应盛放的液体是_____ (填序号)。
①水 ②饱和的 溶液 ③
溶液 ③ 溶液 ④酸性
溶液 ④酸性 溶液
溶液
(3)装置 和
和 中产生的现象相同,但原因却不同。
中产生的现象相同,但原因却不同。 中是由于
中是由于 具有漂白性,而
具有漂白性,而 中的原因是
中的原因是_____ 。
(4)铜与过量 反应的探究如下:
反应的探究如下: 溶解的离子方程式为
溶解的离子方程式为_____ ;产生的气体为_____ 。
(5)比较实验①和②,说明 的作用是
的作用是_____ 。
(6)用足量 处理实验②新制的溶液得到沉淀
处理实验②新制的溶液得到沉淀 ,元素分析表明
,元素分析表明 为铜的氧化物,提纯干燥后的
为铜的氧化物,提纯干燥后的 在惰性氛围下加热,
在惰性氛围下加热, 完全分解为
完全分解为 黑色氧化物
黑色氧化物 ,
,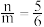 。
。 的化学式为
的化学式为_____ 。
(2)装置
 的作用是贮存多余的气体,
的作用是贮存多余的气体, 中广口瓶内应盛放的液体是
中广口瓶内应盛放的液体是①水 ②饱和的
 溶液 ③
溶液 ③ 溶液 ④酸性
溶液 ④酸性 溶液
溶液(3)装置
 和
和 中产生的现象相同,但原因却不同。
中产生的现象相同,但原因却不同。 中是由于
中是由于 具有漂白性,而
具有漂白性,而 中的原因是
中的原因是(4)铜与过量
 反应的探究如下:
反应的探究如下: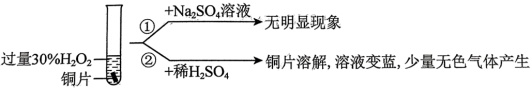
 溶解的离子方程式为
溶解的离子方程式为(5)比较实验①和②,说明
 的作用是
的作用是(6)用足量
 处理实验②新制的溶液得到沉淀
处理实验②新制的溶液得到沉淀 ,元素分析表明
,元素分析表明 为铜的氧化物,提纯干燥后的
为铜的氧化物,提纯干燥后的 在惰性氛围下加热,
在惰性氛围下加热, 完全分解为
完全分解为 黑色氧化物
黑色氧化物 ,
, 。
。 的化学式为
的化学式为
您最近一年使用:0次



