名校
解题方法
1 . 从废旧镍钴锰三元锂电池正极材料[主要含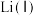 、
、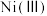 、
、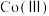 、
、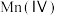 等金属的氧化物]中回收钴的一种流程如下:
等金属的氧化物]中回收钴的一种流程如下: 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是
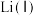 、
、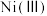 、
、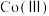 、
、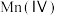 等金属的氧化物]中回收钴的一种流程如下:
等金属的氧化物]中回收钴的一种流程如下: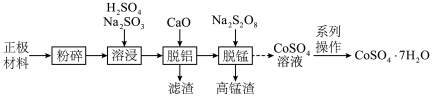
 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是A.“溶浸”中 被还原 被还原 |
B.“脱铝”得到的滤渣成分是 |
C.“脱锰”的离子方程式为: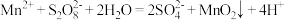 |
| D.“系列操作”含蒸发结晶、洗涤、干燥 |
您最近一年使用:0次
2 . 铊(Tl)本身是一种剧毒物质,为毒性最大的金属元素之一,但是铊在工业中的用途非常广泛,主要存在于一些矿物和工业废水中,也可以从含铊的合金中提取.从某铅锌厂的富铊灰(主要成分为 、
、 、
、 、
、 、
、 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示:
①在氯化物-硫酸水溶液中,铊元素以 形式存在;
形式存在;
(2)萃取过程的反应原理为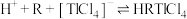 .
.
请回答下列问题:
(1)基态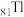 原子核外电子的运动状态有
原子核外电子的运动状态有________ 种.
(2)“浸取I”过程中为提高铊的浸取速率,可采取的措施有________________ (写出两条).
(3)写出“浸取I”中 发生反应的化学方程式:
发生反应的化学方程式:________________ ,“滤渣”的主要成分是________ (填化学式).
(4)请从化学平衡的角度解释“反萃取”过程中加入 溶液的原因:
溶液的原因:________________ .
(5)写出“还原氯化沉淀”中反应的离子方程式:________________ .
(6)通过沉淀法也可以去除工业废水中的 和
和 .
.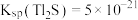 ,某地区规定工业污水中铊的污染物排放限值为
,某地区规定工业污水中铊的污染物排放限值为 ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中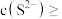
________  (假设污水中铊全部以
(假设污水中铊全部以 形式存在).
形式存在).
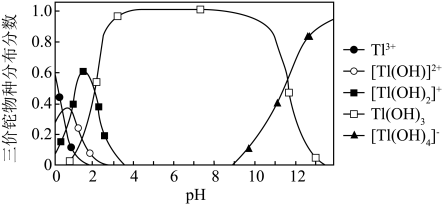
②向含铊废水中加入溴水,使 充分氧化成
充分氧化成 ,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是________________ .
 、
、 、
、 、
、 、
、 )中回收铊的工艺流程如图所示:
)中回收铊的工艺流程如图所示: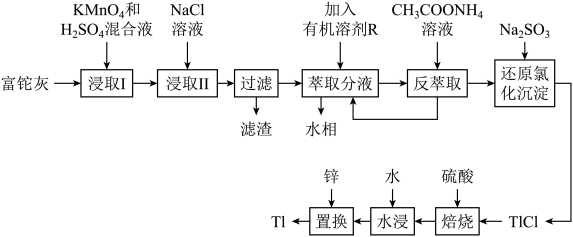
①在氯化物-硫酸水溶液中,铊元素以
 形式存在;
形式存在;(2)萃取过程的反应原理为
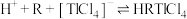 .
.请回答下列问题:
(1)基态
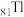 原子核外电子的运动状态有
原子核外电子的运动状态有(2)“浸取I”过程中为提高铊的浸取速率,可采取的措施有
(3)写出“浸取I”中
 发生反应的化学方程式:
发生反应的化学方程式:(4)请从化学平衡的角度解释“反萃取”过程中加入
 溶液的原因:
溶液的原因:(5)写出“还原氯化沉淀”中反应的离子方程式:
(6)通过沉淀法也可以去除工业废水中的
 和
和 .
.
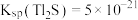 ,某地区规定工业污水中铊的污染物排放限值为
,某地区规定工业污水中铊的污染物排放限值为 ,若铊的含量符合国家排放限值,则处理后的废水中
,若铊的含量符合国家排放限值,则处理后的废水中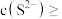
 (假设污水中铊全部以
(假设污水中铊全部以 形式存在).
形式存在).②向含铊废水中加入溴水,使
 充分氧化成
充分氧化成 ,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
,调节溶液pH,沉淀去除铊元素.若pH过大,铊元素去除率下降的原因是
您最近一年使用:0次
解题方法
3 . 利用热镀锌厂在生产过程中产生的副产品锌灰(主要成分为ZnO、 及少量
及少量 、CuO、PbO等)为原料制备氧化锌或皓矾(
、CuO、PbO等)为原料制备氧化锌或皓矾( )工艺流程如下:
)工艺流程如下: 、
、 进入溶液;
进入溶液;
②25℃时, ,
, ;
;
③深度除杂标准:溶液中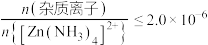 ;
;
④有机萃取剂(用HR表示)可萃取出 ,其萃取原反应为:
,其萃取原反应为: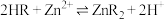 。
。
(1)浸渣中含有的物质包括PbOCl、______ 。
(2)除砷时, 转化为
转化为 沉淀,写出该反应的离子方程式
沉淀,写出该反应的离子方程式______ 。
(3)若深度除铜所得滤液中 的浓度为0.2
的浓度为0.2 ,则溶液中
,则溶液中 (不考虑水解)浓度至少为
(不考虑水解)浓度至少为______  ,才能达到深度除杂标准。
,才能达到深度除杂标准。
(4)反萃取加入的X最佳物质为______ 。
(5)“沉锌”过程获得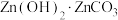 ,离子方程式为
,离子方程式为______ 。
(6)获取皓矾的一系列操作包括______ 、过滤、洗涤、干燥。取28.7g产品加热至不同温度,剩余固体的质量变化如图所示。已知B→D的过程中产生两种气体,分析数据,写出该过程的化学方程式______ 。
 及少量
及少量 、CuO、PbO等)为原料制备氧化锌或皓矾(
、CuO、PbO等)为原料制备氧化锌或皓矾( )工艺流程如下:
)工艺流程如下:
 、
、 进入溶液;
进入溶液;②25℃时,
 ,
, ;
;③深度除杂标准:溶液中
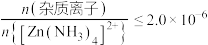 ;
;④有机萃取剂(用HR表示)可萃取出
 ,其萃取原反应为:
,其萃取原反应为: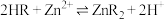 。
。(1)浸渣中含有的物质包括PbOCl、
(2)除砷时,
 转化为
转化为 沉淀,写出该反应的离子方程式
沉淀,写出该反应的离子方程式(3)若深度除铜所得滤液中
 的浓度为0.2
的浓度为0.2 ,则溶液中
,则溶液中 (不考虑水解)浓度至少为
(不考虑水解)浓度至少为 ,才能达到深度除杂标准。
,才能达到深度除杂标准。(4)反萃取加入的X最佳物质为
(5)“沉锌”过程获得
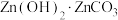 ,离子方程式为
,离子方程式为(6)获取皓矾的一系列操作包括
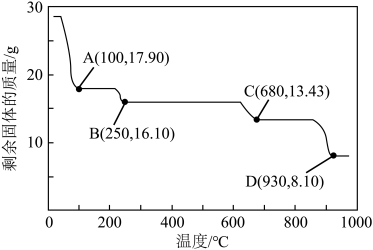
您最近一年使用:0次
名校
4 . 碘酸钾 是常用的食盐加碘剂,用
是常用的食盐加碘剂,用 氧化
氧化 得到
得到 溶液,再经一系列步骤得到
溶液,再经一系列步骤得到 产品。
产品。 是一种白色晶体,在水中溶解度随温度升高而增大。
是一种白色晶体,在水中溶解度随温度升高而增大。
下列说法错误的是
 是常用的食盐加碘剂,用
是常用的食盐加碘剂,用 氧化
氧化 得到
得到 溶液,再经一系列步骤得到
溶液,再经一系列步骤得到 产品。
产品。
 是一种白色晶体,在水中溶解度随温度升高而增大。
是一种白色晶体,在水中溶解度随温度升高而增大。下列说法错误的是
A.水浴加热时发生反应的离子方程式为 |
| B.滴入适量乙醇的作用是除去多余的高锰酸钾 |
| C.为提高洗涤效果,可用热水进行洗涤 |
| D.在冷却结晶时,温度过低可能导致产品的纯度降低 |
您最近一年使用:0次
5 . 聚合硫酸铁(Ⅲ)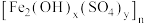 是一种新型、高效铁盐类无机高分子絮凝剂,工业上用高硫铝土矿(主要成分为
是一种新型、高效铁盐类无机高分子絮凝剂,工业上用高硫铝土矿(主要成分为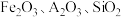 、少量
、少量 )为原料制备聚合硫酸铁的部分工艺流程如图所示。下列说法正确的是
)为原料制备聚合硫酸铁的部分工艺流程如图所示。下列说法正确的是
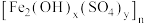 是一种新型、高效铁盐类无机高分子絮凝剂,工业上用高硫铝土矿(主要成分为
是一种新型、高效铁盐类无机高分子絮凝剂,工业上用高硫铝土矿(主要成分为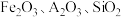 、少量
、少量 )为原料制备聚合硫酸铁的部分工艺流程如图所示。下列说法正确的是
)为原料制备聚合硫酸铁的部分工艺流程如图所示。下列说法正确的是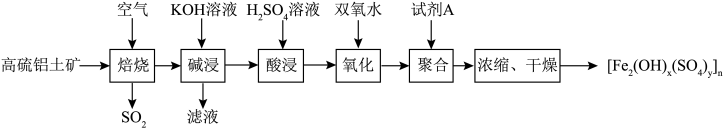
A.“焙烧”过程中若生成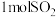 ,则转移 ,则转移 电子 电子 |
B.“滤液”中含有的阴离子主要为 |
| C.“聚合”过程中试剂A作还原剂,使各种离子发生聚合 |
| D.实际生产过程中,为了加快反应速率,整个流程均选择高温条件 |
您最近一年使用:0次
名校
6 . 研究有机物的结构和性质对生产生活意义深远。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。___________ ,B物质的分子式为:___________ 。
(2)按官能团分类,D所属的类别是___________ 。
(3)1molE与足量的金属钠反应产生___________ L氢气(标况下)。
(4)实验室制取C的化学方程式___________ 。
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。___________ (填名称)。
(6)脱氢维生素C中,键角①___________ 键角②(填“>”、“=”或“<”)。
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是___________ 。
(8)标出维生素C中所有的手性碳原子(用*标注)___________ 。
 .已知A-F六种有机化合物,根据要求回答问题。
.已知A-F六种有机化合物,根据要求回答问题。A. 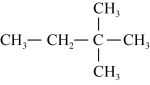 B.
B. 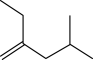 C.
C. D.
D. 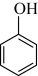 E.
E.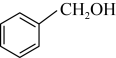
(2)按官能团分类,D所属的类别是
(3)1molE与足量的金属钠反应产生
(4)实验室制取C的化学方程式
 .蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被
.蔬菜和水果中富含维生素C,维生素C具有还原性,其又被称为抗坏血酸,在酸性溶液中可以被 等氧化剂氧化为脱氢维生素C.根据要求回答问题。
等氧化剂氧化为脱氢维生素C.根据要求回答问题。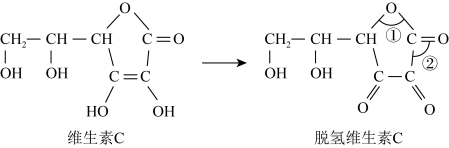
(6)脱氢维生素C中,键角①
(7)向碘和淀粉溶液中加入维生素C,可能观察到的现象是
(8)标出维生素C中所有的手性碳原子(用*标注)
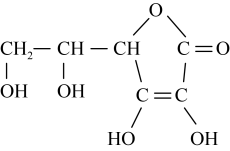
您最近一年使用:0次
解题方法
7 . 化学让生活更加美好。下列对化学物质的使用所作的解释不正确的是
选项 | 化学物质的使用 | 解释 |
A | 滴眼液中含有微量硝酸银 | 银离子可使蛋白质变性 |
B | 用氢氟酸雕刻玻璃 |
|
C | 用铝罐盛放浓硫酸 | 浓硫酸不与 |
D | 维生素C常用作抗氧化剂 | 维生素C能被氧化为脱氢抗坏血酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
69次组卷
|
2卷引用:广东省部分学校2024届高三下学期5月份大联考化学试题
名校
解题方法
8 . 用某复合金属作电极电解催化还原 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是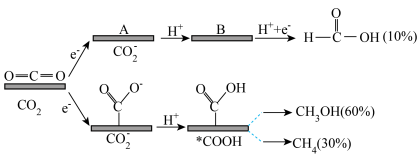
| A.过程中有极性键和非极性的断裂和形成 |
B.中间体B的结构简式为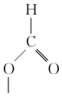 |
C. |
D.若有 完全转化,反应中转移的电子数为3.8mol 完全转化,反应中转移的电子数为3.8mol |
您最近一年使用:0次
名校
解题方法
9 . 固态化合物M的组成为CuSi2O5,以M为原料实现如下转化:
(1)①固体D的成分为_______ ,溶液E中含氮微粒有_______ 。
②写出反应Ⅱ的化学反应方程式_______ 。
③溶液F加热可得纳米 ,过程中pH会明显下降,原因是
,过程中pH会明显下降,原因是_______ 。
(2)下列说法正确的是_______。
(3)已知 能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验_______ 。

(1)①固体D的成分为
②写出反应Ⅱ的化学反应方程式
③溶液F加热可得纳米
 ,过程中pH会明显下降,原因是
,过程中pH会明显下降,原因是(2)下列说法正确的是_______。
| A.反应Ⅰ不能在陶瓷坩埚中进行 |
| B.固体X可溶于浓氨水 |
| C.溶液A经净化处理后可用于工业粘合剂 |
D.反应Ⅲ中发生的离子反应有: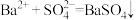 |
 能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
能溶于较浓强碱溶液,蓝色溶液C中可能存在铝元素,请设计实验方案进行检验
您最近一年使用:0次
名校
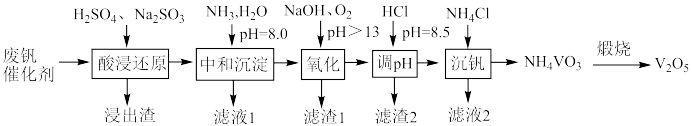
10 . 五氧化二饥广泛用于冶金、化工等行业。某废钒催化剂主要含有 、
、 、CaO、
、CaO、 、
、 、
、 等,采取如下工艺流程回收其中的钒制备
等,采取如下工艺流程回收其中的钒制备 ;
;
回答下列问题:
(1)基态V原子的价电子轨道表示式为________ 。
(2)浸出渣的主要成分是________ ,“酸浸还原”中 ;和
;和 均转化为
均转化为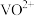 ,写出
,写出 转化为
转化为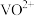 反应的离子方程式为
反应的离子方程式为________ 。
(3)“氧化”中被氧化的元素主要有________ (填元素符号)。
(4)“调pH”中有沉淀生成,写出生成沉淀反应的离子方程式________ 。
(5)“沉钒”中需要加入过量 ,其原因是
,其原因是________ 。 ,晶体未经洗涤直接进行“煅烧”,将导致
,晶体未经洗涤直接进行“煅烧”,将导致 产品中混有
产品中混有________ 杂质。
(6)工艺中可循环利用的物质有________ 。
(7)一定温度下, 溶解在NaOH溶液中,可得到偏钒酸钠。偏钒酸钠阴离子呈现如图1所示的无限链状结构。碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图2所示。
溶解在NaOH溶液中,可得到偏钒酸钠。偏钒酸钠阴离子呈现如图1所示的无限链状结构。碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图2所示。________ 。
②碳化钒晶胞中与碳原子距离最近且相等的碳原子个数为________ 。
③若碳化钒合金的密度为 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则晶胞参数
,则晶胞参数________ nm。
 、
、 、CaO、
、CaO、 、
、 、
、 等,采取如下工艺流程回收其中的钒制备
等,采取如下工艺流程回收其中的钒制备 ;
;
| 金属离子 |  |  |  |  |
开始沉淀时( )的pH )的pH | 12.4 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 13.8 | 4.7 | 3.2 | 9.0 |
(1)基态V原子的价电子轨道表示式为
(2)浸出渣的主要成分是
 ;和
;和 均转化为
均转化为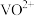 ,写出
,写出 转化为
转化为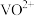 反应的离子方程式为
反应的离子方程式为(3)“氧化”中被氧化的元素主要有
(4)“调pH”中有沉淀生成,写出生成沉淀反应的离子方程式
(5)“沉钒”中需要加入过量
 ,其原因是
,其原因是 ,晶体未经洗涤直接进行“煅烧”,将导致
,晶体未经洗涤直接进行“煅烧”,将导致 产品中混有
产品中混有(6)工艺中可循环利用的物质有
(7)一定温度下,
 溶解在NaOH溶液中,可得到偏钒酸钠。偏钒酸钠阴离子呈现如图1所示的无限链状结构。碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图2所示。
溶解在NaOH溶液中,可得到偏钒酸钠。偏钒酸钠阴离子呈现如图1所示的无限链状结构。碳化钒主要用于制造钒钢及碳化物硬质合金添加剂,其晶胞结构如图2所示。
②碳化钒晶胞中与碳原子距离最近且相等的碳原子个数为
③若碳化钒合金的密度为
 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则晶胞参数
,则晶胞参数
您最近一年使用:0次

 与玻璃中
与玻璃中 反应
反应 反应
反应

