名校
1 . 以 为有效成分的漂白液应用广泛。某实验小组以
为有效成分的漂白液应用广泛。某实验小组以 为氧化剂,在实验室模拟氨氮废水的处理过程。
为氧化剂,在实验室模拟氨氮废水的处理过程。
I.制备漂白液
(1)用氯碱工业的产物制备漂白液的离子方程式为___________ 。
(2) 溶液中
溶液中 或
或 的组成分数
的组成分数 与
与 的关系如图所示。
的关系如图所示。 的电离常数
的电离常数 值为
值为___________ 。 含量的检测方法如图所示:
含量的检测方法如图所示: 的作用
的作用___________ 。
②若消耗 盐酸标准溶液
盐酸标准溶液 ,则漂白液中
,则漂白液中 的浓度为
的浓度为___________  。
。
Ⅱ.模拟氨氮废水(以 表示)的处理
表示)的处理
(4)反应的化学方程式为___________ 。
(5)实际消耗的 溶液的量高于理论值,可能原因是
溶液的量高于理论值,可能原因是___________ 。
(6)测定相同时间不同 值时次氯酸钠氧化去除氨氮的去除率如下图所示。
值时次氯酸钠氧化去除氨氮的去除率如下图所示。 范围为
范围为___________ 。
② 较低或较高去除率均下降的原因是
较低或较高去除率均下降的原因是___________ 。
 为有效成分的漂白液应用广泛。某实验小组以
为有效成分的漂白液应用广泛。某实验小组以 为氧化剂,在实验室模拟氨氮废水的处理过程。
为氧化剂,在实验室模拟氨氮废水的处理过程。I.制备漂白液
(1)用氯碱工业的产物制备漂白液的离子方程式为
(2)
 溶液中
溶液中 或
或 的组成分数
的组成分数 与
与 的关系如图所示。
的关系如图所示。 的电离常数
的电离常数 值为
值为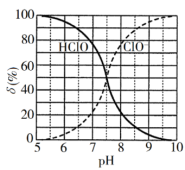
 含量的检测方法如图所示:
含量的检测方法如图所示: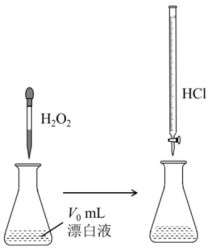
 的作用
的作用②若消耗
 盐酸标准溶液
盐酸标准溶液 ,则漂白液中
,则漂白液中 的浓度为
的浓度为 。
。Ⅱ.模拟氨氮废水(以
 表示)的处理
表示)的处理(4)反应的化学方程式为
(5)实际消耗的
 溶液的量高于理论值,可能原因是
溶液的量高于理论值,可能原因是(6)测定相同时间不同
 值时次氯酸钠氧化去除氨氮的去除率如下图所示。
值时次氯酸钠氧化去除氨氮的去除率如下图所示。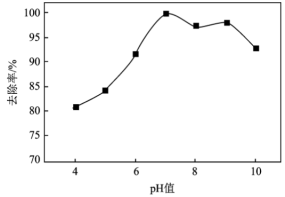
 范围为
范围为②
 较低或较高去除率均下降的原因是
较低或较高去除率均下降的原因是
您最近一年使用:0次
解题方法
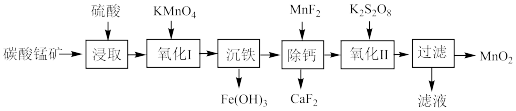
2 . 以碳酸锰矿(含 和少量FeO、
和少量FeO、 、CaO)为原料制取
、CaO)为原料制取 的工业流程如图所示。已知:
的工业流程如图所示。已知: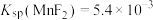 ,
,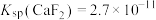 ,
, 氧化性强于
氧化性强于 ,其还原产物为
,其还原产物为 。
。
(1)Mn在元素周期表中的位置___________ 。
(2)为提高碳酸锰矿浸取速率,在用硫酸“浸取”时可采取的措施有:①___________ ;②搅拌;③适当升高温度等。
(3)“氧化I”的离子方程式为___________ 。
(4)“沉铁”过程加入的含钙元素的沉铁剂可能为___________ (写出一种即可)。
(5)若“除钙”后溶液中 ,则此时溶液中
,则此时溶液中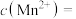
___________ mol/L。
(6)“氧化II”需加入 且过量,其原因是
且过量,其原因是___________ 。
(7)“过滤”后的滤液的溶质主要是___________ (填化学式)和过量的 。
。
 和少量FeO、
和少量FeO、 、CaO)为原料制取
、CaO)为原料制取 的工业流程如图所示。已知:
的工业流程如图所示。已知: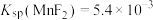 ,
,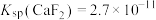 ,
, 氧化性强于
氧化性强于 ,其还原产物为
,其还原产物为 。
。
(1)Mn在元素周期表中的位置
(2)为提高碳酸锰矿浸取速率,在用硫酸“浸取”时可采取的措施有:①
(3)“氧化I”的离子方程式为
(4)“沉铁”过程加入的含钙元素的沉铁剂可能为
(5)若“除钙”后溶液中
 ,则此时溶液中
,则此时溶液中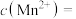
(6)“氧化II”需加入
 且过量,其原因是
且过量,其原因是(7)“过滤”后的滤液的溶质主要是
 。
。
您最近一年使用:0次
2024-09-17更新
|
87次组卷
|
2卷引用:山西省吕梁市2025届高三上学期开学考试化学试题
3 . 二氧化氯 是一种强氧化剂,广泛用于消毒杀菌、漂白、脱硫和脱硝等。
是一种强氧化剂,广泛用于消毒杀菌、漂白、脱硫和脱硝等。
(1)亚氯酸钠 可用于制备
可用于制备 。
。
① 氧化
氧化 可得到
可得到 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ 。
② 溶液用
溶液用 酸化也可得到
酸化也可得到 和
和 。反应中
。反应中 作
作___________ 。(填字母)
A.氧化剂 B.还原剂 C.催化剂 D.酸性介质
(2) 可将污水中
可将污水中 氧化为
氧化为 沉淀而除去,其还原产物
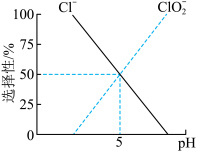
沉淀而除去,其还原产物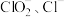 的选择性与
的选择性与 关系如图所示。写出
关系如图所示。写出 时,
时, 与
与 反应的离子方程式:
反应的离子方程式:___________ 。
 溶液中含氯组分(
溶液中含氯组分( 未画出)的百分含量(
未画出)的百分含量( )随
)随 变化情况如图所示。
变化情况如图所示。 时,溶液中
时,溶液中
___________ (填>、<、=)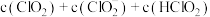 。
。
(2)其他条件一定时,测得随 溶液
溶液 的增大,其杀菌效率呈下降趋势,可能的原因是
的增大,其杀菌效率呈下降趋势,可能的原因是___________ 。
 是一种强氧化剂,广泛用于消毒杀菌、漂白、脱硫和脱硝等。
是一种强氧化剂,广泛用于消毒杀菌、漂白、脱硫和脱硝等。(1)亚氯酸钠
 可用于制备
可用于制备 。
。①
 氧化
氧化 可得到
可得到 ,写出反应的化学方程式:
,写出反应的化学方程式:②
 溶液用
溶液用 酸化也可得到
酸化也可得到 和
和 。反应中
。反应中 作
作A.氧化剂 B.还原剂 C.催化剂 D.酸性介质
(2)
 可将污水中
可将污水中 氧化为
氧化为 沉淀而除去,其还原产物
沉淀而除去,其还原产物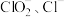 的选择性与
的选择性与 关系如图所示。写出
关系如图所示。写出 时,
时, 与
与 反应的离子方程式:
反应的离子方程式:
 溶液中含氯组分(
溶液中含氯组分( 未画出)的百分含量(
未画出)的百分含量( )随
)随 变化情况如图所示。
变化情况如图所示。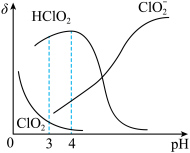
 时,溶液中
时,溶液中
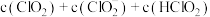 。
。(2)其他条件一定时,测得随
 溶液
溶液 的增大,其杀菌效率呈下降趋势,可能的原因是
的增大,其杀菌效率呈下降趋势,可能的原因是
您最近一年使用:0次
解题方法
4 . 实验室模拟工业硫酸镍(除 外,还含有少量
外,还含有少量 等)制备高纯硫酸镍的实验过程可表示为
等)制备高纯硫酸镍的实验过程可表示为 (开始沉淀的
(开始沉淀的 按金属离子浓度为
按金属离子浓度为 计算)如下表。
计算)如下表。
(1)“氧化”的目的是___________ 。
(2)下列可以替代 调节
调节 的是
的是___________ (填字母)。滤渣Ⅰ的化学式为___________ 。
A. B.
B. C.
C. D.
D.
(3)滤渣Ⅱ的化学式为___________ 。该步骤用到的玻璃仪器有烧杯、___________ 、___________ 。
(4)高纯硫酸镍可用于制备镍镉电池正极材料 。
。
① 中
中 的化合价为
的化合价为___________ 。
②写出在强碱溶液中用 氧化
氧化 生成
生成 的离子方程式:
的离子方程式:___________ 。
 外,还含有少量
外,还含有少量 等)制备高纯硫酸镍的实验过程可表示为
等)制备高纯硫酸镍的实验过程可表示为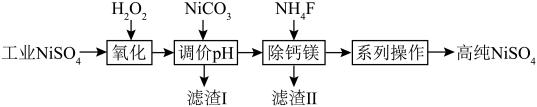
 (开始沉淀的
(开始沉淀的 按金属离子浓度为
按金属离子浓度为 计算)如下表。
计算)如下表。| 金属离子 | 开始沉淀的 | 沉淀完全的 |
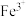 | 1.9 | 3.2 |
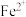 | 7.0 | 9.0 |
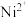 | 7.2 | 9.2 |
(1)“氧化”的目的是
(2)下列可以替代
 调节
调节 的是
的是A.
 B.
B. C.
C. D.
D.
(3)滤渣Ⅱ的化学式为
(4)高纯硫酸镍可用于制备镍镉电池正极材料
 。
。①
 中
中 的化合价为
的化合价为②写出在强碱溶液中用
 氧化
氧化 生成
生成 的离子方程式:
的离子方程式:
您最近一年使用:0次
5 . 油画创作需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄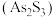 褪色的主要原因是发生了以下两种化学反应。下列说法正确的是
褪色的主要原因是发生了以下两种化学反应。下列说法正确的是
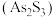 褪色的主要原因是发生了以下两种化学反应。下列说法正确的是
褪色的主要原因是发生了以下两种化学反应。下列说法正确的是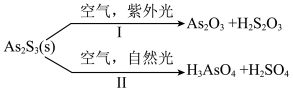
A. 与水作用可生成对应的酸: 与水作用可生成对应的酸: |
B.反应Ⅰ中元素 和 和 都被氧化 都被氧化 |
C.反应Ⅰ和Ⅱ中,氧化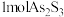 转移电子数之比为 转移电子数之比为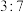 |
D.反应Ⅰ和Ⅱ中,参加反应的 :Ⅰ<Ⅱ :Ⅰ<Ⅱ |
您最近一年使用:0次
6 . Ⅰ.写出下列物质的电子式:
(1)过氧化钙:______ 。
(2)过氧化氢:______ 。
(3)氢化钙______ (金属氢化物都是离子化合物,均含有 价的氢离子)。
价的氢离子)。
Ⅱ.纯净的过氧化钙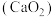 是一种新型水产养殖增氧剂,常用于鲜活水产品的运输,可以起到杀菌、供氧的作用。
是一种新型水产养殖增氧剂,常用于鲜活水产品的运输,可以起到杀菌、供氧的作用。
(4)写出供氧的化学方程式:______ 。
Ⅲ.已知过一硫酸 中硫为
中硫为 ,其第一步电离完全,第二步微弱。
,其第一步电离完全,第二步微弱。
(5)每个 分子中存在过氧键的数目为
分子中存在过氧键的数目为______ 个(每两个 价的氧原子之间形成一个过氧键)。
价的氧原子之间形成一个过氧键)。
(6)下列有关 的说法不正确的是________。
的说法不正确的是________。
(7)泡沫灭火器中硫酸铝与一种钠盐反应产生大量气体,写出离子方程式:______ 。
(8)已知 有
有 和
和 价,
价, 加入
加入 溶液中,生成紫红色溶液。由此推断,酸性条件下,
溶液中,生成紫红色溶液。由此推断,酸性条件下, 与双氧水反应的离子方程式为
与双氧水反应的离子方程式为______ 。
(1)过氧化钙:
(2)过氧化氢:
(3)氢化钙
 价的氢离子)。
价的氢离子)。Ⅱ.纯净的过氧化钙
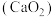 是一种新型水产养殖增氧剂,常用于鲜活水产品的运输,可以起到杀菌、供氧的作用。
是一种新型水产养殖增氧剂,常用于鲜活水产品的运输,可以起到杀菌、供氧的作用。(4)写出供氧的化学方程式:
Ⅲ.已知过一硫酸
 中硫为
中硫为 ,其第一步电离完全,第二步微弱。
,其第一步电离完全,第二步微弱。(5)每个
 分子中存在过氧键的数目为
分子中存在过氧键的数目为 价的氧原子之间形成一个过氧键)。
价的氧原子之间形成一个过氧键)。(6)下列有关
 的说法不正确的是________。
的说法不正确的是________。A. 是二元酸,是强电解质 是二元酸,是强电解质 |
B. 是正盐,溶液呈中性 是正盐,溶液呈中性 |
C. 与足量烧碱溶液反应的离子方程式为: 与足量烧碱溶液反应的离子方程式为: |
D. 具有强氧化性,能与 具有强氧化性,能与 反应 反应 |
(8)已知
 有
有 和
和 价,
价, 加入
加入 溶液中,生成紫红色溶液。由此推断,酸性条件下,
溶液中,生成紫红色溶液。由此推断,酸性条件下, 与双氧水反应的离子方程式为
与双氧水反应的离子方程式为
您最近一年使用:0次
7 . 亚硒酸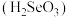 能与酸性
能与酸性 溶液发生如下反应:
溶液发生如下反应: 。下列叙述正确的是
。下列叙述正确的是
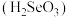 能与酸性
能与酸性 溶液发生如下反应:
溶液发生如下反应: 。下列叙述正确的是
。下列叙述正确的是A.氧化剂与还原剂的物质的量之比为 |
B.在该反应中 表现强氧化性 表现强氧化性 |
C. 完全反应转移 完全反应转移 电子 电子 |
D.分离产物中 宜采用分液操作 宜采用分液操作 |
您最近一年使用:0次
8 . 高纯纳米钛酸钡被广泛用于自动温控发热原件、PTC热敏电阻器件等领域,化工生产上以重晶石BaSO4为原料制备,生产流程如图所示,回答下列相关问题:________ 、________ 。
(2)科研发现,焦炭热还原重晶石反应过程在不同温度下其产物发生如图所示变化:________ (写出反应方程式即可),若该反应转移了2 mol电子,则氧化产物的质量为________ g;写出400℃时反应的方程式________________ 。
(3)生产流程中“系列操作”为________ 、冷却结晶、过滤等。该操作若在实验室中完成,下列仪器一定使用不到的是________ (填写仪器名称)。________ (无需标注反应条件),有人认为该反应属于氧化还原反应,试评价该观点是否正确,说出理由________________ 。
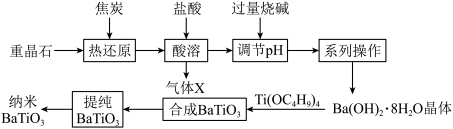
(2)科研发现,焦炭热还原重晶石反应过程在不同温度下其产物发生如图所示变化:
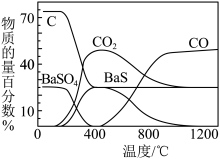
(3)生产流程中“系列操作”为
您最近一年使用:0次
2024-09-15更新
|
32次组卷
|
2卷引用:安徽省十校联盟2024-2025学年高二上学期9月份开学考试化学试题
名校
9 .  分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。(700℃左右有两个吸热峰。)
分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。(700℃左右有两个吸热峰。)
 分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。(700℃左右有两个吸热峰。)
分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。(700℃左右有两个吸热峰。)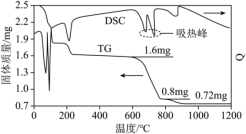
| A.0~400℃范围内,发生了化学变化 | B.600~800℃范围内,没有氧化还原反应发生 |
C.1000℃时,剩余固体的成分为 | D. 分解生成的气体可以用于制硫酸 分解生成的气体可以用于制硫酸 |
您最近一年使用:0次
2024-09-15更新
|
127次组卷
|
2卷引用:黑龙江省哈尔滨市第三中学校2024-2025学年高三上学期8月月考化学试卷
解题方法
10 . “价—类二维图”是学习元素及其化合物知识的高效模型。回答问题:_______ (填标号)。
①b有多种同素异形体
②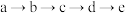 的转化均为氧化还原反应
的转化均为氧化还原反应
③将A持续通入石蕊溶液,溶液先变红后褪色
④ 的转化中,可通过加入还原剂实现
的转化中,可通过加入还原剂实现
(2)a是一种“臭名昭著”的有毒气体。用足量 溶液吸收
溶液吸收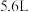 的a气体(标准状况),所消耗
的a气体(标准状况),所消耗 物质的量为
物质的量为_______  。
。
(3)d溶于水可得到_______ (填化学式),其冷的浓溶液可用以下金属容器储存的是_______ (填标号)。
① ②
② ③
③ ④
④
(4)向c(含硫物质)的水溶液中通入B,溶液的导电性会_______ (填“增强”、“不变”、“减弱”),写出该反应的离子方程式_______ 。
(5)D被称为百毒净,可用于自来水的消毒。根据D在上图中的位置,推断D的化学式为_______ 。制取D的微观过程如下图所示:_______ 。
(6)B和E(E是一种钠盐)均能将电镀废水中的氰化钠 做无害化处理,自身被还原为
做无害化处理,自身被还原为 。处理相同量的氰化钠,所需B的物质的量是E的
。处理相同量的氰化钠,所需B的物质的量是E的_______ 倍。
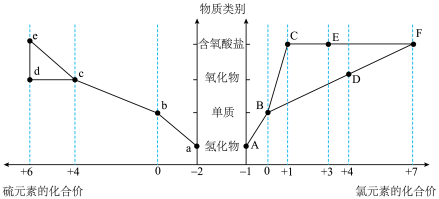
①b有多种同素异形体
②
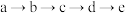 的转化均为氧化还原反应
的转化均为氧化还原反应③将A持续通入石蕊溶液,溶液先变红后褪色
④
 的转化中,可通过加入还原剂实现
的转化中,可通过加入还原剂实现(2)a是一种“臭名昭著”的有毒气体。用足量
 溶液吸收
溶液吸收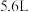 的a气体(标准状况),所消耗
的a气体(标准状况),所消耗 物质的量为
物质的量为 。
。(3)d溶于水可得到
①
 ②
② ③
③ ④
④
(4)向c(含硫物质)的水溶液中通入B,溶液的导电性会
(5)D被称为百毒净,可用于自来水的消毒。根据D在上图中的位置,推断D的化学式为
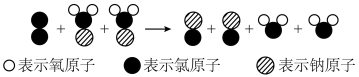
(6)B和E(E是一种钠盐)均能将电镀废水中的氰化钠
 做无害化处理,自身被还原为
做无害化处理,自身被还原为 。处理相同量的氰化钠,所需B的物质的量是E的
。处理相同量的氰化钠,所需B的物质的量是E的
您最近一年使用:0次



