名校
1 . 自来水是自然界中的淡水经过絮凝、沉淀、过滤、消毒等工艺处理后得到的。高铁酸钾(K2FeO4,极易溶于水)是常见的水处理剂,其原理如图所示。完成下列问题:
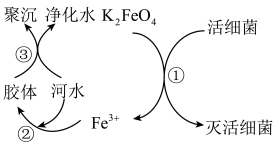
(1)K2FeO4的电离方程式______ 。过程①中K2FeO4表现了______ (填“氧化”或“还原”)性。
(2)根据上述原理分析,作水处理剂时,K2FeO4的作用有______ 、______ (填两个)。
(3)制备高铁酸钾常用的反应原理为:Fe(OH)3+KClO+KOH→K2FeO4+KCl+H2O(反应未配平)。
①通过该反应说明:在碱性条件下,氧化性KClO______ K2FeO4。
A.大于 B.小于 C.等于 D.无法比较
②配平该反应的化学方程式,并用单线桥法 表示电子转移的方向和数目说明______ ;
世界环保联盟要求ClO2逐渐取代Cl2作为自来水消毒剂
已知:NaCl+3H2O NaClO3+3H2↑
NaClO3+3H2↑
发生器:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
ClO2的生产流程示意图如图:
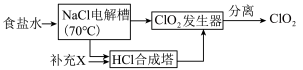
(4)该工艺中,需要补充的物质X为______ (填化学式,下同)。
(5)能参与循环的物质是______ 。
已知:ClO2是极易溶于水的气体,具有强氧化性。用如图装置探究ClO2性质。回答下列问题:
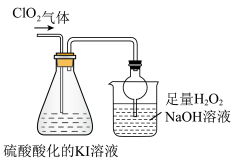
(6)锥形瓶内ClO2进气导管不伸入液面以下,原因是______ 。
(7)烧杯内液体用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是2:1,则还原产物的化学式是______ 。
反应后向锥形瓶中加入少量四氯化碳,溶液上下分层,下层为紫红色
已知:I2+Na2S=2NaI+S
(8)若将锥形瓶内溶液改为Na2S溶液,通入ClO2后溶液无明显现象。由此可以产生两种假设:
假设a:ClO2与Na2S不反应。假设b:ClO2与Na2S反应。
①你认为哪种假设正确,阐述原因:______ 。
②请设计实验证明你的假设(仅用离子方程式表示):______ 。

(1)K2FeO4的电离方程式
(2)根据上述原理分析,作水处理剂时,K2FeO4的作用有
(3)制备高铁酸钾常用的反应原理为:Fe(OH)3+KClO+KOH→K2FeO4+KCl+H2O(反应未配平)。
①通过该反应说明:在碱性条件下,氧化性KClO
A.大于 B.小于 C.等于 D.无法比较
②配平该反应的化学方程式,并用
世界环保联盟要求ClO2逐渐取代Cl2作为自来水消毒剂
已知:NaCl+3H2O
 NaClO3+3H2↑
NaClO3+3H2↑发生器:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
ClO2的生产流程示意图如图:

(4)该工艺中,需要补充的物质X为
(5)能参与循环的物质是
已知:ClO2是极易溶于水的气体,具有强氧化性。用如图装置探究ClO2性质。回答下列问题:

(6)锥形瓶内ClO2进气导管不伸入液面以下,原因是
(7)烧杯内液体用于吸收尾气,若反应的氧化产物是一种单质,且氧化剂与氧化产物的物质的量之比是2:1,则还原产物的化学式是
反应后向锥形瓶中加入少量四氯化碳,溶液上下分层,下层为紫红色
已知:I2+Na2S=2NaI+S
(8)若将锥形瓶内溶液改为Na2S溶液,通入ClO2后溶液无明显现象。由此可以产生两种假设:
假设a:ClO2与Na2S不反应。假设b:ClO2与Na2S反应。
①你认为哪种假设正确,阐述原因:
②请设计实验证明你的假设(仅用离子方程式表示):
您最近一年使用:0次
2023-03-04更新
|
304次组卷
|
2卷引用:上海市杨浦高级中学2022-2023学年高一上学期期末考试化学试题
名校
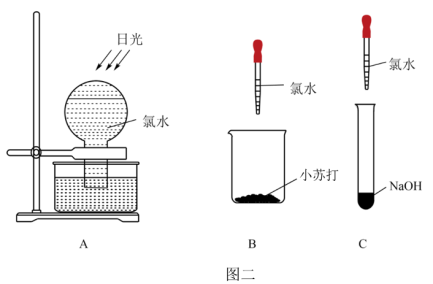
2 . 某化学兴趣小组为了探究 的相关性质,设计了如图一的一系列实验。
的相关性质,设计了如图一的一系列实验。

查阅资料:① 与
与 不反应;
不反应;
②氯元素形成物质的二维价类图如下所示:
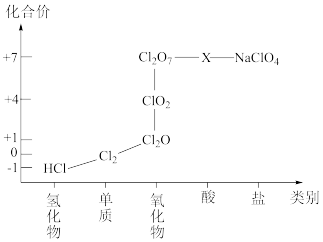
(1)根据二维图中信息,写出氯的最高价含氧酸的化学式_______ 。
(2)将 通入水中,其离子方程式为
通入水中,其离子方程式为_______ 。
(3)实验室可用该反应 制备
制备 ,该反应中盐酸体现
,该反应中盐酸体现_______ (填字母),其中氧化剂与还原剂的微粒个数之比为_______ 。
A.酸性 B.氧化性 C.还原性 D.挥发性
(4)图一中,通入_______ 后,从集气瓶A、B的现象可得出的结论是_______ 。
(5)图二中三组实验,不会产生气体的是_______ ﹔请用一个离子方程式表示图二B装置中发生的反应_______ 。
 的相关性质,设计了如图一的一系列实验。
的相关性质,设计了如图一的一系列实验。
查阅资料:①
 与
与 不反应;
不反应;②氯元素形成物质的二维价类图如下所示:

(1)根据二维图中信息,写出氯的最高价含氧酸的化学式
(2)将
 通入水中,其离子方程式为
通入水中,其离子方程式为(3)实验室可用该反应
 制备
制备 ,该反应中盐酸体现
,该反应中盐酸体现A.酸性 B.氧化性 C.还原性 D.挥发性
(4)图一中,通入
(5)图二中三组实验,不会产生气体的是

您最近一年使用:0次
2022-11-13更新
|
247次组卷
|
2卷引用:重庆市第八中学校2022-2023学年高一上学期期中考试(半期考试)化学试题
名校
解题方法
3 . 某化学兴趣小组利用下图装置(部分夹持装置省略)制备氯气并探究其性质:
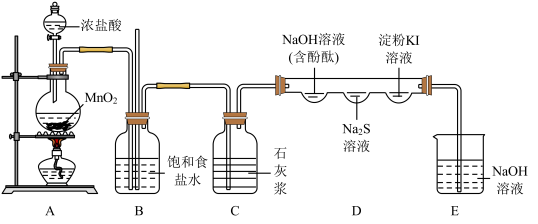
回答以下问题:
(1)装置A中发生反应的离子方程式为_______ ,0.4 mol HCl发生反应时,转移电子的物质的量为_______ 。
(2)利用装置C模拟工业制备漂白粉,写出该反应的化学方程式_______ 。若C中导管口堵塞,则B中观察到的现象是_______ 。
(3)实验进行一段时间后,装置D中含酚酞的NaOH溶液红色逐渐褪去,产生该现象的原因可能为:①氯气溶于水呈酸性,与氢氧化钠发生中和反应使溶液褪色;②_______ 。
(4)随着反应进行,装置D中 溶液处观察到的现象为
溶液处观察到的现象为_______ ;淀粉KI溶液处先变蓝后褪色,原因是氯气氧化碘单质生成 ,写出褪色过程的化学方程式
,写出褪色过程的化学方程式_______ 。
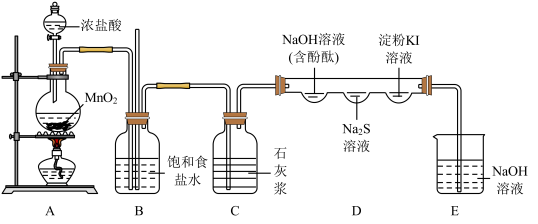
回答以下问题:
(1)装置A中发生反应的离子方程式为
(2)利用装置C模拟工业制备漂白粉,写出该反应的化学方程式
(3)实验进行一段时间后,装置D中含酚酞的NaOH溶液红色逐渐褪去,产生该现象的原因可能为:①氯气溶于水呈酸性,与氢氧化钠发生中和反应使溶液褪色;②
(4)随着反应进行,装置D中
 溶液处观察到的现象为
溶液处观察到的现象为 ,写出褪色过程的化学方程式
,写出褪色过程的化学方程式
您最近一年使用:0次
2023-02-10更新
|
362次组卷
|
2卷引用:山东省潍坊市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
4 . 铁及其化合物的制备与性质探究。
I.乳酸亚铁[CH3CH(OH)COO]2Fe是一种常见的补血剂,可由FeCO3与乳酸反应制得,实验室经常采用如下装置制备FeCO3(夹持装置略)。
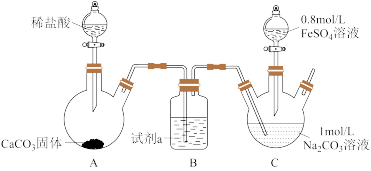
具体实验流程如下:装置C中,先通入CO2至pH约为7,滴加一定量FeSO4,将所得白色沉淀过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a为_______ 。
(2)写出整个实验过程中C中发生反应的离子方程式_______ 。
(3)某实验小组用酸性高锰酸钾标准液去测定补血剂中乳酸亚铁含量,从而计算乳酸亚铁的质量分数,经过反复多次测定乳酸亚铁的质量分数总是大于100%,其原因是_______ 。
II.无水FeCl3是一种常见的化工原料,实验室可采用下列装置制备。
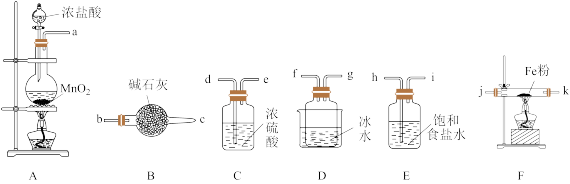
已知:①FeCl3极易水解;②FeCl3在300℃以上升华。
(4)装置的连接顺序为a→_______ →j→k→_______ (按气流方向,用小写字母表示)。
(5)将所得无水FeCl3溶于_______ 可得FeCl3溶液,FeCl3溶液是一种常用的创伤止血剂,其止血原理为_______ 。
(6)某兴趣小组在FeCl3溶液中通入SO2,观察到的主要现象为随着SO2的通入,溶液迅速由黄色变为红棕色,静置一小时后溶液变为浅绿色。通过查阅资料得知,溶液中主要有两种变化,第一种:Fe2+与SO2会生成一种络合物[Fe(SO2)6]3+(红棕色);第二种:Fe3+与SO2发生氧化还原反应。
①写出第二种情况下反应的离子方程式:_______ 。
②这两种反应平衡常数的大小关系为K1_______ K2(填“<”“>”或“=”)。
I.乳酸亚铁[CH3CH(OH)COO]2Fe是一种常见的补血剂,可由FeCO3与乳酸反应制得,实验室经常采用如下装置制备FeCO3(夹持装置略)。

具体实验流程如下:装置C中,先通入CO2至pH约为7,滴加一定量FeSO4,将所得白色沉淀过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a为
(2)写出整个实验过程中C中发生反应的离子方程式
(3)某实验小组用酸性高锰酸钾标准液去测定补血剂中乳酸亚铁含量,从而计算乳酸亚铁的质量分数,经过反复多次测定乳酸亚铁的质量分数总是大于100%,其原因是
II.无水FeCl3是一种常见的化工原料,实验室可采用下列装置制备。

已知:①FeCl3极易水解;②FeCl3在300℃以上升华。
(4)装置的连接顺序为a→
(5)将所得无水FeCl3溶于
(6)某兴趣小组在FeCl3溶液中通入SO2,观察到的主要现象为随着SO2的通入,溶液迅速由黄色变为红棕色,静置一小时后溶液变为浅绿色。通过查阅资料得知,溶液中主要有两种变化,第一种:Fe2+与SO2会生成一种络合物[Fe(SO2)6]3+(红棕色);第二种:Fe3+与SO2发生氧化还原反应。
①写出第二种情况下反应的离子方程式:
②这两种反应平衡常数的大小关系为K1
您最近一年使用:0次
解题方法
5 . 某化学兴趣小组利用如图所示装置制备饱和氯水,并探究新制饱和氯水的性质及其中氯元素的含量。请回答下列问题:

(1)仪器 的名称为
的名称为_______ , 中发生反应的离子方程式为
中发生反应的离子方程式为_______ 。
(2)装置乙盛装的试剂为_______ ,装置丁的作用为_______ 。
(3)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还有很多其他方法,如利用高锰酸钾和浓盐酸反应: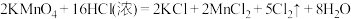 ,该反应每消耗
,该反应每消耗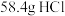 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为_______ mol。
(4)已知: 可将
可将 氧化为
氧化为 ,
, 遇淀粉变蓝。现将新制的饱和氯水逐滴滴入淀粉—
遇淀粉变蓝。现将新制的饱和氯水逐滴滴入淀粉— 溶液中至过量,可观察到现象:溶液先变蓝后褪色。出现该现象的原因是
溶液中至过量,可观察到现象:溶液先变蓝后褪色。出现该现象的原因是_______ (用离子方程式解释,下同)、_______ ,由该实验可知氧化性:
_______ (填“>”或“<”) 。
。
(5)测定新制饱和氯水中氯元素的含量:量取 新制饱和氯水,置于光照条件下至溶液中只含1种溶质(不考虑
新制饱和氯水,置于光照条件下至溶液中只含1种溶质(不考虑 挥发),加入足量
挥发),加入足量 溶液,过滤、洗涤、干燥、称重,最终得到
溶液,过滤、洗涤、干燥、称重,最终得到 沉淀,则该新制饱和氯水中氯元素的含量为
沉淀,则该新制饱和氯水中氯元素的含量为_______ (用含 的代数式表示)
的代数式表示) 。
。

(1)仪器
 的名称为
的名称为 中发生反应的离子方程式为
中发生反应的离子方程式为(2)装置乙盛装的试剂为
(3)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还有很多其他方法,如利用高锰酸钾和浓盐酸反应:
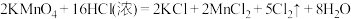 ,该反应每消耗
,该反应每消耗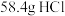 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为(4)已知:
 可将
可将 氧化为
氧化为 ,
, 遇淀粉变蓝。现将新制的饱和氯水逐滴滴入淀粉—
遇淀粉变蓝。现将新制的饱和氯水逐滴滴入淀粉— 溶液中至过量,可观察到现象:溶液先变蓝后褪色。出现该现象的原因是
溶液中至过量,可观察到现象:溶液先变蓝后褪色。出现该现象的原因是
 。
。(5)测定新制饱和氯水中氯元素的含量:量取
 新制饱和氯水,置于光照条件下至溶液中只含1种溶质(不考虑
新制饱和氯水,置于光照条件下至溶液中只含1种溶质(不考虑 挥发),加入足量
挥发),加入足量 溶液,过滤、洗涤、干燥、称重,最终得到
溶液,过滤、洗涤、干燥、称重,最终得到 沉淀,则该新制饱和氯水中氯元素的含量为
沉淀,则该新制饱和氯水中氯元素的含量为 的代数式表示)
的代数式表示) 。
。
您最近一年使用:0次
名校
解题方法
6 . 物质的大小会对其性质有极大影响。
(1)纳米金:具有高电子密度、介电特性和催化作用。纳米金的制法:将0.01%的 溶液煮沸,迅速加入1%的柠檬酸钠(
溶液煮沸,迅速加入1%的柠檬酸钠( )溶液,持续煮沸7~10分钟。制备时溶液会因为加入的柠檬酸钠的量不同而产生不同的颜色,如下表所示。
)溶液,持续煮沸7~10分钟。制备时溶液会因为加入的柠檬酸钠的量不同而产生不同的颜色,如下表所示。
资料: 的溶液呈黄色,其酸性比柠檬酸强。
的溶液呈黄色,其酸性比柠檬酸强。
①在制备过程中,存在如下反应,已知产物 是柠檬酸脱去一个羧基得到的,核磁共振氢谱显示其有4组峰。请补全并配平下面的反应方程式(要写出
是柠檬酸脱去一个羧基得到的,核磁共振氢谱显示其有4组峰。请补全并配平下面的反应方程式(要写出 的结构简式)
的结构简式) _______ 。
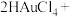 □
□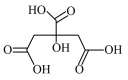 →□_______+□_______(
→□_______+□_______( )+□
)+□ +□HCl
+□HCl
②柠檬酸钠的作用是_______ ,如果一段时间后的液体仍为黄色,则可以_______ (填操作)来检验是否生成纳米金。
(2)微米水:可以高效诱导分子的还原反应,且不需要任何的外加还原剂或外加电荷。科学家使用上述方法制取纳米金时,引入了不加柠檬酸的对照组。令人惊奇的是对照组也发生了反应,他经过猜想与论证,最终将目光锁定在水身上,用如下装置(如图1所示)进行验证。

①使用丙酮酸( )来验证,通过检验由丙酮酸生成的产物
)来验证,通过检验由丙酮酸生成的产物_______ ,证明猜想成立。
②发现随着丙酮酸浓度的增加,还原效率会迅速降低,图2与图3中丙酮酸浓度均为10mol/L。

还原效率会随着雾化气体压强的增大而增大的原因是_______ 。
③为探究还原反应的具体过程,继续设计实验:向水中加入一种指示剂R,这种指示剂正常状态下不显色,R在遇到一定浓度的 与还原剂后会显示红色荧光,过程可以表示为:R(无色)
与还原剂后会显示红色荧光,过程可以表示为:R(无色) (红色荧光)。加入R后观测到的现象如图4所示。
(红色荧光)。加入R后观测到的现象如图4所示。

结合图4和上述实验,你可以得出什么推论?_______ 。
(3)综合上述内容,你对物质有了哪些更深入的认识?_______ 。
(1)纳米金:具有高电子密度、介电特性和催化作用。纳米金的制法:将0.01%的
 溶液煮沸,迅速加入1%的柠檬酸钠(
溶液煮沸,迅速加入1%的柠檬酸钠( )溶液,持续煮沸7~10分钟。制备时溶液会因为加入的柠檬酸钠的量不同而产生不同的颜色,如下表所示。
)溶液,持续煮沸7~10分钟。制备时溶液会因为加入的柠檬酸钠的量不同而产生不同的颜色,如下表所示。| 纳米金颗粒大小(nm) | 颜色 |
| 2~5 | 黄 |
| 10~20 | 红 |
| 30~80 | 紫 |
 的溶液呈黄色,其酸性比柠檬酸强。
的溶液呈黄色,其酸性比柠檬酸强。①在制备过程中,存在如下反应,已知产物
 是柠檬酸脱去一个羧基得到的,核磁共振氢谱显示其有4组峰。请补全并配平下面的反应方程式(要写出
是柠檬酸脱去一个羧基得到的,核磁共振氢谱显示其有4组峰。请补全并配平下面的反应方程式(要写出 的结构简式)
的结构简式) 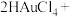 □
□ →□_______+□_______(
→□_______+□_______( )+□
)+□ +□HCl
+□HCl②柠檬酸钠的作用是
(2)微米水:可以高效诱导分子的还原反应,且不需要任何的外加还原剂或外加电荷。科学家使用上述方法制取纳米金时,引入了不加柠檬酸的对照组。令人惊奇的是对照组也发生了反应,他经过猜想与论证,最终将目光锁定在水身上,用如下装置(如图1所示)进行验证。

①使用丙酮酸(
 )来验证,通过检验由丙酮酸生成的产物
)来验证,通过检验由丙酮酸生成的产物②发现随着丙酮酸浓度的增加,还原效率会迅速降低,图2与图3中丙酮酸浓度均为10mol/L。

还原效率会随着雾化气体压强的增大而增大的原因是
③为探究还原反应的具体过程,继续设计实验:向水中加入一种指示剂R,这种指示剂正常状态下不显色,R在遇到一定浓度的
 与还原剂后会显示红色荧光,过程可以表示为:R(无色)
与还原剂后会显示红色荧光,过程可以表示为:R(无色) (红色荧光)。加入R后观测到的现象如图4所示。
(红色荧光)。加入R后观测到的现象如图4所示。
结合图4和上述实验,你可以得出什么推论?
(3)综合上述内容,你对物质有了哪些更深入的认识?
您最近一年使用:0次
2022-05-31更新
|
262次组卷
|
2卷引用:北京市东城区第五中学2022届高三三模化学试题
名校
7 . 利用 氧化绿色的
氧化绿色的 浓强碱溶液制备
浓强碱溶液制备 的装置如下图所示(加热、夹持装置略):
的装置如下图所示(加热、夹持装置略):_______ 。
(2)如果d中用足量的 溶液吸收多余氯气,写出相应的离子方程式:
溶液吸收多余氯气,写出相应的离子方程式:_______ 。
(3)一段时间后,当仪器C中_______ (填实验现象)即停止通氯气。熄灭 处酒精灯,再
处酒精灯,再_______ ,待冷却后拆除装置。
(4)某同学在实验中发现,若用稀盐酸代替浓盐酸与 混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:
混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:
假设1: 的浓度不够大;
的浓度不够大;
假设2:_______ ;
假设3: 和
和 的浓度均不够大。
的浓度均不够大。
设计实验方案,进行实验。在下表中写出实验步骤以及预期现象和结论。(限选实验试剂:蒸馏水、浓 、
、 固体、
固体、 固体、稀盐酸、
固体、稀盐酸、 溶液、淀粉-KI溶液)
溶液、淀粉-KI溶液)
(5)医学上常用酸性 溶液和草酸(
溶液和草酸( )溶液反应(实验中会生成
)溶液反应(实验中会生成 )来测血液中血钙的含量。测定方法是取
)来测血液中血钙的含量。测定方法是取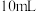 血液用蒸馏水稀释后,向其中加入足量的
血液用蒸馏水稀释后,向其中加入足量的 溶液,反应生成
溶液,反应生成 沉淀,将沉淀用稀硫酸溶解并不断搅拌得到
沉淀,将沉淀用稀硫酸溶解并不断搅拌得到 后,再滴入
后,再滴入 溶液进行反应,反应完全时消耗了
溶液进行反应,反应完全时消耗了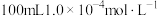 的
的 溶液(相关反应的方程式为:
溶液(相关反应的方程式为: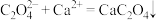 、
、 、
、
 。则
。则 该血液中含钙
该血液中含钙_______ g。
 氧化绿色的
氧化绿色的 浓强碱溶液制备
浓强碱溶液制备 的装置如下图所示(加热、夹持装置略):
的装置如下图所示(加热、夹持装置略):
(2)如果d中用足量的
 溶液吸收多余氯气,写出相应的离子方程式:
溶液吸收多余氯气,写出相应的离子方程式:(3)一段时间后,当仪器C中
 处酒精灯,再
处酒精灯,再(4)某同学在实验中发现,若用稀盐酸代替浓盐酸与
 混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:
混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:假设1:
 的浓度不够大;
的浓度不够大;假设2:
假设3:
 和
和 的浓度均不够大。
的浓度均不够大。设计实验方案,进行实验。在下表中写出实验步骤以及预期现象和结论。(限选实验试剂:蒸馏水、浓
 、
、 固体、
固体、 固体、稀盐酸、
固体、稀盐酸、 溶液、淀粉-KI溶液)
溶液、淀粉-KI溶液)| 实验步骤 | 预期现象与结论 |
步骤1:取少量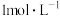 稀盐酸于试管A中,加入少量 稀盐酸于试管A中,加入少量 ,滴加几滴浓硫酸,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 ,滴加几滴浓硫酸,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 | ①若淀粉-KI溶液变蓝,则假设1成立 ②若淀粉-KI溶液不变蓝,则假设2或假设3成立 |
步骤2:取少量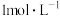 稀盐酸于试管B中,加入少量 稀盐酸于试管B中,加入少量 ,加入少量NaCl固体,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 ,加入少量NaCl固体,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 | ①若淀粉-KI溶液变蓝,则 ②若淀粉-KI溶液不变蓝,结合步骤1中的结论②,则 |
(5)医学上常用酸性
 溶液和草酸(
溶液和草酸( )溶液反应(实验中会生成
)溶液反应(实验中会生成 )来测血液中血钙的含量。测定方法是取
)来测血液中血钙的含量。测定方法是取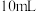 血液用蒸馏水稀释后,向其中加入足量的
血液用蒸馏水稀释后,向其中加入足量的 溶液,反应生成
溶液,反应生成 沉淀,将沉淀用稀硫酸溶解并不断搅拌得到
沉淀,将沉淀用稀硫酸溶解并不断搅拌得到 后,再滴入
后,再滴入 溶液进行反应,反应完全时消耗了
溶液进行反应,反应完全时消耗了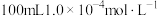 的
的 溶液(相关反应的方程式为:
溶液(相关反应的方程式为: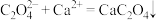 、
、 、
、
 。则
。则 该血液中含钙
该血液中含钙
您最近一年使用:0次
2022-12-14更新
|
81次组卷
|
4卷引用:山西省晋城二中2022-2023学年高一上学期12月(第三次)月考化学试题
8 . 以含硫废水(主要含有Na2S和Na2SO3) 为原料制备Na2S2O3· 5H2O。

(1)制备Na2S2O3· 5H2O。反应前先向三颈烧瓶(装置见图)中通入SO2气体,一段时间后,再向其中加入含硫废水(Na2S和Na2SO3混合溶液),加热,充分反应,直至烧瓶中溶液变澄清为止。所得溶液经蒸发浓缩、冷却结晶、过滤、洗涤、真空干燥后即得到产品。
①三颈烧瓶中SO2与Na2S、Na2SO3溶液[假设其中n(Na2S) : n(Na2SO3)=2:1] 反应生成Na2S2O3的其化学方程式为___________ 。
②先向三颈烧瓶中通入SO2气体后,再滴加含硫废水的原因是___________ 。
③NaOH溶液的作用是___________ 。
(2)测定某样品中NaClO2的质量分数。取样品0.2000g溶于水配成100mL溶液,取出20.00 mL溶液于锥形瓶中,再加入足量硫酸酸化的KI溶液,充分反应后(NaClO2被还原为Cl-,其它物质不参加反应),加入2~3滴淀粉溶液,然后再用0.1000 mol·L-1Na2S2O3;标准溶液滴定,经3次测定,每次消耗Na2S2O3标准溶液的体积如下:
已知:Na2S2O3+ I2=Na2S4O6+ 2NaI
①滴定终点的现象为___________ 。
②计算该样品中NaClO2的质量分数为___________ 。( 写出计算过程!)

(1)制备Na2S2O3· 5H2O。反应前先向三颈烧瓶(装置见图)中通入SO2气体,一段时间后,再向其中加入含硫废水(Na2S和Na2SO3混合溶液),加热,充分反应,直至烧瓶中溶液变澄清为止。所得溶液经蒸发浓缩、冷却结晶、过滤、洗涤、真空干燥后即得到产品。
①三颈烧瓶中SO2与Na2S、Na2SO3溶液[假设其中n(Na2S) : n(Na2SO3)=2:1] 反应生成Na2S2O3的其化学方程式为
②先向三颈烧瓶中通入SO2气体后,再滴加含硫废水的原因是
③NaOH溶液的作用是
(2)测定某样品中NaClO2的质量分数。取样品0.2000g溶于水配成100mL溶液,取出20.00 mL溶液于锥形瓶中,再加入足量硫酸酸化的KI溶液,充分反应后(NaClO2被还原为Cl-,其它物质不参加反应),加入2~3滴淀粉溶液,然后再用0.1000 mol·L-1Na2S2O3;标准溶液滴定,经3次测定,每次消耗Na2S2O3标准溶液的体积如下:
| 实验序号 | 1 | 2 | 3 |
| 消耗Na2S2O3标准溶液的体积(mL) | 16.02 | 15.98 | 17.02 |
①滴定终点的现象为
②计算该样品中NaClO2的质量分数为
您最近一年使用:0次
名校
9 . 工业上,利用黄铁矿(主要成分是 )制备硫酸以及冶炼铁,其简易流程如下:
)制备硫酸以及冶炼铁,其简易流程如下:
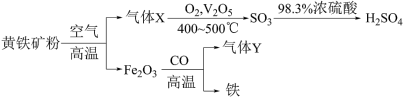
请回答下列问题:
(1)气体Y的相对分子质量为44,气体Y的电子式为_______ 。
(2)气体X转化成 的反应是放热反应,则参与反应的气体X和
的反应是放热反应,则参与反应的气体X和 的总能量
的总能量_______ (填“高于”“低于”或“等于”)生成的 的总能量。用
的总能量。用 的浓硫酸吸收
的浓硫酸吸收 ,避免直接与水反应形成大量酸雾,污染环境,反应的能量变化如图所示。由此可知:
,避免直接与水反应形成大量酸雾,污染环境,反应的能量变化如图所示。由此可知: 是
是_______ (填“放热”或“吸热”)反应。

(3)配平下列方程式并推断X的化学式:_______ ,_______ _______
_______ _______
_______ _______X。X的化学式是
_______X。X的化学式是_______ 。
(4)向 溶液中通入气体X,没有明显现象,再通入
溶液中通入气体X,没有明显现象,再通入 ,产生白色沉淀,该白色沉淀是
,产生白色沉淀,该白色沉淀是_______ (填化学式)。
(5)铁片和铜片在稀硫酸中构成原电池,装置如图所示。可观察到正极表面上实验现象有_______ 。写出负极的电极反应式:_______ 。

(6)在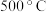 时,向
时,向 恒容密闭容器中充入
恒容密闭容器中充入 和
和 发生反应:
发生反应: ,经过
,经过 达到平衡,测得生成
达到平衡,测得生成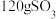 。
。
①反应开始到平衡时 的平均反应速率为
的平均反应速率为_______  。
。
②在该条件下, 的平衡转化率为
的平衡转化率为_______ 。
 )制备硫酸以及冶炼铁,其简易流程如下:
)制备硫酸以及冶炼铁,其简易流程如下: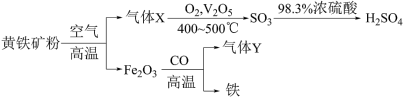
请回答下列问题:
(1)气体Y的相对分子质量为44,气体Y的电子式为
(2)气体X转化成
 的反应是放热反应,则参与反应的气体X和
的反应是放热反应,则参与反应的气体X和 的总能量
的总能量 的总能量。用
的总能量。用 的浓硫酸吸收
的浓硫酸吸收 ,避免直接与水反应形成大量酸雾,污染环境,反应的能量变化如图所示。由此可知:
,避免直接与水反应形成大量酸雾,污染环境,反应的能量变化如图所示。由此可知: 是
是
(3)配平下列方程式并推断X的化学式:
 _______
_______ _______
_______ _______X。X的化学式是
_______X。X的化学式是(4)向
 溶液中通入气体X,没有明显现象,再通入
溶液中通入气体X,没有明显现象,再通入 ,产生白色沉淀,该白色沉淀是
,产生白色沉淀,该白色沉淀是(5)铁片和铜片在稀硫酸中构成原电池,装置如图所示。可观察到正极表面上实验现象有

(6)在
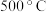 时,向
时,向 恒容密闭容器中充入
恒容密闭容器中充入 和
和 发生反应:
发生反应: ,经过
,经过 达到平衡,测得生成
达到平衡,测得生成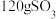 。
。①反应开始到平衡时
 的平均反应速率为
的平均反应速率为 。
。②在该条件下,
 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
10 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。

回答下列问题:
(1)盛放浓盐酸的仪器名称是_____ 。
(2)工业上以碘和氯酸钾为原料进行生产。已知氧化产物为KH(IO3)2同时生成的两种还原产物得到的电子数相同,且还原产物为黄绿色气体和无氧酸盐,则反应的化学方程式为____ 。
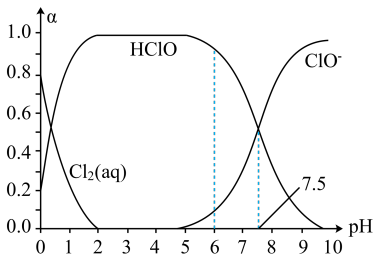
(3)新制氯水常用于杀菌消毒,在25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-的物质的量分数(α)随pH变化的关系如图所示。①由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=____ 时杀菌效果强。当pH=7.5时,氯水中含氯元素的微粒有_____ 。
②将氯水滴在蓝色石蕊试纸上,发生的现象:____ ,说明氯水具有____ (填性质)。
(4)资料查得:“84消毒液”与双氧水混合会反应产生一种常见的无色无味气体,且消毒能力大大降低,写出该反应的离子方程式____ 。

回答下列问题:
(1)盛放浓盐酸的仪器名称是
(2)工业上以碘和氯酸钾为原料进行生产。已知氧化产物为KH(IO3)2同时生成的两种还原产物得到的电子数相同,且还原产物为黄绿色气体和无氧酸盐,则反应的化学方程式为
(3)新制氯水常用于杀菌消毒,在25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-的物质的量分数(α)随pH变化的关系如图所示。①由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=

②将氯水滴在蓝色石蕊试纸上,发生的现象:
(4)资料查得:“84消毒液”与双氧水混合会反应产生一种常见的无色无味气体,且消毒能力大大降低,写出该反应的离子方程式
您最近一年使用:0次



