名校
解题方法
1 . 加碘食盐中的碘以KIO3形式存在。根据反应:IO +5I-+6H+=3I2+3H2O,可用碘化钾淀粉试纸和食醋进行实验,证明食盐中存在IO
+5I-+6H+=3I2+3H2O,可用碘化钾淀粉试纸和食醋进行实验,证明食盐中存在IO 。下列说法错误的是
。下列说法错误的是
 +5I-+6H+=3I2+3H2O,可用碘化钾淀粉试纸和食醋进行实验,证明食盐中存在IO
+5I-+6H+=3I2+3H2O,可用碘化钾淀粉试纸和食醋进行实验,证明食盐中存在IO 。下列说法错误的是
。下列说法错误的是| A.实验时可观察到试纸变为蓝色 |
B.实验可证明该条件下氧化性:IO > I2 > I2 |
| C.每生成3mol I2转移电子的物质的量6mol |
D.该反应中IO 作氧化剂,发生还原反应 作氧化剂,发生还原反应 |
您最近一年使用:0次
2021-02-08更新
|
123次组卷
|
4卷引用:江西省永丰县永丰中学2020-2021学年高一上学期期中考试化学试题
名校
2 . 食盐中所加的碘以碘酸钾(KIO3)形式存在。根据反应:IO +I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO
+I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO 。下列说法不正确的是
。下列说法不正确的是
 +I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO
+I-+H+→I2+H2O(未配平),可用KI淀粉试纸和食醋进行实验,证明加碘食盐中存在IO 。下列说法不正确的是
。下列说法不正确的是| A.上述反应中氧化剂和还原剂的物质的量之比为1∶5 |
| B.实验时可观察到试纸变蓝 |
| C.实验可证明该条件下I-的还原性强于Cl- |
| D.食醋中含有的乙酸是强酸,它能提供反应所需的H+ |
您最近一年使用:0次
2020-07-04更新
|
322次组卷
|
5卷引用:江西省南昌市豫章中学20212-2022学年高一下学期第一次月考化学试题
江西省南昌市豫章中学20212-2022学年高一下学期第一次月考化学试题北京市东城区北京景山学校2019~2020学年高一下学期期末考试化学试题贵州省铜仁市伟才学校2019-2020学年高一下学期期末考试化学(理)试题黑龙江省大庆市肇州县第二中学2019-2020学年高一下学期期末考试化学试题(已下线)1.3.4 氧化还原反应方程式的配平-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)
3 . 查阅资料得知MnO2+NaBr+H2SO4→Na2SO4+MnSO4+Br2↑+H2O(未配平)。某兴趣小组的同学利用如图所示的装置探究苯与液溴的反应类型。下列说法正确的是


| A.实验装置的连接顺序为c→a→d→b,b中产生淡黄色沉淀,证明苯与液溴发生的是取代反应 |
| B.装置c中发生反应的还原剂与氧化剂物质的量之比为2∶1 |
| C.装置d中仪器G的名称为直形冷凝管 |
| D.反应后装置d中混合液经碱洗、分液后,上层液体蒸馏得到溴苯 |
您最近一年使用:0次
名校
解题方法
4 . 某学习小组探究不同含硫物质的转化。
任务I.从以下试剂中选择合适的试剂完成 →
→ 的转化。
的转化。
试剂:①浓H2SO4②稀H2SO4③酸性KMnO4溶液 ④Na2SO3溶液 ⑤Cu ⑥品红溶液
(1)写出完成转化的化学方程式:_____ 。
(2)设计实验,证明实现该转化(写出操作和现象):_____ 。
任务II.完成硫元素在 、
、 、
、 价之间的转化。
价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
SO2 Na2SO3
Na2SO3 Na2S2O3
Na2S2O3 X
X
(3)①中加入的物质是_____ ,写出③的离子方程式:_____ 。
任务III.工业上常用空气催化氢氧化法除去电石渣浆(含CaO)上清液中的S2-,并制取石膏CaSO4•2H2O,其中的物质转化过程如图所示。

(4)过程II中,反应的离子方程式为_____ 。
(5)根据物质转化过程,若将10L上清液中的S2-转化为SO (S2-浓度为320mg/L),理论上共需要标准状况下的O2的体积为
(S2-浓度为320mg/L),理论上共需要标准状况下的O2的体积为_____ L。
任务I.从以下试剂中选择合适的试剂完成
 →
→ 的转化。
的转化。试剂:①浓H2SO4②稀H2SO4③酸性KMnO4溶液 ④Na2SO3溶液 ⑤Cu ⑥品红溶液
(1)写出完成转化的化学方程式:
(2)设计实验,证明实现该转化(写出操作和现象):
任务II.完成硫元素在
 、
、 、
、 价之间的转化。
价之间的转化。查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
SO2
 Na2SO3
Na2SO3 Na2S2O3
Na2S2O3 X
X(3)①中加入的物质是
任务III.工业上常用空气催化氢氧化法除去电石渣浆(含CaO)上清液中的S2-,并制取石膏CaSO4•2H2O,其中的物质转化过程如图所示。

(4)过程II中,反应的离子方程式为
(5)根据物质转化过程,若将10L上清液中的S2-转化为SO
 (S2-浓度为320mg/L),理论上共需要标准状况下的O2的体积为
(S2-浓度为320mg/L),理论上共需要标准状况下的O2的体积为
您最近一年使用:0次
解题方法
5 . 镓(Ga)被誉为“电子工业脊梁”,性质与铝相似。氮化镓(GaN)在5G基站和互联网系统建设等方面用途广泛。以砷化镓废料(主要成分是GaAs,含Fe2O3、Al2O3和CaCO3等杂质)制备GaN和Na3AsO4∙12H2O的流程如下:

请回答下列问题:
(1)滤渣2的主要成分是_______ (填化学式)。
(2)“碱浸”中发生主要反应的化学方程式为_______ ,在该反应中氧化剂和还原剂的物质的量之比为_______ 。
(3)“调pH2”时通入过量CO2,写出离子方程式:_______ 。操作a包括蒸发浓缩、降温结晶、过滤、洗涤、低温干燥,“低温干燥”的目的是_______ 。
(4)制备氮化镓时生成一种气体,它是_______ (填化学式)。
(5)制备氮化镓需要纯氨气,实验室制备氨气宜选择的装置是_______ (填字母)。
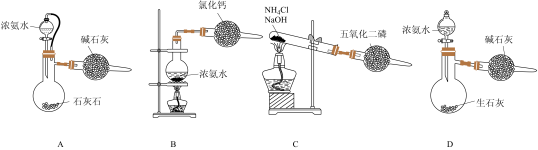
(6)设计简单实验证明滤液1是否含Fe3+:_______ 。

请回答下列问题:
(1)滤渣2的主要成分是
(2)“碱浸”中发生主要反应的化学方程式为
(3)“调pH2”时通入过量CO2,写出离子方程式:
(4)制备氮化镓时生成一种气体,它是
(5)制备氮化镓需要纯氨气,实验室制备氨气宜选择的装置是

(6)设计简单实验证明滤液1是否含Fe3+:
您最近一年使用:0次
名校
6 . 纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,以主要成分为CuFeS2的黄铜矿(含有杂质SiO2)为原料制取纳米Cu2O的一种工艺流程如图:

常温下几种金属氢氧化物的Ksp[Fe(OH)3]=8.0×10-38、Ksp[Fe(OH)2]=4.0×10-16、Ksp[Cu(OH)2]=2.0×10-19。
(1)X可以是O2、H2O2、Cl2等试剂,氧化等量的Fe2+时,消耗的三种氧化剂物质的量之比为____ ,浸泡后所得溶液中金属离子为Cu2+、Fe2+,写出相应的离子方程式____ 。
(2)试剂Y可以是____ ,浸泡后所得溶液中金属离子为Cu2+浓度为0.2mol/L,则pH的调控范围为____ 。
(3)若葡萄糖用RCHO表示,则热还原时反应的化学方程式为____ ,证明所得到的Cu2O是纳米级微粒的简单方法是____ 。

常温下几种金属氢氧化物的Ksp[Fe(OH)3]=8.0×10-38、Ksp[Fe(OH)2]=4.0×10-16、Ksp[Cu(OH)2]=2.0×10-19。
(1)X可以是O2、H2O2、Cl2等试剂,氧化等量的Fe2+时,消耗的三种氧化剂物质的量之比为
(2)试剂Y可以是
(3)若葡萄糖用RCHO表示,则热还原时反应的化学方程式为
您最近一年使用:0次
名校
7 . 氮及其化合物是中学化学重要内容,请回答下列问题:
(1)工商管理条例明文规定:食品生产经营者不得购进、存放、使用亚硝酸盐作为食品添加剂。亚硝酸钠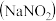 属于
属于 _______  填“氧化物”或“盐”
填“氧化物”或“盐” ,它是一种强氧化剂,与
,它是一种强氧化剂,与 共热生成
共热生成 ,是实验室制
,是实验室制 的方法,写出
的方法,写出 与
与 共热发生反应的化学方程式
共热发生反应的化学方程式 _______ 。若有 发生反应,则反应中电子转移的数目为
发生反应,则反应中电子转移的数目为 _______ 。
(2)亚硝酸钠外观与食盐相似,且均有咸味。某课外探究小组欲对亚硝酸钠与氯化钠进行鉴别,其鉴别方法如下:将样品放入稀硫酸与另外一种溶液 溶质为
溶质为 的混合液中,振荡,再滴加淀粉溶液,如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠,如果溶液无变化,则可以证明该样品盐为氯化钠。
的混合液中,振荡,再滴加淀粉溶液,如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠,如果溶液无变化,则可以证明该样品盐为氯化钠。 与亚硝酸钠发生的反应可表示为
与亚硝酸钠发生的反应可表示为 已配平
已配平 ,则
,则 是
是 _______  填化学式
填化学式 ,该反应的离子方程式为
,该反应的离子方程式为 _______ 。
(3)甲、乙两同学欲用 和
和 制取等量的
制取等量的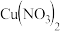 晶体,甲用稀硝酸,乙用浓硝酸。你认为用
晶体,甲用稀硝酸,乙用浓硝酸。你认为用 _______ 硝酸好 填“浓”或“稀”
填“浓”或“稀” ,理由是
,理由是 _______ 。
(1)工商管理条例明文规定:食品生产经营者不得购进、存放、使用亚硝酸盐作为食品添加剂。亚硝酸钠
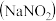 属于
属于  填“氧化物”或“盐”
填“氧化物”或“盐” ,它是一种强氧化剂,与
,它是一种强氧化剂,与 共热生成
共热生成 ,是实验室制
,是实验室制 的方法,写出
的方法,写出 与
与 共热发生反应的化学方程式
共热发生反应的化学方程式  发生反应,则反应中电子转移的数目为
发生反应,则反应中电子转移的数目为 (2)亚硝酸钠外观与食盐相似,且均有咸味。某课外探究小组欲对亚硝酸钠与氯化钠进行鉴别,其鉴别方法如下:将样品放入稀硫酸与另外一种溶液
 溶质为
溶质为 的混合液中,振荡,再滴加淀粉溶液,如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠,如果溶液无变化,则可以证明该样品盐为氯化钠。
的混合液中,振荡,再滴加淀粉溶液,如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠,如果溶液无变化,则可以证明该样品盐为氯化钠。 与亚硝酸钠发生的反应可表示为
与亚硝酸钠发生的反应可表示为 已配平
已配平 ,则
,则 是
是  填化学式
填化学式 ,该反应的离子方程式为
,该反应的离子方程式为 (3)甲、乙两同学欲用
 和
和 制取等量的
制取等量的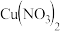 晶体,甲用稀硝酸,乙用浓硝酸。你认为用
晶体,甲用稀硝酸,乙用浓硝酸。你认为用  填“浓”或“稀”
填“浓”或“稀” ,理由是
,理由是
您最近一年使用:0次
2022-05-27更新
|
128次组卷
|
3卷引用:江西省清江中学2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
8 . 被世卫组织列为Al级新型高效安全消毒剂的二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,易溶于水,沸点为11℃,遇热不稳定易分解发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁( )]还原氯酸钠(
)]还原氯酸钠( )制取二氧化氯。某研究小组利用如图装置制备
)制取二氧化氯。某研究小组利用如图装置制备 ,向三颈烧瓶中加入
,向三颈烧瓶中加入 溶液、浓
溶液、浓 通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:

(1) 中S元素的化合价为
中S元素的化合价为_______ 价;仪器a的名称是_______ 。
(2)三颈烧瓶中发生反应的离子方程式为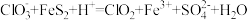 (未配平)。
(未配平)。
①该反应中被氧化的元素为_______ (填元素符号),还原产物为_______ (填化学式)。
②配平该离子方程式:_______ 。
(3)设计实验证明ClO2的氧化性比 的强:
的强:_______ 。
(4)将少量ClO2水溶液滴入盛有MnSO4溶液的试管中,振荡,有黑色沉淀生成,已知反应中氧化剂与还原剂的物质的量之比为2:5,则该反应的离子方程式为_______ 。
 )]还原氯酸钠(
)]还原氯酸钠( )制取二氧化氯。某研究小组利用如图装置制备
)制取二氧化氯。某研究小组利用如图装置制备 ,向三颈烧瓶中加入
,向三颈烧瓶中加入 溶液、浓
溶液、浓 通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
(1)
 中S元素的化合价为
中S元素的化合价为(2)三颈烧瓶中发生反应的离子方程式为
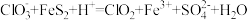 (未配平)。
(未配平)。①该反应中被氧化的元素为
②配平该离子方程式:
(3)设计实验证明ClO2的氧化性比
 的强:
的强:(4)将少量ClO2水溶液滴入盛有MnSO4溶液的试管中,振荡,有黑色沉淀生成,已知反应中氧化剂与还原剂的物质的量之比为2:5,则该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
9 . 某学习小组探究 的性质:
的性质:
(1)【观察】描述其颜色、状态:___________ 。
(2)【预测性质】从元素化合价来看, 中氧元素显
中氧元素显___________ 价,它具有的性质是___________ (填“氧化性”“还原性”或“氧化性和还原性”)。
(3)【设计实验】探究 和
和 反应情况
反应情况
取少量 粉末于试管,加入适量蒸馏水,产生气泡,用一根带火星的木条放在试管口,观察到木条复燃。振荡试管,使固体全部溶解,不再产生气泡时,将溶液分装甲、乙两支试管。向甲试管中撒少量
粉末于试管,加入适量蒸馏水,产生气泡,用一根带火星的木条放在试管口,观察到木条复燃。振荡试管,使固体全部溶解,不再产生气泡时,将溶液分装甲、乙两支试管。向甲试管中撒少量 粉末,又产生气泡;向乙试管中滴几滴酚酞溶液,溶液变红色,立即褪色。
粉末,又产生气泡;向乙试管中滴几滴酚酞溶液,溶液变红色,立即褪色。
①一般认为, 和
和 反应过程分两步:
反应过程分两步:
第一步, ;第二步,
;第二步,___________ (补充化学方程式)。
②为了进一步证明上述反应过程真实性,取少量粉末于试管,加入蒸馏水,使固体全部溶解,不再产生气泡时滴加几滴稀硫酸酸化的淀粉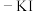 溶液,若
溶液,若___________ (填实验现象),则证明结论成立。(已知:淀粉溶液遇 变蓝色。)
变蓝色。)
(4)【归纳总结】根据 和
和 反应生成
反应生成 和
和 ,
,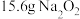 完全反应,参与反应的氧化剂质量为
完全反应,参与反应的氧化剂质量为___________ 。
(5)【问题与讨论】通过上述探究,你认为实验室保存 注意什么问题?答:
注意什么问题?答:______ 。
 的性质:
的性质:(1)【观察】描述其颜色、状态:
(2)【预测性质】从元素化合价来看,
 中氧元素显
中氧元素显(3)【设计实验】探究
 和
和 反应情况
反应情况取少量
 粉末于试管,加入适量蒸馏水,产生气泡,用一根带火星的木条放在试管口,观察到木条复燃。振荡试管,使固体全部溶解,不再产生气泡时,将溶液分装甲、乙两支试管。向甲试管中撒少量
粉末于试管,加入适量蒸馏水,产生气泡,用一根带火星的木条放在试管口,观察到木条复燃。振荡试管,使固体全部溶解,不再产生气泡时,将溶液分装甲、乙两支试管。向甲试管中撒少量 粉末,又产生气泡;向乙试管中滴几滴酚酞溶液,溶液变红色,立即褪色。
粉末,又产生气泡;向乙试管中滴几滴酚酞溶液,溶液变红色,立即褪色。①一般认为,
 和
和 反应过程分两步:
反应过程分两步:第一步,
 ;第二步,
;第二步,②为了进一步证明上述反应过程真实性,取少量粉末于试管,加入蒸馏水,使固体全部溶解,不再产生气泡时滴加几滴稀硫酸酸化的淀粉
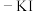 溶液,若
溶液,若 变蓝色。)
变蓝色。)(4)【归纳总结】根据
 和
和 反应生成
反应生成 和
和 ,
,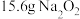 完全反应,参与反应的氧化剂质量为
完全反应,参与反应的氧化剂质量为(5)【问题与讨论】通过上述探究,你认为实验室保存
 注意什么问题?答:
注意什么问题?答:
您最近一年使用:0次
名校
10 . 草酸与高锰酸钾在酸性条件下能够发生反应: MnO +H2C2O4+H+→Mn2++CO2↑+H2O(未配平)
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)
通过下表实验探究外界因素对反应速率的影响。
(1)该反应中氧化剂和还原剂的物质的量之比为___________ 。
(2)其中T1=___________ ;V2=___________ 。
(3)若t1 <8,则由实验可得出的结论是___________ ;忽略溶液体积的变化,利用实验B中的数据计算,0~8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=___________ 。
(4)在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快。
①同学们据此提出以下假设:
假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:反应生成的K+或SO 该反应有催化作用
该反应有催化作用
丙同学认为假设3不合理,其理由是___________ 。
②丁同学用如下实验证明假设2:除了酸性高锰酸钾和草酸外,还需要选择的试剂是___________ 。(填化学式)
 +H2C2O4+H+→Mn2++CO2↑+H2O(未配平)
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)通过下表实验探究外界因素对反应速率的影响。
| 实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | |||
| A | 293 | 4 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 4 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 4 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)其中T1=
(3)若t1 <8,则由实验可得出的结论是
(4)在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快。
①同学们据此提出以下假设:
假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:反应生成的K+或SO
 该反应有催化作用
该反应有催化作用丙同学认为假设3不合理,其理由是
②丁同学用如下实验证明假设2:除了酸性高锰酸钾和草酸外,还需要选择的试剂是
您最近一年使用:0次
2021-10-23更新
|
185次组卷
|
3卷引用:江西省赣州市十六县(市)十九校2021-2022学年高一下学期期中联考化学试题



