名校
解题方法
1 . 加碘食盐中的碘以KIO3形式存在。根据反应:IO +5I-+6H+=3I2+3H2O,可用碘化钾淀粉试纸和食醋进行实验,证明食盐中存在IO
+5I-+6H+=3I2+3H2O,可用碘化钾淀粉试纸和食醋进行实验,证明食盐中存在IO 。下列说法错误的是
。下列说法错误的是
 +5I-+6H+=3I2+3H2O,可用碘化钾淀粉试纸和食醋进行实验,证明食盐中存在IO
+5I-+6H+=3I2+3H2O,可用碘化钾淀粉试纸和食醋进行实验,证明食盐中存在IO 。下列说法错误的是
。下列说法错误的是| A.实验时可观察到试纸变为蓝色 |
B.实验可证明该条件下氧化性:IO > I2 > I2 |
| C.每生成3mol I2转移电子的物质的量6mol |
D.该反应中IO 作氧化剂,发生还原反应 作氧化剂,发生还原反应 |
您最近一年使用:0次
2021-02-08更新
|
123次组卷
|
4卷引用:陕西省武功县2021-2022学年高一上学期期中考试化学试题
2 . 碘元素是人体必需的微量元素之一。某学习小组在实验室进行海带提碘的探究,实验过程如下:
Ⅰ.海带中碘元素的确定
(1)同学们称取一定量干海带,将海带先剪碎,然后用水浸泡、洗净、晾干,放入_______ (填仪器名称)中灼烧至海带完全成灰烬,然后继续进行下列流程。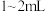 ,加入
,加入 稀硫酸、
稀硫酸、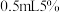 的
的 溶液,然后再加入
溶液,然后再加入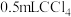 ,振荡后静置,若观察到
,振荡后静置,若观察到_______ (填实验现象),则证明海带中含有碘元素,上述过程中涉及的离子反应方程式为_______ 。
Ⅱ.海带提碘 中,可采取的操作是
中,可采取的操作是_______ 。
(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需经过蒸馏,指出图实验装置中存在的错误之处_______ 。
Ⅲ.人体碘的重要来源之一是食用加碘食盐(含 )。为测定加碘食盐中的碘含量,学习小组设计如下实验:
)。为测定加碘食盐中的碘含量,学习小组设计如下实验: 食盐样品,加适量蒸馏水使其完全溶解;
食盐样品,加适量蒸馏水使其完全溶解;
②用稀硫酸酸化所得溶液,加入足量 溶液,使
溶液,使 与
与 反应完全生成
反应完全生成 ;
;
③向②中混合液逐滴加入浓度为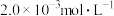 的
的 溶液,恰好反应完全时,消耗
溶液,恰好反应完全时,消耗 溶液
溶液 。(已知:
。(已知: )
)
(5)写出步骤②中发生反应的离子方程式_______ 。
(6)上述实验样品中碘元素的含量为_______ 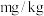 (用含w的代数式表示)。
(用含w的代数式表示)。
Ⅰ.海带中碘元素的确定
(1)同学们称取一定量干海带,将海带先剪碎,然后用水浸泡、洗净、晾干,放入

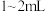 ,加入
,加入 稀硫酸、
稀硫酸、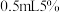 的
的 溶液,然后再加入
溶液,然后再加入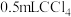 ,振荡后静置,若观察到
,振荡后静置,若观察到Ⅱ.海带提碘

 中,可采取的操作是
中,可采取的操作是(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需经过蒸馏,指出图实验装置中存在的错误之处
Ⅲ.人体碘的重要来源之一是食用加碘食盐(含
 )。为测定加碘食盐中的碘含量,学习小组设计如下实验:
)。为测定加碘食盐中的碘含量,学习小组设计如下实验: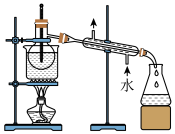
 食盐样品,加适量蒸馏水使其完全溶解;
食盐样品,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量
 溶液,使
溶液,使 与
与 反应完全生成
反应完全生成 ;
;③向②中混合液逐滴加入浓度为
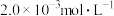 的
的 溶液,恰好反应完全时,消耗
溶液,恰好反应完全时,消耗 溶液
溶液 。(已知:
。(已知: )
)(5)写出步骤②中发生反应的离子方程式
(6)上述实验样品中碘元素的含量为
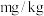 (用含w的代数式表示)。
(用含w的代数式表示)。
您最近一年使用:0次
2024-02-20更新
|
197次组卷
|
2卷引用:陕西省咸阳市实验中学2021-2022学年高一下学期阶段性检测(一)化学试题
3 . 如图是有关钠与水反应及产物检验的实验装置。实验开始时先向管内加入滴有酚酞试液的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中。

回答下列问题:
(1)能证明钠的密度比水小的现象是___________ 。
(2)能证明钠的熔点低的现象是___________ 。
(3)能证明有氢氧化钠生成的现象是___________ 。
(4)能证明有气体产生的现象是A端液面___________ (填“上升”“下降”或“不变”)。
(5)写出U型管中发生反应的离子方程式:___________ ,若反应生成氢气的体积为11.2L(标准状况下),则反应过程中转移电子数为___________ 。
(6)若将上述装置中液体替换为 溶液,除上述现象外,还会产生的现象是
溶液,除上述现象外,还会产生的现象是_________ 。

回答下列问题:
(1)能证明钠的密度比水小的现象是
(2)能证明钠的熔点低的现象是
(3)能证明有氢氧化钠生成的现象是
(4)能证明有气体产生的现象是A端液面
(5)写出U型管中发生反应的离子方程式:
(6)若将上述装置中液体替换为
 溶液,除上述现象外,还会产生的现象是
溶液,除上述现象外,还会产生的现象是
您最近一年使用:0次
4 . 已知反应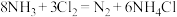 ,下列说法正确的是
,下列说法正确的是
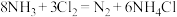 ,下列说法正确的是
,下列说法正确的是A. 被氧化 被氧化 |
B.上述反应证明还原性: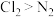 |
| C.氧化产物和还原产物的物质的量之比为6∶1 |
| D.氧化剂和还原剂的物质的量之比为3∶2 |
您最近一年使用:0次
名校
解题方法
5 . 请回答下列问题:
(1)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气),若反应中消耗Cl2 1.5mol则被氧化的NH3在标准状况下的体积为___________ L。
(2)8.4g氮气和9.6g某单质Rx所含原子个数相同,且分子个数之比为3:2,则x的值是___________ ,R的摩尔质量是___________ 。
(3)在发生离子反应的反应物或生成物中,一定存在的是___________(填字母)。
(4)有一瓶澄清的溶液其中可能含有H+、Mg2+、Ba2+、 、
、 、
、 ,取该溶液进行以下实验:
,取该溶液进行以下实验:
①用pH试纸检验,表明溶液呈强酸性,可以排除___________ 的存在。
②取出部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,继续滴加NaOH溶液,有白色沉淀产生,则可证明___________ 的存在。
③取部分上述碱性溶液加Na2CO3溶液,有白色沉淀生成,证明___________ 的存在,又可以排除___________ 的存在。
④根据上述实验事实还能确定溶液中肯定存在的离子是___________ 。
(1)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气),若反应中消耗Cl2 1.5mol则被氧化的NH3在标准状况下的体积为
(2)8.4g氮气和9.6g某单质Rx所含原子个数相同,且分子个数之比为3:2,则x的值是
(3)在发生离子反应的反应物或生成物中,一定存在的是___________(填字母)。
| A.单质 | B.氧化物 | C.盐 | D.化合物 |
 、
、 、
、 ,取该溶液进行以下实验:
,取该溶液进行以下实验:①用pH试纸检验,表明溶液呈强酸性,可以排除
②取出部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,继续滴加NaOH溶液,有白色沉淀产生,则可证明
③取部分上述碱性溶液加Na2CO3溶液,有白色沉淀生成,证明
④根据上述实验事实还能确定溶液中肯定存在的离子是
您最近一年使用:0次
名校
6 . 金属钛在医疗领域的使用非常广泛,可以应用在人体骨骼、组织移植和再造,如制人造髋关节、膝关节、头盖骨。主动心瓣等。TiCl4是制备金属钛的重要中间体,某小组同学利用如下装置在实验室制备TiCl4(夹持装置略去)。

相关信息如下表所示:
请回答下列问题:
(1)仪器b的名称为_______ ,装置A中导管a的作用为_______ 。装置B中所装试剂为_______ ,装置A中发生反应的离子方程式为_______ 。
(2)装置C中除生成TiCl4外,同时还生成一种气态不成盐氧化物,该反应的化学方程式为_______ 。制得的TiCl4中常含有少量CCl4,从混合液体中分离出TiCl4的操作名称为_______ 。
(3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;_______ (按正确的顺序填入下列操作的序号)。
①打开分液漏斗活塞
②关闭分液漏斗活塞
③停止加热,充分冷却
④加热装置C中陶瓷管
(4)设计实验证明装置D中收集到的液体中含有TiCl4:_______ 。
(5)TiCl4可制备纳米TiO2:以N2为载体,用TiCl4和水蒸气反应生成Ti(OH)4。再控制温度生成纳米xTiO2∙yH2O。测定产物xTiO2∙yH2O组成的方法如下:
步骤一:取样品2.100g,在酸性条件下充分溶解,并用适量铝将TiO2+还原为Ti3+,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,并用稀硫酸定容,得待测液。
步骤二:取待测液25.00mL于锥形瓶中,加几淌KSCN溶液作指示剂,用0.1000mol·L-1的NH4Fe(SO4)2标准溶液滴定,将Ti3+氧化为TiO2+。重复滴定2次。滴定所得的相关数据如下表:
①步骤一中用稀硫酸而不用水定容的原因是_______ 。
②通过计算确定该样品的组成为_______ 。

相关信息如下表所示:
| 熔点/℃ | 沸点/℃ | 密度/(g∙cm-3) | 水溶性 | |
| TiCl4 | -24 | 136.4 | 1.7 | 易水解生成白色沉淀,能溶于有机溶剂 |
| CCl4 | -23 | 76.8 | 1.6 | 难溶于水 |
(1)仪器b的名称为
(2)装置C中除生成TiCl4外,同时还生成一种气态不成盐氧化物,该反应的化学方程式为
(3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;
①打开分液漏斗活塞
②关闭分液漏斗活塞
③停止加热,充分冷却
④加热装置C中陶瓷管
(4)设计实验证明装置D中收集到的液体中含有TiCl4:
(5)TiCl4可制备纳米TiO2:以N2为载体,用TiCl4和水蒸气反应生成Ti(OH)4。再控制温度生成纳米xTiO2∙yH2O。测定产物xTiO2∙yH2O组成的方法如下:
步骤一:取样品2.100g,在酸性条件下充分溶解,并用适量铝将TiO2+还原为Ti3+,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,并用稀硫酸定容,得待测液。
步骤二:取待测液25.00mL于锥形瓶中,加几淌KSCN溶液作指示剂,用0.1000mol·L-1的NH4Fe(SO4)2标准溶液滴定,将Ti3+氧化为TiO2+。重复滴定2次。滴定所得的相关数据如下表:
| 滴定序号 | 待测液体积/mL | NH4Fe(SO4)2标准溶液滴定管起点读数/mL | NH4Fe(SO4)2标准溶液滴定管终点读数/mL |
| 1 | 25.00 | 0.02 | 24.02 |
| 2 | 25.00 | 0.08 | 24.06 |
| 3 | 25.00 | 0.12 | 24.14 |
②通过计算确定该样品的组成为
您最近一年使用:0次
2021-04-04更新
|
605次组卷
|
4卷引用:陕西省榆林市2021届高考模拟第三次测试(三模)理综化学试题
陕西省榆林市2021届高考模拟第三次测试(三模)理综化学试题河南省新乡市2021届高三第二次模拟理综化学试题(已下线)押山东卷第20题 化学实验综合题-备战2021年高考化学临考题号押题(山东卷)河北省石家庄市第二中学2021-2022学年高三上学期11月第一次考试化学试题
名校
解题方法
7 . (Ⅰ)某校课外活动小组同学设计实验,探究木炭与浓硫酸在加热条件下反应生成气体的成分。

(1)木炭与浓硫酸反应的化学方程式:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O,其中浓H2SO4所起的作用是
CO2↑+2SO2↑+2H2O,其中浓H2SO4所起的作用是_______ (填“氧化剂”或“还原剂”)。若有0.2mol碳的完全反应,则消耗H2SO4的质量是_______ g,标况下产生SO2的体积为_______ L。
(2)A装置中品红溶液颜色褪色,证明含有_______ 气体。
(3)实验过程中,装置C将观察到的现象是_______ ,证明含有_______ 气体。若该结论正确,则B中的现象应为_______
(4)煤和石油的燃烧过程中都有二氧化硫和二氧化碳排放,其中二氧化硫造成的环境影响主要是_______ ,二氧化碳造成的环境影响主要是_______ 。(每空格只填一个选项)
A.酸雨 B.破坏臭氧层 C.温室效应
(Ⅱ)在实验室欲制取适量的NO气体。
①反应的化学方程式为:_______
②下图中最适宜完成该实验的简易装置是_______ (填序号);


(1)木炭与浓硫酸反应的化学方程式:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O,其中浓H2SO4所起的作用是
CO2↑+2SO2↑+2H2O,其中浓H2SO4所起的作用是(2)A装置中品红溶液颜色褪色,证明含有
(3)实验过程中,装置C将观察到的现象是
(4)煤和石油的燃烧过程中都有二氧化硫和二氧化碳排放,其中二氧化硫造成的环境影响主要是
A.酸雨 B.破坏臭氧层 C.温室效应
(Ⅱ)在实验室欲制取适量的NO气体。
①反应的化学方程式为:
②下图中最适宜完成该实验的简易装置是

您最近一年使用:0次
8 . 过氧化钠和氢化钠(NaH),广泛应用于工业生产.
(1)氢化钠(NaH)中氢元素的化合价为_____________ .
(2)NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,该反应中的氧化剂是_________ ,氧化剂与还原剂的物质的量之比是_____________ .
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为_____________________ .
(4)过氧化钠是呼吸面和防毒面具中氧气的来源,写出过氧化钠与二氧化碳反应的化学方程式______________ ,证明有氧气产生的方法是______________ .
(1)氢化钠(NaH)中氢元素的化合价为
(2)NaH能与水剧烈反应:NaH+H2O═NaOH+H2↑,该反应中的氧化剂是
(3)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,该反应的化学方程式为
(4)过氧化钠是呼吸面和防毒面具中氧气的来源,写出过氧化钠与二氧化碳反应的化学方程式
您最近一年使用:0次
解题方法
9 . 在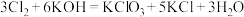 的反应中,下列说法不正确的是
的反应中,下列说法不正确的是
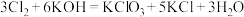 的反应中,下列说法不正确的是
的反应中,下列说法不正确的是A. 既是氧化剂,又是还原剂 既是氧化剂,又是还原剂 |
B. 是还原产物, 是还原产物, 是氧化产物 是氧化产物 |
| C.若有3个氯分子充分反应,转移电子为6个 |
| D.被还原的氯气的质量是被氧化的氯气的质量的5倍 |
您最近一年使用:0次
名校
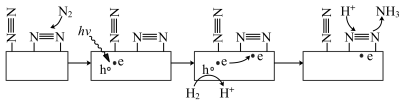
10 . 合成氨技术对全球农业、工业和医药等领域都产生了重大影响。一种以 和
和 为原料光催化合成氨气的原理如图,其中hv表示失去电子后带正电的空穴,·
为原料光催化合成氨气的原理如图,其中hv表示失去电子后带正电的空穴,· 表示电子,设
表示电子,设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 和
和 为原料光催化合成氨气的原理如图,其中hv表示失去电子后带正电的空穴,·
为原料光催化合成氨气的原理如图,其中hv表示失去电子后带正电的空穴,· 表示电子,设
表示电子,设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
A.总反应为 |
| B.反应过程中有极性键和非极性键的断裂与形成 |
C.每生成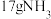 ,转移的电子数为 ,转移的电子数为 |
D.标准状况下,相同体积的 和 和 的物质的量相同 的物质的量相同 |
您最近一年使用:0次



