解题方法
1 . 利用电解产生的 与
与 发生反应生成高活性的羟基自由基(
发生反应生成高活性的羟基自由基( ,有很强氧化性),能有效降解水体中的有机污染物,原理如图所示。下列说法正确的是
,有很强氧化性),能有效降解水体中的有机污染物,原理如图所示。下列说法正确的是
 与
与 发生反应生成高活性的羟基自由基(
发生反应生成高活性的羟基自由基( ,有很强氧化性),能有效降解水体中的有机污染物,原理如图所示。下列说法正确的是
,有很强氧化性),能有效降解水体中的有机污染物,原理如图所示。下列说法正确的是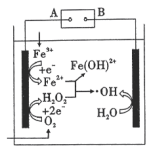
| A.电源的B极为负极 |
| B.生成羟基自由基的反应仅有一个 |
| C.利用羟基自由基来处理有机物,效率高、无污染 |
D.电解池外电路转移 电子,理论上可产生的 电子,理论上可产生的 为 为 |
您最近一年使用:0次
名校
解题方法
2 . 工业利用钛铁矿(主要成分是钛酸亚铁)冶炼钛的主反应: ,设
,设 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
 ,设
,设 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是A. 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 |
B.1L0.1mol/L 溶液中,阳离子数目大于 溶液中,阳离子数目大于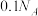 |
C.每生成1mol ,转移电子数为 ,转移电子数为 |
D. 易水解,水解产物为 易水解,水解产物为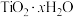 |
您最近一年使用:0次
解题方法
3 . 芬顿试剂是以 和
和 组成的水溶液体系,具有极强的氧化能力,可用于氧化降解水体中的有机污染物。活性中间体
组成的水溶液体系,具有极强的氧化能力,可用于氧化降解水体中的有机污染物。活性中间体 产生机理如图所示。下列说法正确的是
产生机理如图所示。下列说法正确的是
 和
和 组成的水溶液体系,具有极强的氧化能力,可用于氧化降解水体中的有机污染物。活性中间体
组成的水溶液体系,具有极强的氧化能力,可用于氧化降解水体中的有机污染物。活性中间体 产生机理如图所示。下列说法正确的是
产生机理如图所示。下列说法正确的是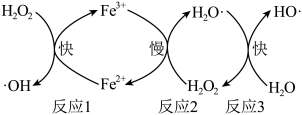
A. 在 在 产生的过程中作催化剂 产生的过程中作催化剂 |
| B.芬顿试剂去除有机污染物时使用温度不宜过高 |
C.“反应1”为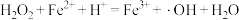 |
D.芬顿试剂降解 苯酚为 苯酚为 和 和 ,理论上消耗 ,理论上消耗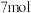 的 的 |
您最近一年使用:0次
4 . 稀有气体氙的氟化物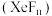 与
与 溶液反应剧烈,与水反应则较为温和,反应式如下:
溶液反应剧烈,与水反应则较为温和,反应式如下:
下列说法正确的是
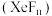 与
与 溶液反应剧烈,与水反应则较为温和,反应式如下:
溶液反应剧烈,与水反应则较为温和,反应式如下:| 与水反应 | 与 溶液反应 溶液反应 |
i.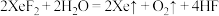 | ii.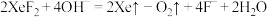 |
iii. | Ⅳ.  |
A. 具有平面三角形结构 具有平面三角形结构 | B. 的还原性比 的还原性比 强 强 |
C.反应 均为氧化还原反应 均为氧化还原反应 | D.反应iv每生成 ,转移 ,转移 电子 电子 |
您最近一年使用:0次
5 . 我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑,下列说法不正确 的是(NA为阿伏加德罗常数的值)
| A.该反应在任何温度下都可以自发进行 | B.生成28 g N2转移电子的数目为10NA |
| C.KNO3是氧化剂 | D.K2S和N2都是还原产物 |
您最近一年使用:0次
6 . 中国古代四大发明之一的黑火药,其爆炸过程中发生反应的化学方程式为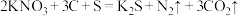 。下列说法正确的是
。下列说法正确的是
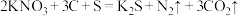 。下列说法正确的是
。下列说法正确的是| A.消耗1 mol KNO3转移电子数为6.02×1023 |
| B.S和KNO3均为还原剂 |
| C.反应过程中氮元素被还原 |
| D.CO2为还原产物 |
您最近一年使用:0次
解题方法
7 . 工业上以钛铁矿( ,其中Ti为+4价)为主要原料制备金属钛的工艺流程如图所示。下列说法错误的是
,其中Ti为+4价)为主要原料制备金属钛的工艺流程如图所示。下列说法错误的是
 ,其中Ti为+4价)为主要原料制备金属钛的工艺流程如图所示。下列说法错误的是
,其中Ti为+4价)为主要原料制备金属钛的工艺流程如图所示。下列说法错误的是
| A.Ti位于元素周期表中第4周期ⅣB族 |
| B.氯化时,被氧化的元素有碳和铁 |
| C.制备Ti时,Ar气做保护气,可用氮气代替 |
D.氯化时,每生成0.1 mol  ,转移电子0.7 mol ,转移电子0.7 mol |
您最近一年使用:0次
名校
8 . PtNiFe—LDHGO催化甲醛氧化的反应机理如图:
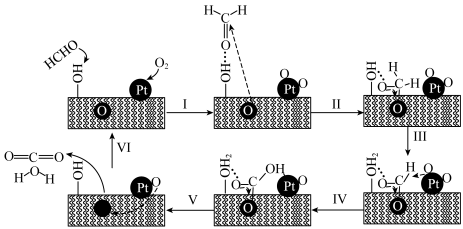
A.步骤Ⅰ中甲醛通过氢键吸附在催化剂表面的 上 上 |
| B.上述反应机理涉及极性键和非极性键的形成 |
C.该反应每生成1 mol ,转移电子的数目约为 ,转移电子的数目约为 |
| D.PtNiFe—LDHGO降低了该反应的活化能 |
您最近一年使用:0次
名校
解题方法
9 . 某课题组利用工业废气中的NO制备NH4NO3的工艺流程如图所示,若装置Ⅰ和装置Ⅱ中反应后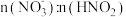 都为
都为 (不考虑HNO2电离),下列说法错误的是
(不考虑HNO2电离),下列说法错误的是
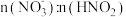 都为
都为 (不考虑HNO2电离),下列说法错误的是
(不考虑HNO2电离),下列说法错误的是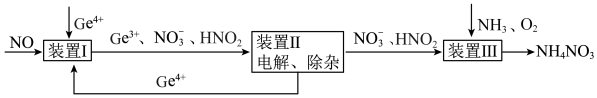
A.装置Ⅰ中反应的离子方程式为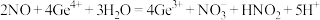 |
| B.装置Ⅰ中若有5.6L(标准状况下)NO参与反应,则转移0.5mol电子 |
C.装置Ⅲ中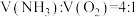 ,可实现原子利用率最大化 ,可实现原子利用率最大化 |
D.装置Ⅲ发生的氧化还原反应中氧化剂和还原剂物质的量之比为 |
您最近一年使用:0次
名校
10 .  是制备金属钛的重要中间体,工业制备原理为
是制备金属钛的重要中间体,工业制备原理为 。设
。设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 是制备金属钛的重要中间体,工业制备原理为
是制备金属钛的重要中间体,工业制备原理为 。设
。设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.12gC中共价键数目最多为 |
B. 的中子数目为 的中子数目为 |
C.若生成的CO体积为26.88L(已换算成标准状况)时,转移电子数目为 |
D. 溶液中含 溶液中含 数目为 数目为 |
您最近一年使用:0次



