10-11高三上·浙江金华·阶段练习
名校
解题方法
1 .
(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。_______
_______+_______→_______+_______+_______+H2O
(2)反应物中发生氧化反应的物质_______ ,被还原的元素是_______ 。
(3)反应中1 mol氧化剂_______ (填“得到”或“失去”)_______ mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:_______

(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
_______+_______→_______+_______+_______+H2O
(2)反应物中发生氧化反应的物质
(3)反应中1 mol氧化剂
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:

您最近一年使用:0次
11-12高三上·北京朝阳·期末
2 . A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。
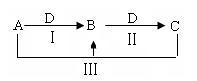
(1)若A为氯碱工业的产品,C为厨房中的用品。
① D的电子式是______ 。
② 反应Ⅲ的离子方程式是______ 。
③ 氯碱工业制备A的化学方程式是______ ,其中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1 mol KI转移电子0.6 mol,则三种物质间反应的离子方程式是______ 。
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
① 反应Ⅲ的离子方程式是______ 。
② B可作净水剂,其原理是______ (用离子方程式表示)。在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是______ 。

(1)若A为氯碱工业的产品,C为厨房中的用品。
① D的电子式是
② 反应Ⅲ的离子方程式是
③ 氯碱工业制备A的化学方程式是
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
① 反应Ⅲ的离子方程式是
② B可作净水剂,其原理是
您最近一年使用:0次
2010·北京东城·一模
3 . 用如下装置可以完成一系列实验(图中夹持装置已略去)。

请回答下列问题:
Ⅰ.若用装置A选用浓硫酸和亚硫酸钠固体制取SO2气体(根据需要可以加热),并通过装置B完成表中设计实验,请填写表中空白:
II.若用装置A选用浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做了如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液。回答下列问题:
(1)p中盛装试剂为__________________ 。
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式_______ 。①处包有的某固体物质可能是______________ 。
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在整个实验过程中,在③处能观察到_________________________ 。
(4)反应较长时间后,②处有棕黄色褪去,生成无色的IO3-,写出该反应的离子方程式:__________________________________________ 。

请回答下列问题:
Ⅰ.若用装置A选用浓硫酸和亚硫酸钠固体制取SO2气体(根据需要可以加热),并通过装置B完成表中设计实验,请填写表中空白:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | 褪色ZXXK] | 浅黄色 | ||
| 体现SO2的性质 |
(1)p中盛装试剂为
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在整个实验过程中,在③处能观察到
(4)反应较长时间后,②处有棕黄色褪去,生成无色的IO3-,写出该反应的离子方程式:
您最近一年使用:0次
2014·江苏徐州·一模
4 . 硫酸铜在生产、生活中应用广泛。某化工厂用含少量铁的废铜渣为原料生产胆矾的流程如下:

(1)写出浸出时铜与稀硫酸、稀硝酸反应生成硫酸铜的化学方程式:
(2)取样检验是为了确认Fe3+是否除净,你的检验方法是_______________________
(3)滤渣c是__________ 。
(4)气体a可以被循环利用,用化学方程式表示气体a被循环利用的原理为2NO+O2=2NO2、____________ 。
(5)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和O2气体,且n(SO3)∶n(SO2)=1∶2,写出硫酸铜受热分解的化学方程式:__________________________ 。
某同学设计了如下图所示的实验装置分别测定生成的SO2、SO3气体的质量和O2气体的体积。此设计有不合理之处,请指出:_______________________________________ 。


(1)写出浸出时铜与稀硫酸、稀硝酸反应生成硫酸铜的化学方程式:
(2)取样检验是为了确认Fe3+是否除净,你的检验方法是
(3)滤渣c是
(4)气体a可以被循环利用,用化学方程式表示气体a被循环利用的原理为2NO+O2=2NO2、
(5)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和O2气体,且n(SO3)∶n(SO2)=1∶2,写出硫酸铜受热分解的化学方程式:
某同学设计了如下图所示的实验装置分别测定生成的SO2、SO3气体的质量和O2气体的体积。此设计有不合理之处,请指出:

您最近一年使用:0次
2016-12-09更新
|
565次组卷
|
6卷引用:2015-2016学年北京大学附属中学河南分校高一上联考化学试卷
10-11高三上·北京朝阳·期末
名校
5 . 水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2O32-+O2+aOH-=Y+S4O62-+2H2O,下列说法中,不正确的是
| A.a = 4 | B.Y的化学式为Fe2O3 |
| C.S2O32-是还原剂 | D.每有1molO2参加反应,转移的电子总数为4mol |
您最近一年使用:0次
6 . 高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
(1)Na2FeO4中铁元素的化合价是_____ 价,Na2FeO4具有较强的______ (填“氧化性”或“还原性”)。
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是_____ (用离子方程式表示)。
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:2FeCl3 + 10NaOH + 3NaClO = 2_______ + 5_______ + 9_________ 。
(4)工业上还可用电解浓NaOH溶液的方法制Na2FeO4 。
① 若电解所需的浓NaOH溶液为16 mol/L,则在实验室配制500 mL该浓度的溶液需NaOH_______ g,配制过程所需玻璃仪器是___________ 。
② 电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:
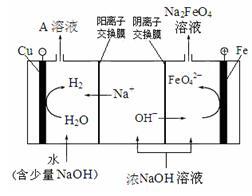
阳极的电极反应式是__________________ ;可循环使用的物质是_______________ ,理由是____________ 。
(1)Na2FeO4中铁元素的化合价是
(2)用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是
(3)工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:2FeCl3 + 10NaOH + 3NaClO = 2
(4)工业上还可用电解浓NaOH溶液的方法制Na2FeO4 。
① 若电解所需的浓NaOH溶液为16 mol/L,则在实验室配制500 mL该浓度的溶液需NaOH
② 电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:

阳极的电极反应式是
您最近一年使用:0次
2014·宁夏银川·二模
7 . 第五主族的磷单质及其化合物在工业上有广泛应用.
(1)同磷灰石在高温下制备黄磷的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)═3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H
已知相同条件下:
4Ca3(PO4)2F(s)+3SiO2(s)═6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H1
2Ca3(PO4)2(s)+10C(s)═P4(g)+6CaO(s)+10CO(g)△H2
SiO2(s)+CaO(s)═CaSiO3(s)△H3
用△H1、△H2和△H3表示△H,则△H=______ ;
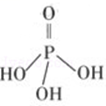
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式如图)之间脱去两个水分子产物,其结构式为______ ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为______ ;
(3)次磷酸钠(NaH2PO2)可用于工业上的化学镀镍.
①化学镀镍的溶液中含有Ni2+和H2PO2﹣,在酸性等条件下发生下述反应:
(a) Ni2++ H2PO2﹣+ → Ni++ H2PO3﹣+
(b)6H2PO﹣2+2H+═2P+4H2PO3+3H2↑
请在答题卡上写出并配平反应式(a)___________________________ ;
②利用①中反应可在塑料镀件表面沉积镍﹣磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀.请从以下方面比较化学镀与电镀.
方法上的不同点:______ ;
原理上的不同点:______ ;
化学镀的优点:______ .
(1)同磷灰石在高温下制备黄磷的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)═3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H
已知相同条件下:
4Ca3(PO4)2F(s)+3SiO2(s)═6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H1
2Ca3(PO4)2(s)+10C(s)═P4(g)+6CaO(s)+10CO(g)△H2
SiO2(s)+CaO(s)═CaSiO3(s)△H3
用△H1、△H2和△H3表示△H,则△H=
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式如图)之间脱去两个水分子产物,其结构式为

(3)次磷酸钠(NaH2PO2)可用于工业上的化学镀镍.
①化学镀镍的溶液中含有Ni2+和H2PO2﹣,在酸性等条件下发生下述反应:
(a) Ni2++ H2PO2﹣+ → Ni++ H2PO3﹣+
(b)6H2PO﹣2+2H+═2P+4H2PO3+3H2↑
请在答题卡上写出并配平反应式(a)
②利用①中反应可在塑料镀件表面沉积镍﹣磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀.请从以下方面比较化学镀与电镀.
方法上的不同点:
原理上的不同点:
化学镀的优点:
您最近一年使用:0次
2014-06-17更新
|
1050次组卷
|
4卷引用:2015届北京市怀柔区高三4月模拟练习化学试卷
2015届北京市怀柔区高三4月模拟练习化学试卷(已下线)2013-2014宁夏银川市第一中学高三第二次模拟考试理综化学试卷贵州省织金县一中2019届高三上学期12月份考试化学试题山东省泰安市2020届高三化学一轮复习《化学与技术》专题测试
12-13高一上·北京·期中
名校
8 . (1)K2Cr2O7+ 14HCl=2KCl + 2CrCl3 + 3Cl2↑+ 7H2O (用“单线桥”表示电子转移的方向和数目________ )氧化剂是_____________ ,氧化产物与还原产物的物质的量之比为_____________ 。
(2)______ mol H2O中共含有9.03×1022个原子,其质量为_______ 。
(3)配平下列氧化还原反应方程式:
___ KMnO4+___ H2S+__ H2SO4(稀) —__ MnSO4+__ S↓+__ K2SO4+__ H2O
(4)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:
3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气)
若反应中消耗Cl21.5 mol则被氧化的NH3在标准状况下的体积为______ L。
(2)
(3)配平下列氧化还原反应方程式:
(4)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:
3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气)
若反应中消耗Cl21.5 mol则被氧化的NH3在标准状况下的体积为
您最近一年使用:0次
11-12高三上·北京朝阳·期中
9 . 2011年9月29日成功发射天宫一号的长征二号F型火箭巨大的推力来源于一个氧化还原反应,反应时偏二甲肼(C2H8N2)做燃料,N2O4做氧化剂,生成三种气体物质,完成并配平该燃烧反应的化学方程式:
_____ C2H8N2+_____ N2O4=____ N2↑+___ CO2↑ +______ __________
(1)火箭发射前低温加注的液态氧化剂N2O4是一种强酸性剧毒物质,常温下,纯净的N2O4是无色气体,可溶于水,且与水反应生成两种含氧酸,该反应的化学方程式为_______________ ,对上述反应中的各种物质,下列说法正确的是_____________ 。
(2)通过仪器分析燃烧剂偏二甲肼分子,得知其分子结构情况如下表:

符合上表结构及数据要求的同分异构体共有________ 种,已知偏二甲肼的结构中有一个氮原子上没有连接氢原子,则偏二甲肼的结构简式是__________________ 。
(1)火箭发射前低温加注的液态氧化剂N2O4是一种强酸性剧毒物质,常温下,纯净的N2O4是无色气体,可溶于水,且与水反应生成两种含氧酸,该反应的化学方程式为
| A.N2O4只做氧化剂 | B.产物中两种酸都是强酸 |
| C.反应中水只做溶剂 | D.N2O4泄漏后可产生红棕色气体 |
(2)通过仪器分析燃烧剂偏二甲肼分子,得知其分子结构情况如下表:

符合上表结构及数据要求的同分异构体共有
您最近一年使用:0次
真题
名校
10 . 氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e→NO+2H2O ;KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:_______________________________
(2)反应中硝酸体现了_________ 、_________ 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是________ mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:___________________________________ 。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了
(3)反应中若产生0.2mol气体,则转移电子的物质的量是
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:
您最近一年使用:0次
2009-11-16更新
|
1908次组卷
|
10卷引用:2012届北京四中高三上学期期中测试化学试卷
(已下线)2012届北京四中高三上学期期中测试化学试卷2007年普通高等学校招生全国统一考试(上海卷)化学试题(已下线)2012-2013学年辽宁省丹东市宽甸二中高二4月月考(一)化学试卷(已下线)2014高考化学二轮专题突破 专题四氧化还原反应练习卷(已下线)2014届高考化学三轮复习排查 专题3离子反应 氧化还原反应练习卷(已下线)2015届四川省成都市高新区高三9月月考化学试卷(已下线)2015届浙江省江山实验中学高三9月月考化学试卷2015届福建省武平县第一中学高三上学期12月月考化学试卷四川省南充高级中学2017-2018学年高一12月月考化学试题沪科版化学拓展性课程4《离子互换反应和氧化还原反应》测试题



