1 . 从酸性含铬废水(主要阴离子为 )中回收铬元素(
)中回收铬元素( )的部分工艺流程如图所示。
)的部分工艺流程如图所示。
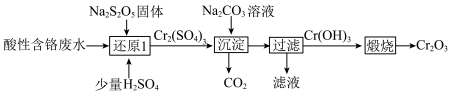
下列有关说法正确的是
 )中回收铬元素(
)中回收铬元素( )的部分工艺流程如图所示。
)的部分工艺流程如图所示。
下列有关说法正确的是
| A.“过滤”时需用玻璃棒搅拌 |
| B.“煅烧”过程中发生了氧化还原反应 |
C.若分别用 、 、 还原等量的 还原等量的 ,消耗 ,消耗 与 与 的物质的量之比为1∶3 的物质的量之比为1∶3 |
D.“还原1”时反应的离子方程式为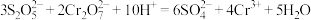 |
您最近一年使用:0次
2024-01-08更新
|
261次组卷
|
6卷引用:青海省西宁市大通县2023-2024学年高一上学期期末考试化学试题
2 . 少量 与
与 溶液能发生如下反应:
溶液能发生如下反应: (方程式未配平),设
(方程式未配平),设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
A.1L 1  溶液含 溶液含 的数目为2 的数目为2 | B.1mol  可制得 可制得 的胶粒数为 的胶粒数为 |
C.78g  含有共价键的数目为 含有共价键的数目为 | D.每生成1mol X,转移的电子数为 |
您最近一年使用:0次
2023-12-01更新
|
156次组卷
|
6卷引用:青海省海南州贵德高级中学2023-2024学年高三上学期10月月考化学试卷
解题方法
3 . 在室温下,Ti不与O2、H2O、强碱、强酸反应,在高温下可与O2反应。Hunter法是最早研究用来制取金属钛的方法,其流程如下图所示。回答下列问题:
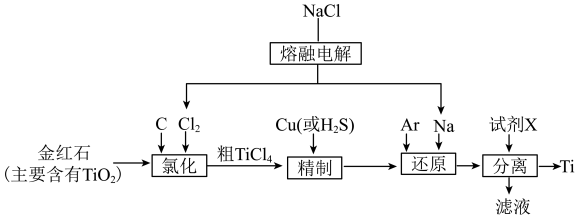
(1)“氯化”是在1000~1050℃下进行,碳被氧化为CO,该反应的化学方程式为___________ 。
(2)“精制”时,粗 中含有大量杂质,可用精馏的方法提纯,对于沸点相近的
中含有大量杂质,可用精馏的方法提纯,对于沸点相近的 杂质可用铜(或
杂质可用铜(或 )将其转化为
)将其转化为 沉淀,反应机理为
沉淀,反应机理为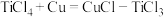 ,
,
 。从总反应看,
。从总反应看, 是该反应的
是该反应的___________ ; 可与
可与 直接反应生成
直接反应生成 ,写出
,写出 与
与 发生反应的化学方程式:
发生反应的化学方程式:___________ 。
(3)“钠还原”是用液态钠还原气态 得到Ti,Ar的作用是
得到Ti,Ar的作用是___________ ;若发生 、
、 等副反应,其原因可能是
等副反应,其原因可能是___________ 。
(4)“分离”时,固体混合物需经取出、破碎、酸浸、过滤、洗涤及干燥等步骤,试剂X为___________ (填名称),滤液循环使用的方法是___________ 。

(1)“氯化”是在1000~1050℃下进行,碳被氧化为CO,该反应的化学方程式为
(2)“精制”时,粗
 中含有大量杂质,可用精馏的方法提纯,对于沸点相近的
中含有大量杂质,可用精馏的方法提纯,对于沸点相近的 杂质可用铜(或
杂质可用铜(或 )将其转化为
)将其转化为 沉淀,反应机理为
沉淀,反应机理为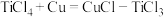 ,
,
 。从总反应看,
。从总反应看, 是该反应的
是该反应的 可与
可与 直接反应生成
直接反应生成 ,写出
,写出 与
与 发生反应的化学方程式:
发生反应的化学方程式:(3)“钠还原”是用液态钠还原气态
 得到Ti,Ar的作用是
得到Ti,Ar的作用是 、
、 等副反应,其原因可能是
等副反应,其原因可能是(4)“分离”时,固体混合物需经取出、破碎、酸浸、过滤、洗涤及干燥等步骤,试剂X为
您最近一年使用:0次
名校
4 . 高铁酸钾( ,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:
实验(一)制备
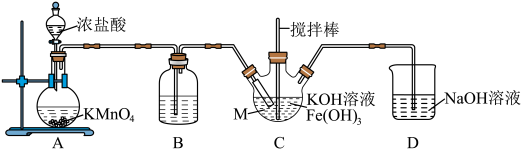
(1)仪器M的名称是_______ ,装置B的作用是_______ 。
(2)装置C中生成 的化学方程式为
的化学方程式为______ 。
(3)实验得知装置C中吸收 的量为装置A中生成
的量为装置A中生成 总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成
总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成 的质量为
的质量为_______ g。
实验(二)探究 的性质。
的性质。
Ⅰ.探究 在酸性条件下的稳定性。
在酸性条件下的稳定性。
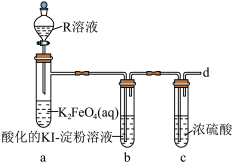
已知:实验中观察到试管b中溶液变为蓝色,试管a中溶液由紫红色变黄色并产生气泡。
(4)R溶液为_______ (填“稀硫酸”或“盐酸”),写出装置a中的离子方程式:______ ,不选择另一种酸的主要原因是_______ 。
(5)设计一种方案检验从d中逸出的气体:_______
Ⅱ.探究在酸性条件下的氧化性。
(6)向 溶液中滴加少量用稀硫酸酸化后的
溶液中滴加少量用稀硫酸酸化后的 溶液,溶液呈紫红色。
溶液,溶液呈紫红色。_______ (填“能”或“不能”)证明氧化性: ,原因是
,原因是_______ (用文字说明)。
 ,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:实验(一)制备


(1)仪器M的名称是
(2)装置C中生成
 的化学方程式为
的化学方程式为(3)实验得知装置C中吸收
 的量为装置A中生成
的量为装置A中生成 总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成
总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成 的质量为
的质量为实验(二)探究
 的性质。
的性质。Ⅰ.探究
 在酸性条件下的稳定性。
在酸性条件下的稳定性。
已知:实验中观察到试管b中溶液变为蓝色,试管a中溶液由紫红色变黄色并产生气泡。
(4)R溶液为
(5)设计一种方案检验从d中逸出的气体:
Ⅱ.探究在酸性条件下的氧化性。
(6)向
 溶液中滴加少量用稀硫酸酸化后的
溶液中滴加少量用稀硫酸酸化后的 溶液,溶液呈紫红色。
溶液,溶液呈紫红色。 ,原因是
,原因是
您最近一年使用:0次
2023-09-27更新
|
352次组卷
|
11卷引用:青海省海南州贵德高级中学2023-2024学年高三上学期10月月考化学试卷
青海省海南州贵德高级中学2023-2024学年高三上学期10月月考化学试卷河北省邢台市五岳联盟2023-2024学年高三上学期9月月考化学试题河北省部分学校2023-2024学年高三上学期9月月考化学试题河南省2023-2024学年高三上学期一轮复习阶段性检测(三)化学试题河南省驻马店市第一次联考2023-2024学年高三上学期9月月考化学试题江西省部分高中学校2024届高三上学期9月大联考化学试题福建省2023-2024学年高三上学期10月百万大联考化学试题 河南省洛阳市洛宁县第一高级中学2023-2024学年高三上学期阶段性考试(三)化学试题河北省保定部分高中2023-2024学年高三上学期9月月考化学试题福建省福州高新区第一中学(闽侯县第三中学)2023-20024学年高三上学期第一次月考化学试题河南省濮阳市油田第一中学2024届高三上学期第一次考试理科综合化学试题
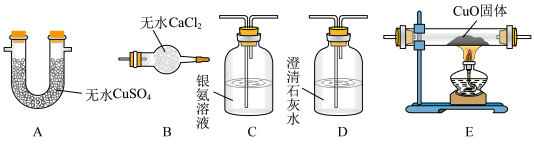
5 . 为探究甲醛与新制Cu(OH)2反应的产物,设计了如下实验。回答下列问题:
I.反应装置如下:
(1)仪器a的名称是___________ ,该反应需控制温度为65℃,宜采用的加热方式为___________ (填标号)。
A.酒精灯加热 B.砂浴 C.油浴 D.水浴
II.为探究气体产物、溶液中产物与固体产物的成分,小组同学经过讨论分析后,关于产物成分有如下猜想:
(2)为确定气体成分,下列实验装置的连接顺序是___________ ( 按气流方向填大写字母,个别装置可重复使用)。(已知:CO与银氨溶液能发生氧化还原反应)___________ 。
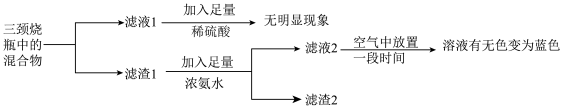
(3)为确定溶液中产物与固体产物,小组做了以下实验: (无色),Cu(NH3)
(无色),Cu(NH3) 易被氧化生成Cu(NH3)
易被氧化生成Cu(NH3) 。
。
①由实验现象可知,液体产物中存在离子是___________ (填离子符号)。
②滤渣1中加入足量浓氨水时,主要反应的离子方程式为___________ 。
③滤液2在空气中放置一段时间后,显蓝色的离子是___________ (填离子符号)。
④通过定量测定发现,固体产物主要是铜。综合以上分析,若主要还原产物的物质的量相等,甲醛与新制氢氧化铜发生的主要反应的化学方程式是___________ 。
I.反应装置如下:
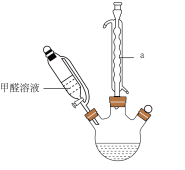
(1)仪器a的名称是
A.酒精灯加热 B.砂浴 C.油浴 D.水浴
II.为探究气体产物、溶液中产物与固体产物的成分,小组同学经过讨论分析后,关于产物成分有如下猜想:
| 气体产物 | H2、CO、CO2 |
| 溶液中产物 | HCOO-、 |
| 固体产物 | Cu、Cu2O |
(3)为确定溶液中产物与固体产物,小组做了以下实验:
 (无色),Cu(NH3)
(无色),Cu(NH3) 易被氧化生成Cu(NH3)
易被氧化生成Cu(NH3) 。
。①由实验现象可知,液体产物中存在离子是
②滤渣1中加入足量浓氨水时,主要反应的离子方程式为
③滤液2在空气中放置一段时间后,显蓝色的离子是
④通过定量测定发现,固体产物主要是铜。综合以上分析,若主要还原产物的物质的量相等,甲醛与新制氢氧化铜发生的主要反应的化学方程式是
您最近一年使用:0次
2023-06-19更新
|
100次组卷
|
4卷引用:青海省西宁市大通回族土族自治县2023-2024学年高三上学期期中考试理综试题
6 . 含硼化合物硼酸( )、硼氢化钠(
)、硼氢化钠( )、硼酸甲酯
)、硼酸甲酯 在工业上有重要用途。回答下列问题:
在工业上有重要用途。回答下列问题:
(1) 在水溶液中会发生如下反应:
在水溶液中会发生如下反应: (反应实质为水电离出的
(反应实质为水电离出的 被还原)。实验测得溶液的碱性越强,该反应的反应速率越小,试解释其中的原因
被还原)。实验测得溶液的碱性越强,该反应的反应速率越小,试解释其中的原因_______ 。
(2)利用硼砂(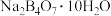 )制备硼酸(
)制备硼酸( )的流程如下图所示:
)的流程如下图所示:
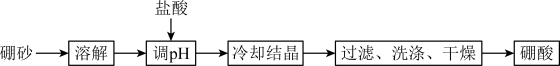
①“调 ”时需要控制溶液
”时需要控制溶液 ,写出用
,写出用 试纸检测溶液
试纸检测溶液 的操作方法:
的操作方法:_______ 。
②“调 ”后溶液中有硼酸生成,写出反应的离子方程式:
”后溶液中有硼酸生成,写出反应的离子方程式:_______ 。
③ 在水中电离方程式为:
在水中电离方程式为: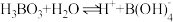 ,
,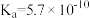 ,据此可判断
,据此可判断 属于
属于_______ 元弱酸,常温下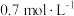 的硼酸溶液中
的硼酸溶液中 的浓度约为
的浓度约为_______ (计算结果保留小数点后一位)。
(3)利用硼酸和甲醇制备硼酸甲酯,发生的反应为: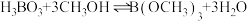 ,不同温度下,硼酸的转化率(
,不同温度下,硼酸的转化率( )随时间变化如图所示:
)随时间变化如图所示:

①该反应的
_______ (填“<”“=”或“>”)0。
②达到平衡时,升高温度,_______ [填“ ”或“
”或“ ”]增大的程度更大。
”]增大的程度更大。
 )、硼氢化钠(
)、硼氢化钠( )、硼酸甲酯
)、硼酸甲酯 在工业上有重要用途。回答下列问题:
在工业上有重要用途。回答下列问题:(1)
 在水溶液中会发生如下反应:
在水溶液中会发生如下反应: (反应实质为水电离出的
(反应实质为水电离出的 被还原)。实验测得溶液的碱性越强,该反应的反应速率越小,试解释其中的原因
被还原)。实验测得溶液的碱性越强,该反应的反应速率越小,试解释其中的原因(2)利用硼砂(
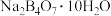 )制备硼酸(
)制备硼酸( )的流程如下图所示:
)的流程如下图所示:
①“调
 ”时需要控制溶液
”时需要控制溶液 ,写出用
,写出用 试纸检测溶液
试纸检测溶液 的操作方法:
的操作方法:②“调
 ”后溶液中有硼酸生成,写出反应的离子方程式:
”后溶液中有硼酸生成,写出反应的离子方程式:③
 在水中电离方程式为:
在水中电离方程式为: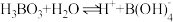 ,
,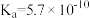 ,据此可判断
,据此可判断 属于
属于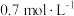 的硼酸溶液中
的硼酸溶液中 的浓度约为
的浓度约为(3)利用硼酸和甲醇制备硼酸甲酯,发生的反应为:
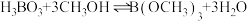 ,不同温度下,硼酸的转化率(
,不同温度下,硼酸的转化率( )随时间变化如图所示:
)随时间变化如图所示:
①该反应的

②达到平衡时,升高温度,
 ”或“
”或“ ”]增大的程度更大。
”]增大的程度更大。
您最近一年使用:0次
2023-02-20更新
|
55次组卷
|
2卷引用:青海省西宁市大通回族土族自治县2022-2023学年高二上学期期末考试化学试题
名校
解题方法
7 . 某含锰废料中主要含MnCO3及少量的FeCO3、SiO2、Cu2(OH)2CO3,以此为原料制备MnO2的流程如下:
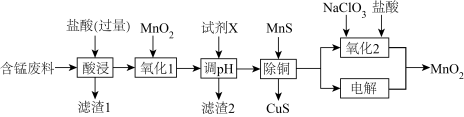
Ⅰ.氢氧化物开始沉淀和完全沉淀的pH如下表:
Ⅱ.常温下Ksp(MnS)=2.0×10-10、Ksp(CuS)=6.0×10-36。
回答下列问题:
(1)滤渣1的主要成分是_________ (填化学式)。
(2)“氧化1”的目的是_________ (用离子方程式表示)。
(3)“调pH”时,试剂X为_________ (任写一种),pH的调节范围为_________ 。
(4)“除铜”时,当溶液中c(Mn2+)=12mol·L-1,溶液中c(Cu2+)=_________  。
。
(5)“氧化2”制备MnO2 (恰好完全反应)时,n(Mn2+):n(ClO )=
)=_________ ( ClO →Cl-);“电解”制备MnO2的阳极电极反应式为
→Cl-);“电解”制备MnO2的阳极电极反应式为_________ 。

Ⅰ.氢氧化物开始沉淀和完全沉淀的pH如下表:
| 氢氧化物 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 |
| 开始沉淀时pH | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀时pH | 9.8 | 8.3 | 3.7 | 6.7 |
回答下列问题:
(1)滤渣1的主要成分是
(2)“氧化1”的目的是
(3)“调pH”时,试剂X为
(4)“除铜”时,当溶液中c(Mn2+)=12mol·L-1,溶液中c(Cu2+)=
 。
。(5)“氧化2”制备MnO2 (恰好完全反应)时,n(Mn2+):n(ClO
 )=
)= →Cl-);“电解”制备MnO2的阳极电极反应式为
→Cl-);“电解”制备MnO2的阳极电极反应式为
您最近一年使用:0次
2022-11-25更新
|
126次组卷
|
4卷引用:青海省西宁市大通县2023-2024学年高二上学期期末考试化学试题
名校
解题方法
8 . 亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______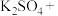 _______
_______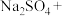 _______
_______
(1)请完成该化学方程式并配平。_______
(2) 中N的化合价为
中N的化合价为_______ ,由N的化合价推测 具有
具有_______ (填“氧化性”、“还原性”或“氧化性、还原性”)。
(3)用上述反应来处理 并不是最佳方法,其原因是
并不是最佳方法,其原因是_______ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的_______ (填“氧化性”或“还原性”)应该比 更
更_______ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和
和 的是_______(填序号)。
的是_______(填序号)。
(5) 与
与 反应:
反应: ,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是
,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是_______ mol。
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式_______ 。
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: _______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______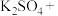 _______
_______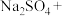 _______
_______
(1)请完成该化学方程式并配平。
(2)
 中N的化合价为
中N的化合价为 具有
具有(3)用上述反应来处理
 并不是最佳方法,其原因是
并不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的 更
更(4)下列方法不能用来区分固体
 和
和 的是_______(填序号)。
的是_______(填序号)。| A.分别溶于水并滴加酚酞试液 | B.分别溶于水并滴加 酸化的 酸化的 溶液 溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
 与
与 反应:
反应: ,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是
,若有0.5mol氧化剂被还原,则被氧化的还原剂的物质的量是(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式
您最近一年使用:0次
名校
解题方法
9 . 高锰酸钾具有强氧化性,广泛应用于化工、医药、金属冶炼等领域。实验室可通过固体碱溶氧化法制备高锰酸钾。回答下列问题:
(1)称取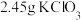 和
和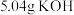 ,置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要
,置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要_______ (填仪器名称),不使用瓷坩埚的原因是_______ 。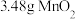 分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色
分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色 。该步反应的化学方程式为
。该步反应的化学方程式为_______ ,分多次加入 的原因是
的原因是_______ 。
(3)待铁坩埚冷却后,将其置于蒸馏水中共煮至固体全部溶解。趁热向浸取液中通入 ,使
,使 歧化为
歧化为 与
与 。用玻璃棒蘸取溶液于滤纸上,观察到
。用玻璃棒蘸取溶液于滤纸上,观察到_______ ,表明转化已完全。静置片刻,抽滤。该步骤若用 代替
代替 ,可能的后果是
,可能的后果是_______ 。
(4)水浴加热滤液至出现 晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热的主要优点是
晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热的主要优点是_______ 。下表是部分化合物溶解度随温度变化的数据,步骤(3)中 不宜通入过多,目的是
不宜通入过多,目的是_______ ,产品经纯化后称重,质量为3.60g。本实验中 的产率为
的产率为_______ %。
(1)称取
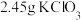 和
和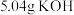 ,置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要
,置于铁坩埚中并混合均匀,加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要
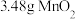 分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色
分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿色 。该步反应的化学方程式为
。该步反应的化学方程式为 的原因是
的原因是(3)待铁坩埚冷却后,将其置于蒸馏水中共煮至固体全部溶解。趁热向浸取液中通入
 ,使
,使 歧化为
歧化为 与
与 。用玻璃棒蘸取溶液于滤纸上,观察到
。用玻璃棒蘸取溶液于滤纸上,观察到 代替
代替 ,可能的后果是
,可能的后果是(4)水浴加热滤液至出现
 晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热的主要优点是
晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热的主要优点是 不宜通入过多,目的是
不宜通入过多,目的是 的产率为
的产率为| 温度/℃ | 20 | 30 | 40 | 50 |
 | 110 | 114 | 117 | 121 |
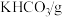 | 33.7 | 39.9 | 47.5 | 65.6 |
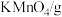 | 6.4 | 9.0 | 12.6 | 16.9 |
您最近一年使用:0次
2022-11-05更新
|
910次组卷
|
5卷引用:2024届青海省西宁市高三下学期一模理综试卷-高中化学
解题方法
10 . 写出下列反应的化学方程式,是离子反应的写出离子方程式。
(1)澄清石灰水与盐酸反应:_______ 。
(2)氢氧化钠与硫酸反应:_______ 。
(3)过氧化氢分解反应:_______ 。
(4)硫酸铜与氢氧化钠反应:_______ 。
(5)氯化钡与硫酸钠反应:_______ 。
(6)氢氧化钙溶液与二氧化碳反应:_______ 。
(1)澄清石灰水与盐酸反应:
(2)氢氧化钠与硫酸反应:
(3)过氧化氢分解反应:
(4)硫酸铜与氢氧化钠反应:
(5)氯化钡与硫酸钠反应:
(6)氢氧化钙溶液与二氧化碳反应:
您最近一年使用:0次



