23. 甲醇(CH
3OH)和二甲醚(CH
3OCH
3)被称为21世纪的新型燃料,具有清洁、高效等性能。
(1)CO
2可用于合成二甲醚(CH
3OCH
3),有关反应的热化学方程式如下:
CO
2(g) + 3H
2(g)=CH
3OH(g) + H
2O(g) △H=-49.0 kJ·mol
-12CH
3OH(g)=CH
3OCH
3(g) + H
2O(g) △H=-23.5 kJ·mol
-1H
2O(l)=H
2O(g) △H= + 44 kJ·mol
-1则CO
2与H
2反应合成二甲醚生成液态水的热化学方程式为:
____________________。
(2)工业上合成甲醇的反应:CO(g)+2H
2(g)

CH
3OH(g) △H=-90.8 kJ·mol
-1。 下列
不能说明该反应在恒温恒容条件下已达化学平衡状态的是
___________A.v
正(H
2) = 2v
逆(CH
3OH) B.n(CO):n(H
2):n(CH
3OH)=1:2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
E.容器的压强不变
(3)若反应2CH
3OH(g)

CH
3OCH
3(g) + H
2O(g)在某温度下的化学平衡常数为400,此温度下,在密闭容器中加入一定量甲醇,反应进行到某时刻,测得各物质的浓度如下表所示:
| 物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 浓度(mol·L-1) | 0.44 | 0.60 | 0.60 |
①比较该时刻正、逆反应速率的大小:v(正)
_____v(逆)(填“>”、“<”或“=”)。
②若加入甲醇后,经10 min反应达到平衡,则平衡后c(CH
3OH)=
______________,
该时间内反应速率v(CH
3OCH
3)=
_____________。
(4)利用二甲醚(CH
3OCH
3)设计一个燃料电池,用KOH溶液作电解质溶液,石墨做电极,该电池负极电极反应式为
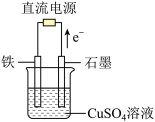
___________________________。以此燃料电池作为外接电源按如图所示电解硫酸铜溶液,如果起始时盛有1000mLpH=5的硫酸铜溶液(25℃,CuSO
4足量),一段时间后溶液的pH变为1,若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入
______其质量约为
_____g。