1 . 某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是___________ 。
(2)已知2个KBrO3在反应中得到10个电子生成X,则X的化学式为___________ 。
(3)根据上述反应可推知___________。
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并用单线桥法标出电子转移的方向和数目:  。
。___________
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是
(2)已知2个KBrO3在反应中得到10个电子生成X,则X的化学式为
(3)根据上述反应可推知___________。
| A.氧化性:KBrO3>H3AsO4 | B.氧化性:H3AsO4>KBrO3 |
| C.还原性:AsH3>X | D.还原性:X>AsH3 |
 。
。
您最近一年使用:0次
20-21高一下·江苏无锡·期中
名校
2 . 电视剧《西游记》中仙境美仑美奂,这些神话仙境中所需的烟雾是 和
和 粉按质量比
粉按质量比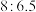 混合放于温热的石棉网上,使用时滴水数滴即产生大量的白烟。又知发生反应后有
混合放于温热的石棉网上,使用时滴水数滴即产生大量的白烟。又知发生反应后有 和水生成。有关的说法中正确的是
和水生成。有关的说法中正确的是
①水起着溶解 ,发生吸热现象以启动反应的发生的作用;②每还原
,发生吸热现象以启动反应的发生的作用;②每还原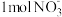 需氧化
需氧化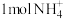 和
和 ;③成烟物质是两性氧化物小颗粒;④成烟物质是小锌粒,它由
;③成烟物质是两性氧化物小颗粒;④成烟物质是小锌粒,它由 反应放热而蒸出。
反应放热而蒸出。
 和
和 粉按质量比
粉按质量比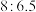 混合放于温热的石棉网上,使用时滴水数滴即产生大量的白烟。又知发生反应后有
混合放于温热的石棉网上,使用时滴水数滴即产生大量的白烟。又知发生反应后有 和水生成。有关的说法中正确的是
和水生成。有关的说法中正确的是①水起着溶解
 ,发生吸热现象以启动反应的发生的作用;②每还原
,发生吸热现象以启动反应的发生的作用;②每还原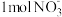 需氧化
需氧化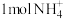 和
和 ;③成烟物质是两性氧化物小颗粒;④成烟物质是小锌粒,它由
;③成烟物质是两性氧化物小颗粒;④成烟物质是小锌粒,它由 反应放热而蒸出。
反应放热而蒸出。| A.①② | B.②③ | C.③④ | D.①④ |
您最近一年使用:0次
2021-04-17更新
|
535次组卷
|
3卷引用:第二章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
(已下线)第二章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)江苏省天一中学2020-2021学年高一下学期期中考试(强化班)化学试题河北沧州泊头一中2020-2021学年高一下学期第二次月考化学试卷
19-20高三·江苏苏州·期末
名校
3 . 铁及其化合物在处理工业废水、废气过程中发挥着重要作用。
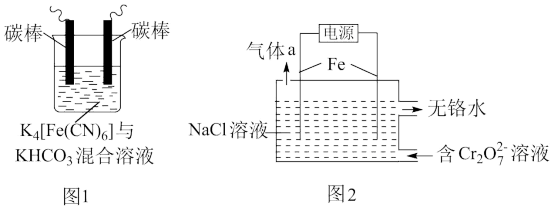
(1)用铁的化合物除硫化氢:2[Fe(CN)6]3-+ 2 +HS- =2[Fe(CN)6]4-+ 2
+HS- =2[Fe(CN)6]4-+ 2 +S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为_______ ;电解过程中阴极区溶液的pH_______ (填“变大”、 “变小”或“不变")。
(2)以铁为电极电解除铬,如图2
已知: + H2O=2
+ H2O=2 +2H+
+2H+
氧化性: >
>
①电解过程中主要反应之一: +6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是
+6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是_______ 。
②电解过程中,不同pH时,通电时间与Cr元素的去除率关系如图3所示,pH=10相比pH=4,Cr元素的去除率偏低的原因可能是_______ 。
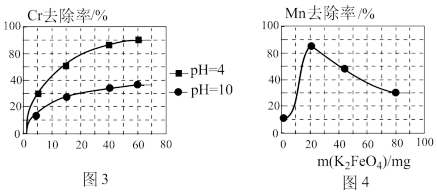
(3)高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式_______ 。
②用K2FeO4处理1L 50 mg/L的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图4所示,当K2FeO4超过20 mg时,Mn元素的去除率下降的原因可能是_______ 。

(1)用铁的化合物除硫化氢:2[Fe(CN)6]3-+ 2
 +HS- =2[Fe(CN)6]4-+ 2
+HS- =2[Fe(CN)6]4-+ 2 +S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为
+S↓,可通过图1使[Fe(CN)6]3-再生,电解时,阳极的电极反应式为(2)以铁为电极电解除铬,如图2
已知:
 + H2O=2
+ H2O=2 +2H+
+2H+氧化性:
 >
>
①电解过程中主要反应之一:
 +6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是
+6Fe2++17H2O= 2Cr(OH)3↓+6Fe(OH)3↓+10H+;气体a主要成分是②电解过程中,不同pH时,通电时间与Cr元素的去除率关系如图3所示,pH=10相比pH=4,Cr元素的去除率偏低的原因可能是

(3)高铁酸钾(K2FeO4)除锰
已知:K2FeO4具有强氧化性,极易溶于水
①在酸性条件下,能与废水中的Mn2+反应生成Fe(OH)3和MnO2沉淀来除锰,该反应的离子方程式
②用K2FeO4处理1L 50 mg/L的含Mn2+废水,Mn元素的去除率与K2FeO4量的关系如图4所示,当K2FeO4超过20 mg时,Mn元素的去除率下降的原因可能是
您最近一年使用:0次
2021-03-25更新
|
449次组卷
|
5卷引用:2.3.1 浓度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)
(已下线)2.3.1 浓度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)【苏州新东方】化学试卷湖北省武汉市蔡甸区汉阳一中2021-2022学年高二上学期12月月考化学试题湖北省武汉市部分重点中学2021-2022学年高二上学期12月联考化学试题江苏省常州市第一中学2023-2024学年高二上学期11月期中考试化学试题
4 . 将 通入足量
通入足量 溶液中,完全反应后再加入
溶液中,完全反应后再加入 溶液,发生的两个化学反应为①
溶液,发生的两个化学反应为①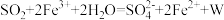 ,②
,②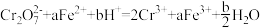 。下列有关说法正确的是
。下列有关说法正确的是
 通入足量
通入足量 溶液中,完全反应后再加入
溶液中,完全反应后再加入 溶液,发生的两个化学反应为①
溶液,发生的两个化学反应为①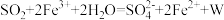 ,②
,②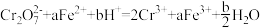 。下列有关说法正确的是
。下列有关说法正确的是A.还原性:  |
B.方程式②中, |
C. 能将 能将 氧化成 氧化成 |
D.方程式①中 为 为 |
您最近一年使用:0次
2021-01-11更新
|
581次组卷
|
2卷引用:专题4 本专题复习提升-高中化学苏教2019版必修第一册
5 .  、NO是大气污染物。吸收
、NO是大气污染物。吸收 和NO,获得
和NO,获得 和
和 产品的流程图(图1)如下(Ce为铈元素):
产品的流程图(图1)如下(Ce为铈元素):
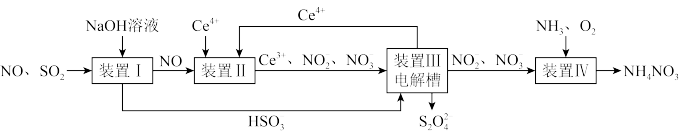
图1
(1)装置Ⅰ中生成 的离子方程式为
的离子方程式为_________________________________________________ 。
(2)各含硫微粒(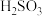 、
、 和
和 )存在于
)存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数与溶液pH的关系如图2所示(常温下)。
与NaOH溶液反应后的溶液中,它们的物质的量分数与溶液pH的关系如图2所示(常温下)。
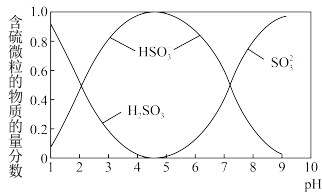
图2
①下列说法正确的是__________ (填序号)。
a. 时,溶液中
时,溶液中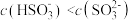
b. 时,溶液中
时,溶液中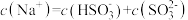
c.为获得尽可能纯的 ,可将溶液的pH控制在4~5
,可将溶液的pH控制在4~5
②向 的
的 溶液中滴加一定浓度的
溶液中滴加一定浓度的 溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:
溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:_____________________________________________ 。
(3)装置Ⅱ中,酸性条件下,NO被 氧化的产物主要是
氧化的产物主要是 、
、 ,写出生成
,写出生成 (无
(无 )的离子方程式:
)的离子方程式:_____________________________________________ 。
(4)已知进入装置Ⅳ的溶液中, 的浓度为
的浓度为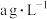 ,要使
,要使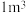 该溶液中的
该溶液中的 完全转化为
完全转化为 ,需至少向装置Ⅳ中通入标准状况下的
,需至少向装置Ⅳ中通入标准状况下的
__________ L。(用含a的代数式表示)
 、NO是大气污染物。吸收
、NO是大气污染物。吸收 和NO,获得
和NO,获得 和
和 产品的流程图(图1)如下(Ce为铈元素):
产品的流程图(图1)如下(Ce为铈元素):
图1
(1)装置Ⅰ中生成
 的离子方程式为
的离子方程式为(2)各含硫微粒(
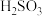 、
、 和
和 )存在于
)存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数与溶液pH的关系如图2所示(常温下)。
与NaOH溶液反应后的溶液中,它们的物质的量分数与溶液pH的关系如图2所示(常温下)。
图2
①下列说法正确的是
a.
 时,溶液中
时,溶液中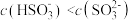
b.
 时,溶液中
时,溶液中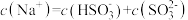
c.为获得尽可能纯的
 ,可将溶液的pH控制在4~5
,可将溶液的pH控制在4~5②向
 的
的 溶液中滴加一定浓度的
溶液中滴加一定浓度的 溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:
溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:(3)装置Ⅱ中,酸性条件下,NO被
 氧化的产物主要是
氧化的产物主要是 、
、 ,写出生成
,写出生成 (无
(无 )的离子方程式:
)的离子方程式:(4)已知进入装置Ⅳ的溶液中,
 的浓度为
的浓度为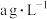 ,要使
,要使 该溶液中的
该溶液中的 完全转化为
完全转化为 ,需至少向装置Ⅳ中通入标准状况下的
,需至少向装置Ⅳ中通入标准状况下的
您最近一年使用:0次
2020-10-12更新
|
530次组卷
|
3卷引用:鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过模拟 2年模拟精编精练
6 . 某离子反应涉及H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
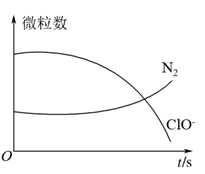
 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
| A.该反应中Cl-为氧化产物 |
| B.消耗1个还原剂微粒,转移6e- |
C. 被ClO-氧化成N2 被ClO-氧化成N2 |
| D.反应后溶液的酸性减弱 |
您最近一年使用:0次
2020-10-02更新
|
1131次组卷
|
8卷引用:人教版(2019)高一必修第一册 第一章 物质及其变化 第三节 氧化还原反应 方法帮
7 . 写出下列反应的离子方程式(已知还原性: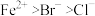 ):
):
(1)向 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 ):
):_________ ;
(2)向 溶液中通入足量
溶液中通入足量 :
:______ ;
(3)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:______ 。
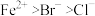 ):
):(1)向
 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 ):
):(2)向
 溶液中通入足量
溶液中通入足量 :
:(3)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:
您最近一年使用:0次
2020-10-01更新
|
1459次组卷
|
3卷引用:人教版(2019)高一必修第一册 第一章 物质及其变化 章末总结
解题方法
8 . 化学实验中,如使某步反应中的有害产物作为另一步反应的反应物,形成一个循环,就可不再向环境排放该种有害物质。如图所示。
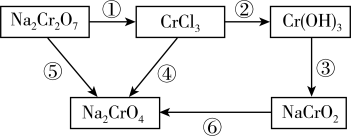
(1)配平反应方程式并回答问题,用单线桥标出两个反应的电子转移的方向和数目。
反应①: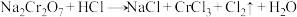 ,
,__________ ,氧化剂为__________ (填化学式,后同),氧化产物为__________ 。
反应⑥: ,
,__________ ,还原剂为__________ ,还原产物为__________ 。
(2)在上述有编号的步骤中,除了①⑥外,还需用到氧化剂的步骤是__________ (填编号)。

(1)配平反应方程式并回答问题,用单线桥标出两个反应的电子转移的方向和数目。
反应①:
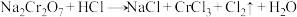 ,
,反应⑥:
 ,
,(2)在上述有编号的步骤中,除了①⑥外,还需用到氧化剂的步骤是
您最近一年使用:0次
2020-09-23更新
|
1586次组卷
|
5卷引用:人教版(2019)高一必修第一册 第一章 物质及其变化 第三节 氧化还原反应 方法帮
人教版(2019)高一必修第一册 第一章 物质及其变化 第三节 氧化还原反应 方法帮高一必修第一册(苏教2019)专题4 第二单元 硫及其化合物的相互转化1高一必修第一册(鲁科2019)第2章 章末综合检测卷(已下线)第05讲 氧化还原反应(讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )(已下线)第05讲 氧化还原反应(讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )
解题方法
9 . 锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选。正极材料的选择决定了锂离子电池的性能。磷酸亚铁锂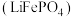 以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
(1)高温固相法是生产磷酸亚铁锂的主要方法。通常以亚铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛中先经过较低温预分解,再经高温焙烧,最后研磨粉碎制成。请回答下列问题:
①补充完整该反应的化学方程式: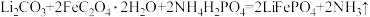
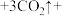
_____ 
______ 。
②理论上,反应中每转移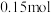 电子,会生成
电子,会生成
_____ g。
③反应需在惰性气氛中进行,其原因是____________ 。
(2)磷酸亚铁锂电池装置如图所示,其中正极材料橄榄石型 通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
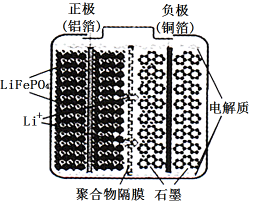
电池工作时的总反应为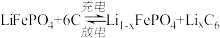 ,则放电时,正极的电极反应式为
,则放电时,正极的电极反应式为________ ,充电时, 迁移方向为
迁移方向为_____ (填“由左向右”或“由右向左”),图中聚合物隔膜应为_____ (填“阳”或“阴”)离子交换膜。
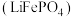 以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。
以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”。(1)高温固相法是生产磷酸亚铁锂的主要方法。通常以亚铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛中先经过较低温预分解,再经高温焙烧,最后研磨粉碎制成。请回答下列问题:
①补充完整该反应的化学方程式:
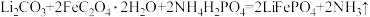
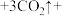

②理论上,反应中每转移
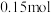 电子,会生成
电子,会生成
③反应需在惰性气氛中进行,其原因是
(2)磷酸亚铁锂电池装置如图所示,其中正极材料橄榄石型
 通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
通过黏合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐。
电池工作时的总反应为
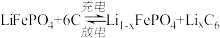 ,则放电时,正极的电极反应式为
,则放电时,正极的电极反应式为 迁移方向为
迁移方向为
您最近一年使用:0次
2020-09-19更新
|
805次组卷
|
3卷引用:鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第2节 化学能转化为电能——电池
鲁科版(2019)选择性必修1 第1章 化学反应与能量转化 第2节 化学能转化为电能——电池山东省青岛通济实验学校学校2021届高三上学期10月月考化学试题(已下线)练习8 原电池 化学电源-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)
解题方法
10 . 配平下列反应方程式。
(1)正向配平类
①___ HCl(浓)+___ MnO2
___ Cl2↑+___ MnCl2+___ H2O
②___ KI+___ KIO3+___ H2SO4=____ I2+___ K2SO4+___ H2O
③___ MnO +
+___ H++___ Cl-=___ Mn2++___ Cl2↑+___ H2O
(2)逆向配平类
①___ S+___ KOH=___ K2S+___ K2SO3+___ H2O
②___ P4+___ KOH+___ H2O=___ K3PO4+___ PH3↑
(3)缺项配平类
①___ ClO-+___ Fe(OH)3+___ =___ Cl-+___ FeO +
+___ H2O
②___ MnO +
+___ H2O2+___ =___ Mn2++___ O2↑+___ H2O
③某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有Al2O3、C、N2、AlN、CO。请将反应物与生成物分别填入以下空格内,并配平。___

(1)正向配平类
①

②
③
 +
+(2)逆向配平类
①
②
(3)缺项配平类
①
 +
+②
 +
+③某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有Al2O3、C、N2、AlN、CO。请将反应物与生成物分别填入以下空格内,并配平。

您最近一年使用:0次
2020-09-02更新
|
2216次组卷
|
3卷引用:苏教版(2020)高一必修第一册专题4 突破3 氧化还原反应与离子反应的综合应用
苏教版(2020)高一必修第一册专题4 突破3 氧化还原反应与离子反应的综合应用鲁科版(2019)高一必修第一册第2章 元素与物质世界 第3节 氧化还原反应 专题4 氧化还原反应的计算及方程式的配平(已下线)易错专题07 氧化还原反应电子转移的表示及方程式的书写-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)



