解题方法
1 . 硼镁泥是硼镁矿生产硼砂晶体(Na2B4O7·10H2O)时的废渣,其主要成分是MgO,还含有Na2B4O7、CaO、Fe2O3、FeO、Al2O3、SiO2等杂质。以硼镁泥为原料制取七水硫酸镁的工艺流程如图所示。
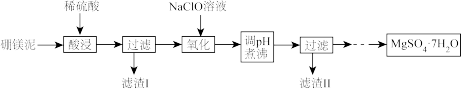
回答下列问题:
(1)硼与浓的氢氧化钠溶液在加热条件下有类似硅的反应,反应后硼元素以BO 形式存在于溶液中,写出硼与浓的氢氧化钠溶液反应的化学方程式:
形式存在于溶液中,写出硼与浓的氢氧化钠溶液反应的化学方程式:_______ 。
(2) Na2B4O7易溶于水,较易发生水解:B4O +7H2O⇌4H3BO3(硼酸) +2OH- (硼酸在常温下溶解度较小)。则滤渣I中除CaSO4外还有
+7H2O⇌4H3BO3(硼酸) +2OH- (硼酸在常温下溶解度较小)。则滤渣I中除CaSO4外还有_______ 、_______ (填化学式)。
(3)“氧化”过程中发生反应的离子方程式为_______ 。
(4)工艺流程中“调pH”应不低于_______ 。 (已知:常温下,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0 ×10-33;当溶液中离子浓度小于等于1 ×10-6mol·L-1时认为该离子沉淀完全)。“煮沸”的目的是_______ 。
(5)该工艺流程中包含多次过滤操作,实验室中过滤后洗涤沉淀的操作为_______ 。
(6)我国科学家研发出以惰性电极材料电解NaBO2的碱性溶液制备NaBH4的方法。阴极产生NaBH4则阳极的电极反应式为。_______ 。

回答下列问题:
(1)硼与浓的氢氧化钠溶液在加热条件下有类似硅的反应,反应后硼元素以BO
 形式存在于溶液中,写出硼与浓的氢氧化钠溶液反应的化学方程式:
形式存在于溶液中,写出硼与浓的氢氧化钠溶液反应的化学方程式:(2) Na2B4O7易溶于水,较易发生水解:B4O
 +7H2O⇌4H3BO3(硼酸) +2OH- (硼酸在常温下溶解度较小)。则滤渣I中除CaSO4外还有
+7H2O⇌4H3BO3(硼酸) +2OH- (硼酸在常温下溶解度较小)。则滤渣I中除CaSO4外还有(3)“氧化”过程中发生反应的离子方程式为
(4)工艺流程中“调pH”应不低于
(5)该工艺流程中包含多次过滤操作,实验室中过滤后洗涤沉淀的操作为
(6)我国科学家研发出以惰性电极材料电解NaBO2的碱性溶液制备NaBH4的方法。阴极产生NaBH4则阳极的电极反应式为。
您最近半年使用:0次
解题方法
2 . 下列有关离子方程式的书写错误的是
A.向饱和NaCl溶液中依次通入足量NH3与CO2:Na++NH3+ CO2+ H2O=NaHCO3↓+NH |
B.向硫酸铝溶液中加入过量氨水:Al3+ +3NH3·H2O=Al(OH)3↓+ 3NH |
C.碳酸氢镁溶液与足量氢氧化钠溶液反应:Mg2++2HCO +4OH-=Mg(OH)2↓+2CO +4OH-=Mg(OH)2↓+2CO +2H2O +2H2O |
D.草酸与足量酸性高锰酸钾溶液反应:2MnO +5C2O +5C2O + 16H+=2Mn2++10CO2↑+8H2O + 16H+=2Mn2++10CO2↑+8H2O |
您最近半年使用:0次
解题方法
3 . 钴具有广泛用途,其正三价化合物具有强氧化性。利用低硫钴矿(含Ca、Fe、Al、Mn、Mg、Co等元素的硫化物及SiO2)可以制取多种化工试剂,采用以下工艺流程可利用低硫钴矿制备CoCO3。
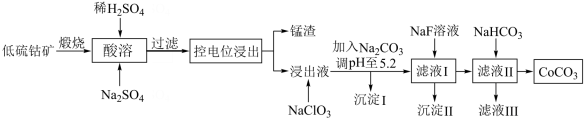
已知下列信息:
①常温下,Ksp(CaF2)=4.9×10-10,Ksp(MgF2)=6.4×10-12;
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)进行“酸溶”时,能提高“酸溶”速率的方法有___________ (任写1种)。
(2)酸溶时Co2O3被还原为Co2+,同时还有___________ 离子被还原。写出Co2O3转化为Co2+反应的离子方程式___________ 。
(3)加入NaClO的作用是___________ 。
(4)加入Na2CO3调pH至5.2,目的是___________ 。沉淀的I主要成分为___________
(5)为了将Mg2+、Ca2+除去[c(Mg2+)、c(Ca2+)≤1×10-5mol/L],加入NaF使“滤液I”中c(F-)最小为___________ mol/L。
(6)“沉钴”步骤的离子方程式是___________ 。

已知下列信息:
①常温下,Ksp(CaF2)=4.9×10-10,Ksp(MgF2)=6.4×10-12;
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 1.9 | 7.0 | 7.6 | 3.0 | 8.1 |
| 完全沉淀 | 3.2 | 9.0 | 9.2 | 4.7 | 10.1 |
(1)进行“酸溶”时,能提高“酸溶”速率的方法有
(2)酸溶时Co2O3被还原为Co2+,同时还有
(3)加入NaClO的作用是
(4)加入Na2CO3调pH至5.2,目的是
(5)为了将Mg2+、Ca2+除去[c(Mg2+)、c(Ca2+)≤1×10-5mol/L],加入NaF使“滤液I”中c(F-)最小为
(6)“沉钴”步骤的离子方程式是
您最近半年使用:0次
名校
4 . 2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效灭活新冠病毒,为阻断疫情做出了巨大贡献。二氧化氯(ClO2)就是其中一种高效消毒灭菌剂。氯酸钠还原法是目前使用较为广泛的ClO2制备方法,其中一种是用NaClO3与CH3OH在催化剂、60℃时,发生反应得到ClO2,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
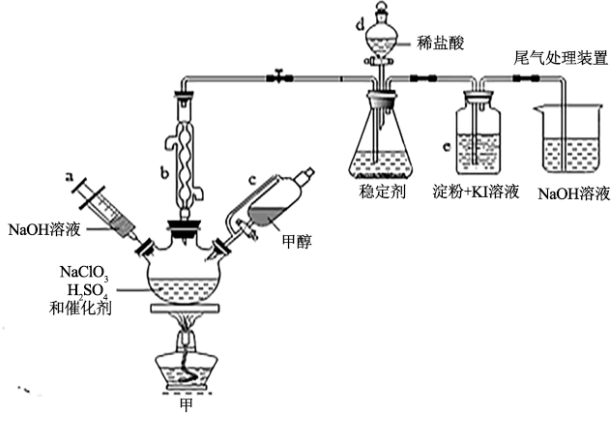
已知:①ClO2的浓度较大时易分解爆炸,一般用CO2或空气稀释到10%以下,实验室也常用稳定剂吸收ClO2,生成NaClO2,使用时加酸只释放出ClO2一种气体;
②ClO2与KI反应的离子方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O
③有关物质沸点如下表;
请回答:
(1)仪器b的名称是___________ ,在装置中的作用是___________ ;比较仪器c和d,实验中c的优点是___________ 。
(2)根据反应条件判断制备装置甲中需改进的一项措施是___________ 。
(3)反应中甲醇被氧化为甲酸,写出制备ClO2的化学方程式:___________ 。该制备法可选用不同的还原性物质作为还原剂例如草酸(草酸的氧化产物为CO2),相比甲醇法,草酸法的优点是___________ 。
(4)下列有关说法正确的是___________ 。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的ClO2
B.装置e主要用于检验是否有Cl2生成
C.在ClO2释放实验中,发生的离子反应方程式是:4H++5 =Cl-+4ClO2↑+2H2O
=Cl-+4ClO2↑+2H2O
D.ClO2和Cl2都为强氧化剂,在相同条件下,等物质的量时,Cl2的氧化能力是ClO2的2.5倍
(5)采用以下方法可以测定所制备的ClO2的量:
Ⅰ.将足量KI用100mL水溶解后加入到锥形瓶,再加3mL稀 ;
;
Ⅱ.将生成的ClO2气体通过导管在锥形瓶中被吸收
Ⅲ.滴加几滴淀粉溶液,用cmol/L的 标准溶液滴定(
标准溶液滴定( ),共用去
),共用去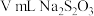 溶液:
溶液:
①达到滴定终点的现象是___________ 。
②实验测得所通入的ClO2的质量为___________ 。

已知:①ClO2的浓度较大时易分解爆炸,一般用CO2或空气稀释到10%以下,实验室也常用稳定剂吸收ClO2,生成NaClO2,使用时加酸只释放出ClO2一种气体;
②ClO2与KI反应的离子方程式为:2ClO2+10I-+8H+=2Cl-+5I2+4H2O
③有关物质沸点如下表;
| 物质 | CH3OH | HCOOH | ClO2 |
| 沸点 | 64.7℃ | 100.8℃ | 11℃ |
(1)仪器b的名称是
(2)根据反应条件判断制备装置甲中需改进的一项措施是
(3)反应中甲醇被氧化为甲酸,写出制备ClO2的化学方程式:
(4)下列有关说法正确的是
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的ClO2
B.装置e主要用于检验是否有Cl2生成
C.在ClO2释放实验中,发生的离子反应方程式是:4H++5
 =Cl-+4ClO2↑+2H2O
=Cl-+4ClO2↑+2H2OD.ClO2和Cl2都为强氧化剂,在相同条件下,等物质的量时,Cl2的氧化能力是ClO2的2.5倍
(5)采用以下方法可以测定所制备的ClO2的量:
Ⅰ.将足量KI用100mL水溶解后加入到锥形瓶,再加3mL稀
 ;
;Ⅱ.将生成的ClO2气体通过导管在锥形瓶中被吸收
Ⅲ.滴加几滴淀粉溶液,用cmol/L的
 标准溶液滴定(
标准溶液滴定( ),共用去
),共用去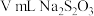 溶液:
溶液:①达到滴定终点的现象是
②实验测得所通入的ClO2的质量为
您最近半年使用:0次
2021-05-23更新
|
610次组卷
|
2卷引用:西藏自治区昌都市第一高级中学2021届高三第一次仿真考试理科综合化学试题
5 . 水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:

回答下列问题:
(1)沉淀A的主要成分是__ 。
(2)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__ ,请写出相应的离子方程式:__ 。
(3)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,实验中称取0.400g水泥样品,滴定时消耗了0.0500mol•L-1KMnO4溶液36.00mL。
①请配平此滴定过程中的反应。
___ MnO +
+___ H++___ H2C2O4——___ Mn2++___ CO2+___ H2O
②求该水泥样品中钙的质量分数为___ 。

回答下列问题:
(1)沉淀A的主要成分是
(2)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(3)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,实验中称取0.400g水泥样品,滴定时消耗了0.0500mol•L-1KMnO4溶液36.00mL。
①请配平此滴定过程中的反应。
 +
+②求该水泥样品中钙的质量分数为
您最近半年使用:0次
解题方法
6 . 亚硝酸钠广泛用于媒染剂、漂白剂等。某兴趣小组用下列装置制取较纯净的NaNO2。
甲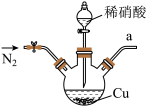 乙
乙 丙
丙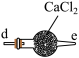 丁
丁
反应原理为:2NO+Na2O2=2NaNO2。已知:NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。下列分析错误的是
甲
 乙
乙 丙
丙 丁
丁
反应原理为:2NO+Na2O2=2NaNO2。已知:NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。下列分析错误的是
| A.甲中滴入稀硝酸前需通入N2 |
| B.仪器的连接顺序为a-f-g-d-e-b |
| C.丙中CaCl2用于干燥NO |
| D.乙中吸收尾气时发生的离子反应为3MnO4-+5NO+4H+=3Mn2++5NO3-+2H2O |
您最近半年使用:0次
2020-04-10更新
|
593次组卷
|
6卷引用:西藏自治区昌都市第一高级中学2020届高三下学期第二次模拟考试理综化学试题
西藏自治区昌都市第一高级中学2020届高三下学期第二次模拟考试理综化学试题四川省成都市2020届高中毕业班第二次诊断性检测理综化学试题湖南省邵阳市重点学校2020届高三综合模拟考试理综化学试题(已下线)第二单元 化学物质的变化测试题-2021年高考化学一轮复习名师精讲练(已下线)第26讲 化学实验基本操作及实验安全-2021年高考化学一轮复习名师精讲练福建省龙岩市第一中学锦山学校2021-2022学年高三上学期第三次月考化学试题
解题方法
7 . 氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如图所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以 、
、 、
、 、
、 的形式存在。
的形式存在。
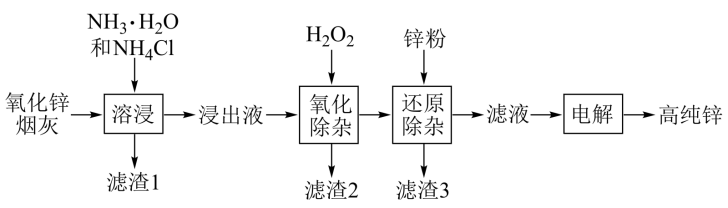
回答下列问题:
 中Zn的化合价为
中Zn的化合价为_______ ,“溶浸”中ZnO发生反应的离子方程式为_______ 。
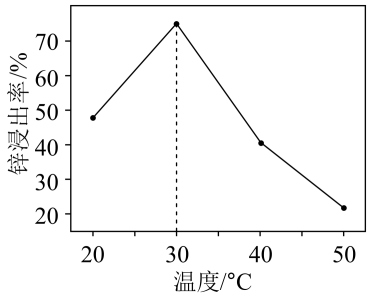
 锌浸出率与温度的关系如图所示,分析
锌浸出率与温度的关系如图所示,分析 时锌浸出率最高的原因为
时锌浸出率最高的原因为_______ 。
 “氧化除杂”中,
“氧化除杂”中, 转化为
转化为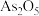 胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为
胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为_______ 。
 “滤渣3”的主要成分为
“滤渣3”的主要成分为_______ 。
 “电解”时
“电解”时 在阴极放电的电极反应式为
在阴极放电的电极反应式为______ 。阳极区放出一种无色无味的气体,将其通入滴有KSCN的 溶液中,无明显现象,该气体是
溶液中,无明显现象,该气体是_______  写化学式
写化学式 。电解后的电解液经补充
。电解后的电解液经补充_______  写一种物质的化学式
写一种物质的化学式 后可返回“溶浸”工序继续使用。
后可返回“溶浸”工序继续使用。
 、
、 、
、 、
、 的形式存在。
的形式存在。
回答下列问题:
 中Zn的化合价为
中Zn的化合价为 锌浸出率与温度的关系如图所示,分析
锌浸出率与温度的关系如图所示,分析 时锌浸出率最高的原因为
时锌浸出率最高的原因为
 “氧化除杂”中,
“氧化除杂”中, 转化为
转化为 胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为
胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为 “滤渣3”的主要成分为
“滤渣3”的主要成分为 “电解”时
“电解”时 在阴极放电的电极反应式为
在阴极放电的电极反应式为 溶液中,无明显现象,该气体是
溶液中,无明显现象,该气体是 写化学式
写化学式 。电解后的电解液经补充
。电解后的电解液经补充 写一种物质的化学式
写一种物质的化学式 后可返回“溶浸”工序继续使用。
后可返回“溶浸”工序继续使用。
您最近半年使用:0次
2020-02-03更新
|
181次组卷
|
2卷引用:西藏拉萨市2020届高三第一次模拟考试理科综合化学试题
8 . 铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(主要含BeO、CuS,还含少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:
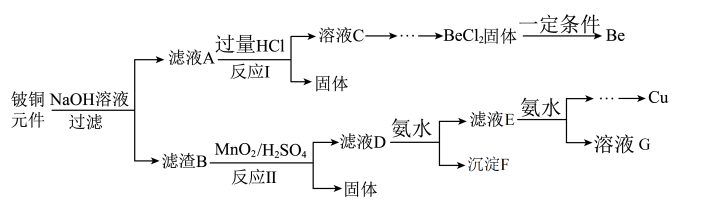
已知:i.铍、铝元素化学性质相似;BeCl2熔融时能微弱电离。
ii.常温下:Ksp[Cu(OH)2]=2.2×10-20, Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13。
回答下列问题:
(1)滤液A的主要成分除NaOH外,还有___________ (填化学式);写出反应I中含铍化合物与过量盐酸反应的离子方程式:___________ 。
(2)滤液C中含NaCl、BeCl2和少量HCl,为得到较纯净的BeCl2溶液,选择下列实验操作最合理步骤的顺序是___________ ;电解熔融BeCl2制备金属铍时,需要加入NaCl,其作用是___________ 。
①加入过量的NaOH:②加入过量的氨水;③加入适量的HCl;④过滤;⑤洗涤。
(3)反应Ⅱ中CuS的氧化产物为S单质,该反应的化学方程式为___________ 。
(4)常温下,若滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,生成沉淀F是________ (填化学式);为了尽可能多的回收铜,所得滤液G的pH最大值为___________ 。

已知:i.铍、铝元素化学性质相似;BeCl2熔融时能微弱电离。
ii.常温下:Ksp[Cu(OH)2]=2.2×10-20, Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13。
回答下列问题:
(1)滤液A的主要成分除NaOH外,还有
(2)滤液C中含NaCl、BeCl2和少量HCl,为得到较纯净的BeCl2溶液,选择下列实验操作最合理步骤的顺序是
①加入过量的NaOH:②加入过量的氨水;③加入适量的HCl;④过滤;⑤洗涤。
(3)反应Ⅱ中CuS的氧化产物为S单质,该反应的化学方程式为
(4)常温下,若滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,生成沉淀F是
您最近半年使用:0次
2019-03-27更新
|
1161次组卷
|
7卷引用:西藏日喀则市上海实验学校2020-2021学年高三下学期第二次模拟考试理综化学试题
西藏日喀则市上海实验学校2020-2021学年高三下学期第二次模拟考试理综化学试题【市级联考】安徽省合肥市2019届高三下学期第二次教学质量检测理科综合化学试题湖南省株洲市攸县第四中学2018-2019学年高二下学期第一次月考化学试题(已下线)四川省成都外国语学校2018-2019学年高二下学期期中考试化学试题四川师范大学附属中学2021届高三12月月考理综化学试题安徽省池州市第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)04 无机化工流程题(4) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
名校
9 . 元素铬(Cr)在自然界主要以+3价和+6价存在。
(1)+6价的Cr能引起细胞的突变而对人体不利,可用亚硫酸钠将其还原。离子反应方程式为:3SO32-+Cr2O72-+8H+===2Cr3++3SO42-+4H2O,该反应氧化剂和还原剂的物质的量之比为___________ 。
(2)工业上利用铬铁矿( FeO. Cr2O3)冶炼铬的工艺流程如图所示:
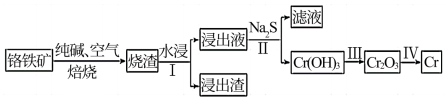
①为加快焙烧速率和提高原料的利用率,可采取的措施之一是___________ 。
②水浸Ⅰ要获得浸出液的操作是___________ 。
③浸出液的主要成分为Na2CrO4,加入Na2S反应后有Na2SO4生成,则操作Ⅱ发生反应的离子方程式为___________ 。
(3)常温下Cr(OH)3的溶度积Ksp=1×10-32,若要使Cr3+完全沉淀pH为___________ [c(Cr3+)降至10-5mol·L-1可认为完全沉淀]。
(4)以铬酸钠(Na2CrO4)为原料,用电化学法可制备重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2CrO42-+2H+=Cr2O72-+H2O)。
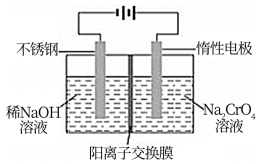
①阳极的电极反应式为___________ 。
②电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则生成重铬酸钠的物质的量为___________ mol。
(1)+6价的Cr能引起细胞的突变而对人体不利,可用亚硫酸钠将其还原。离子反应方程式为:3SO32-+Cr2O72-+8H+===2Cr3++3SO42-+4H2O,该反应氧化剂和还原剂的物质的量之比为
(2)工业上利用铬铁矿( FeO. Cr2O3)冶炼铬的工艺流程如图所示:

①为加快焙烧速率和提高原料的利用率,可采取的措施之一是
②水浸Ⅰ要获得浸出液的操作是
③浸出液的主要成分为Na2CrO4,加入Na2S反应后有Na2SO4生成,则操作Ⅱ发生反应的离子方程式为
(3)常温下Cr(OH)3的溶度积Ksp=1×10-32,若要使Cr3+完全沉淀pH为
(4)以铬酸钠(Na2CrO4)为原料,用电化学法可制备重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2CrO42-+2H+=Cr2O72-+H2O)。

①阳极的电极反应式为
②电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则生成重铬酸钠的物质的量为
您最近半年使用:0次
2019-02-05更新
|
736次组卷
|
3卷引用:西藏自治区昌都市第一高级中学2020届高三下学期第一次模拟考试理综化学试题
解题方法
10 . 2015年8月12日,天津滨海新区爆炸事故确认有氰化钠(NaCN)、亚硝酸钠等,氰化钠毒性很强,遇水、酸会产生有毒易燃氰化氢气体。氰化氢的沸点只有26摄氏度,因此相当容易挥发进入空气,这就大大增加了中毒的风险。同时氰化钠遇到亚硝酸钠会发生爆炸。回答下列问题
(1)写出氰化钠遇水产生氰化氢的离子方程式________________________________ 。
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理。氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式______________________________________________ 。
(3)氰化钠遇到亚硝酸钠能生成两种气体发生爆炸,写出化学反应方程式________________ 。
(4)爆炸残留在废水中的CN- 可以用 处理,拟定下列流程进行废水处理,
处理,拟定下列流程进行废水处理,
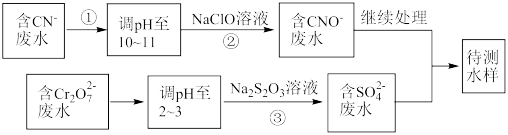
①上述处理废水流程中主要使用的方法是_______ ;
A.混凝法 B.中和法 C.沉淀法 D.氧化还原法
②过程②中反应后无气体放出,该反应的离子方程式为_______________________ ;
③步骤③中,每处理0.4 mol 时转移电子2.4 mol,该反应的离子方程式为
时转移电子2.4 mol,该反应的离子方程式为____________ ;
④处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4·7H2O将 还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅢCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol
还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅢCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol ,需加入amol FeSO4·7H2O,下列结论正确的是
,需加入amol FeSO4·7H2O,下列结论正确的是_______ 。
A.x=0.5,a=6 B.x=0.5,a=10 C.x=1.5,a=6 D.x=1.5,a=10
(1)写出氰化钠遇水产生氰化氢的离子方程式
(2)爆炸现场约700吨的氰化钠大约需要900吨的双氧水来处理。氰化钠与双氧水相遇后,会释放出氨气同时析出白色晶体,使得氰化钠的毒性大大降低,写出氰化钠与双氧水反应的化学方程式
(3)氰化钠遇到亚硝酸钠能生成两种气体发生爆炸,写出化学反应方程式
(4)爆炸残留在废水中的CN- 可以用
 处理,拟定下列流程进行废水处理,
处理,拟定下列流程进行废水处理,
①上述处理废水流程中主要使用的方法是
A.混凝法 B.中和法 C.沉淀法 D.氧化还原法
②过程②中反应后无气体放出,该反应的离子方程式为
③步骤③中,每处理0.4 mol
 时转移电子2.4 mol,该反应的离子方程式为
时转移电子2.4 mol,该反应的离子方程式为④处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4·7H2O将
 还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅢCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol
还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FexⅢCr(2-x)Ⅲ]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol ,需加入amol FeSO4·7H2O,下列结论正确的是
,需加入amol FeSO4·7H2O,下列结论正确的是A.x=0.5,a=6 B.x=0.5,a=10 C.x=1.5,a=6 D.x=1.5,a=10
您最近半年使用:0次
2016-12-09更新
|
238次组卷
|
2卷引用:2016届西藏山南第二高级中学高三下一模理综化学试卷



