解题方法
1 . 砷的化合物可用于半导体领域。一种从酸性高浓度含砷废水[砷主要以亚砷酸(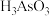 )形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
)形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
Ⅰ. ;
;
Ⅱ.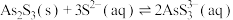 ;
;
Ⅲ.砷酸( )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 等还原;
等还原;
Ⅳ.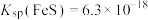 ,
, 。
。
回答下列问题;
(1)“沉砷”时,亚砷酸转化为 的化学方程式为
的化学方程式为_____________________________ 。
(2)“沉砷”时产生的废气可用______________ 溶液吸收处理(填化学式)。
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是_________ (填化学式);此时溶液中存在平衡: ,该反应的平衡常数K=
,该反应的平衡常数K=_____________ (保留2位小数)。
(4)向滤液Ⅱ中通入氧气进行“氧化脱硫”,反应的离子方程式为_____________________ 。
(5)“沉砷”过程中FeS不可用过量的 替换,原因是
替换,原因是 ______________________________ (从平衡移动的角度解释)。
(6)该流程最后一步用 “还原”砷酸,发生反应的化学方程式为
“还原”砷酸,发生反应的化学方程式为____________________ 。
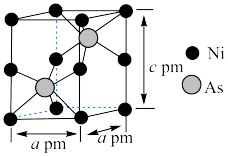
(7)某含砷化合物晶体的晶胞如图所示,As原子位于紧邻Ni原子构成的正三棱柱的体心。晶胞参数为a pm、a pm、c pm,则该晶体的密度为_______  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
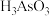 )形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下:
)形式存在,废水中还含有一定量的硫酸]中回收砷的工艺流程如下: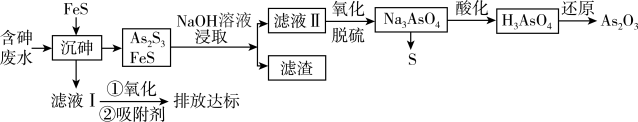
Ⅰ.
 ;
;Ⅱ.
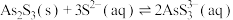 ;
;Ⅲ.砷酸(
 )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 等还原;
等还原;Ⅳ.
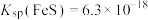 ,
, 。
。回答下列问题;
(1)“沉砷”时,亚砷酸转化为
 的化学方程式为
的化学方程式为(2)“沉砷”时产生的废气可用
(3)“NaOH溶液浸取”后,所得“滤渣”的主要成分是
 ,该反应的平衡常数K=
,该反应的平衡常数K=(4)向滤液Ⅱ中通入氧气进行“氧化脱硫”,反应的离子方程式为
(5)“沉砷”过程中FeS不可用过量的
 替换,原因是
替换,原因是 (6)该流程最后一步用
 “还原”砷酸,发生反应的化学方程式为
“还原”砷酸,发生反应的化学方程式为(7)某含砷化合物晶体的晶胞如图所示,As原子位于紧邻Ni原子构成的正三棱柱的体心。晶胞参数为a pm、a pm、c pm,则该晶体的密度为
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解题方法
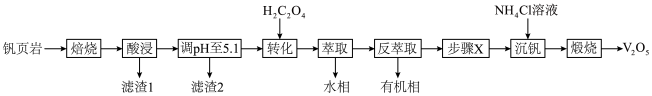
2 . V有“工业味精”之称。工业上提取钒的工艺有多种,一种从钒页岩(一种主要含Si、Fe、Al、V元素的矿石)中提取V的工艺流程如下:
①“酸浸”时有VO 生成;
生成;
② 在有机溶剂中的溶解度大于水,“萃取”时离子的萃取顺序为
在有机溶剂中的溶解度大于水,“萃取”时离子的萃取顺序为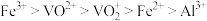 ;
;
③VO 和
和 可以相互转化。
可以相互转化。
回答下列问题:
(1)“焙烧”时可添加适量“盐对”NaCl- 与钒页岩形成混合物,这样做的目的是
与钒页岩形成混合物,这样做的目的是____________________ 。
(2)“滤渣1”除掉的主要杂质元素是_______ (填元素符号)。
(3) 作用是将VO
作用是将VO 转化为
转化为 ,转化的目的是
,转化的目的是_____________ ,发生的离子反应方程式为_____________________ 。
(4)①“沉钒”时,生成 沉淀,“步骤X”应该加入
沉淀,“步骤X”应该加入________ (填“氧化剂”或“还原剂”),写出“沉钒”时的离子反应方程式_______________________ 。
②以“沉钒率”( 沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高于80℃时沉钒率下降的原因是
沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高于80℃时沉钒率下降的原因是_______________ 。 可以溶解在NaOH溶液中,得到
可以溶解在NaOH溶液中,得到 ,
, 在不同的pH下可以得到不同聚合度的多钒酸盐,其阴离子呈如图所示的无限链状结构,其中一种酸式钒酸根离子可以表示为
在不同的pH下可以得到不同聚合度的多钒酸盐,其阴离子呈如图所示的无限链状结构,其中一种酸式钒酸根离子可以表示为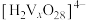 ,其中
,其中
________ 。 的立方晶胞如图所示,则在晶胞中,黑球代表的是
的立方晶胞如图所示,则在晶胞中,黑球代表的是_____ 原子。
①“酸浸”时有VO
 生成;
生成;②
 在有机溶剂中的溶解度大于水,“萃取”时离子的萃取顺序为
在有机溶剂中的溶解度大于水,“萃取”时离子的萃取顺序为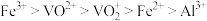 ;
;③VO
 和
和 可以相互转化。
可以相互转化。回答下列问题:
(1)“焙烧”时可添加适量“盐对”NaCl-
 与钒页岩形成混合物,这样做的目的是
与钒页岩形成混合物,这样做的目的是(2)“滤渣1”除掉的主要杂质元素是
(3)
 作用是将VO
作用是将VO 转化为
转化为 ,转化的目的是
,转化的目的是(4)①“沉钒”时,生成
 沉淀,“步骤X”应该加入
沉淀,“步骤X”应该加入②以“沉钒率”(
 沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高于80℃时沉钒率下降的原因是
沉淀中V的质量和钒页岩中钒的质量之比)表示钒的回收率如图所示,温度高于80℃时沉钒率下降的原因是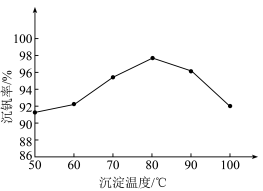
 可以溶解在NaOH溶液中,得到
可以溶解在NaOH溶液中,得到 ,
, 在不同的pH下可以得到不同聚合度的多钒酸盐,其阴离子呈如图所示的无限链状结构,其中一种酸式钒酸根离子可以表示为
在不同的pH下可以得到不同聚合度的多钒酸盐,其阴离子呈如图所示的无限链状结构,其中一种酸式钒酸根离子可以表示为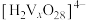 ,其中
,其中
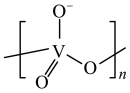
 的立方晶胞如图所示,则在晶胞中,黑球代表的是
的立方晶胞如图所示,则在晶胞中,黑球代表的是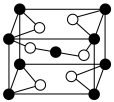
您最近一年使用:0次
解题方法
3 . GaN是制造微电子器件,光电子器件的新型半导体材料。综合利用炼锌矿渣{主要含铁酸镓[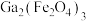 ]、铁酸锌(
]、铁酸锌( ),还含少量Fe及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
),还含少量Fe及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。 在酸性条件下不稳定,易转化为
在酸性条件下不稳定,易转化为 。
。
②常温下,“浸出液”中的金属离子对应的氢氧化物的溶度积常数如下表,离子浓度小于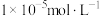 时可视为沉淀完全。
时可视为沉淀完全。
③ ,
, 。
。
回答下列问题:
(1)写出两条加快“浸出”速率的措施:_______ 。
(2) 中铁元素的化合价为
中铁元素的化合价为___ , 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为_______ 。
(3)“调pH”时需调节溶液pH的最小值为_______ 。
(4)“滤液1”中主要含有的金属阳离子为_______ ,检验“滤液1”中是否含有 的试剂为
的试剂为_______ (填名称)。
(5)“转化2”加入铁粉时主要发生反应的离子方程式为_______ 。
(6)“电解”反萃取液(溶质为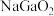 )制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为
)制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为_______ (填化学式)。
(7)闪锌矿型的GaN晶胞结构如图所示,设 为阿伏加德罗常数的值,晶胞参数为a nm,以晶胞参数为单位长度建立原子坐标系,1号原子的坐标为
为阿伏加德罗常数的值,晶胞参数为a nm,以晶胞参数为单位长度建立原子坐标系,1号原子的坐标为 。
。_______ 。
②闪锌矿型的GaN晶体密度为_______  。
。
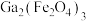 ]、铁酸锌(
]、铁酸锌( ),还含少量Fe及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
),还含少量Fe及一些难溶于酸的物质}获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如图。
 在酸性条件下不稳定,易转化为
在酸性条件下不稳定,易转化为 。
。②常温下,“浸出液”中的金属离子对应的氢氧化物的溶度积常数如下表,离子浓度小于
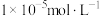 时可视为沉淀完全。
时可视为沉淀完全。| 氢氧化物 |  |  |  |  |
 |  |  | 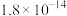 | 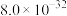 |
 ,
, 。
。回答下列问题:
(1)写出两条加快“浸出”速率的措施:
(2)
 中铁元素的化合价为
中铁元素的化合价为 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为(3)“调pH”时需调节溶液pH的最小值为
(4)“滤液1”中主要含有的金属阳离子为
 的试剂为
的试剂为(5)“转化2”加入铁粉时主要发生反应的离子方程式为
(6)“电解”反萃取液(溶质为
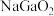 )制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为
)制粗镓后的电解废液经处理后可循环使用,电解废液的主要溶质为(7)闪锌矿型的GaN晶胞结构如图所示,设
 为阿伏加德罗常数的值,晶胞参数为a nm,以晶胞参数为单位长度建立原子坐标系,1号原子的坐标为
为阿伏加德罗常数的值,晶胞参数为a nm,以晶胞参数为单位长度建立原子坐标系,1号原子的坐标为 。
。
②闪锌矿型的GaN晶体密度为
 。
。
您最近一年使用:0次
解题方法
4 . 在生活中亚硝酸钠 应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
②酸性高锰酸钾溶液可将 氧化成
氧化成 。
。
回答下列问题:
Ⅰ. 的制备:
的制备:
(1)装置A中的仪器名称分别是______ ,仪器按气流方向连接顺序为b→______ 。
(2)反应开始前打开止水夹a,通入过量氮气的目的是______ ;反应结束后打开止水夹a,再通入过量氮气的目的是______ 。
(3)装置D的作用是______ 。
(4)判断 已被NO反应完全的现象是
已被NO反应完全的现象是______ 。
Ⅱ.
(5)写出实验室制氨气的化学方程式______ 。
Ⅲ.测定的纯度(假设杂质不与反应):
(6)准确称取反应后的固体3.000g于烧杯中,加入蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,滴入 的酸性
的酸性 溶液至恰好完全反应,用去16mL的酸性
溶液至恰好完全反应,用去16mL的酸性 溶液。固体中
溶液。固体中 的纯度为
的纯度为______ %。
 应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知
应用十分广泛,它是一种白色固体,外观与NaCl极其相似;少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长。某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)。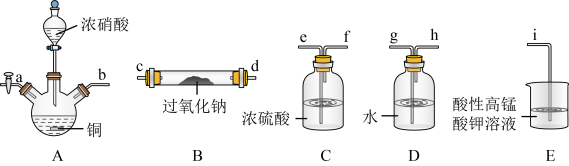
②酸性高锰酸钾溶液可将
 氧化成
氧化成 。
。回答下列问题:
Ⅰ.
 的制备:
的制备:(1)装置A中的仪器名称分别是
(2)反应开始前打开止水夹a,通入过量氮气的目的是
(3)装置D的作用是
(4)判断
 已被NO反应完全的现象是
已被NO反应完全的现象是Ⅱ.
(5)写出实验室制氨气的化学方程式
Ⅲ.测定的纯度(假设杂质不与反应):
(6)准确称取反应后的固体3.000g于烧杯中,加入蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,滴入
 的酸性
的酸性 溶液至恰好完全反应,用去16mL的酸性
溶液至恰好完全反应,用去16mL的酸性 溶液。固体中
溶液。固体中 的纯度为
的纯度为
您最近一年使用:0次
名校
解题方法
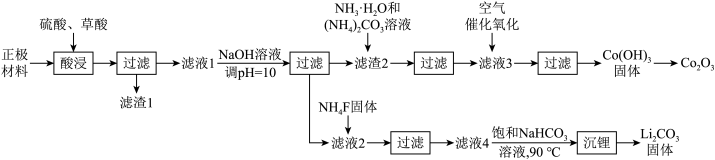
5 . 某化工厂利用废旧锂离子电池正极材料(含有LiCoO2以及少量Ca、Mg、Fe、Al等)制备Co2O3和Li2CO3.工艺流程如下: 如下表:
如下表:
②常温时, 的溶度积
的溶度积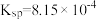 ,该数值随温度升高而减小。
,该数值随温度升高而减小。
(1)LiCoO2中Co元素的化合价为___________ ;基态Co原子的价层电子表示式为___________ 。
(2)“酸浸”时发生反应: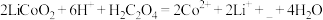 ,补充完整上述离子方程式
,补充完整上述离子方程式___________ 。
(3)已知滤渣2中含有 ,则常温下滤液2中
,则常温下滤液2中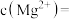
___________ mol/L。
(4)滤液3中含金属元素的离子主要是 ,通入空气发生催化氧化反应的离子方程式为
,通入空气发生催化氧化反应的离子方程式为___________ 。
(5)沉锂操作过程中的存在反应: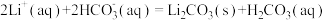 ,该操作中需将温度升高到90℃,原因是
,该操作中需将温度升高到90℃,原因是___________ 。
(6)由 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。 在晶胞中的位置为
在晶胞中的位置为___________ ;
②设阿伏加德罗常数的值为 。晶胞
。晶胞 的密度为b
的密度为b ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为___________ pm。
 如下表:
如下表:| 物质 |  |  |  |  |
 | 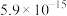 |  | 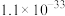 |  |
 的溶度积
的溶度积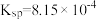 ,该数值随温度升高而减小。
,该数值随温度升高而减小。(1)LiCoO2中Co元素的化合价为
(2)“酸浸”时发生反应:
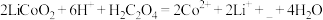 ,补充完整上述离子方程式
,补充完整上述离子方程式(3)已知滤渣2中含有
 ,则常温下滤液2中
,则常温下滤液2中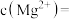
(4)滤液3中含金属元素的离子主要是
 ,通入空气发生催化氧化反应的离子方程式为
,通入空气发生催化氧化反应的离子方程式为(5)沉锂操作过程中的存在反应:
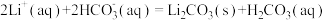 ,该操作中需将温度升高到90℃,原因是
,该操作中需将温度升高到90℃,原因是(6)由
 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。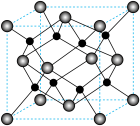
 在晶胞中的位置为
在晶胞中的位置为②设阿伏加德罗常数的值为
 。晶胞
。晶胞 的密度为b
的密度为b ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为
您最近一年使用:0次
解题方法
6 . 某制酸工厂产生的废酸液主要成分为HF、 、
、 、
、 、
、 ,一种处理工艺如下:
,一种处理工艺如下: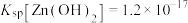
回答下列问题:
(1)基态As原子的价层电子排布图为__________________ ,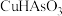 中As的化合价为
中As的化合价为_________ 。
(2)原废水中含有的 浓度为52.0
浓度为52.0 ,则
,则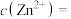
_____  ,常温下,有B离子的去除量、“调pH”为6.0后,
,常温下,有B离子的去除量、“调pH”为6.0后, 的去除率为
的去除率为_______ 。(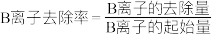 )
)
(3)强碱(AOH)的化学式为_____________ 。
(4)写出“还原”过程中 发生反应的化学方程式
发生反应的化学方程式_______________ 。
(5)产品结构分析。晶体W的晶胞结构如图所示:__________ 。
②W的化学式为_____________ 。
(6)产品纯度分析。称取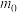 g
g  样品,用碱溶解,加入淀粉作指示剂,用浓度为
样品,用碱溶解,加入淀粉作指示剂,用浓度为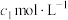 的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为
的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为 mL,则制得的产品纯度为
mL,则制得的产品纯度为___________ 。(用含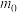 、
、 、
、 的代数式表示)
的代数式表示)
 、
、 、
、 、
、 ,一种处理工艺如下:
,一种处理工艺如下: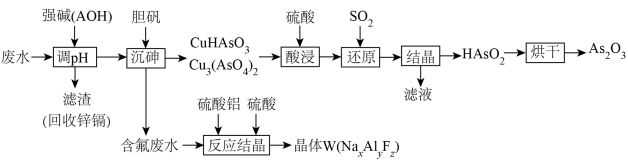
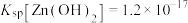
回答下列问题:
(1)基态As原子的价层电子排布图为
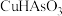 中As的化合价为
中As的化合价为(2)原废水中含有的
 浓度为52.0
浓度为52.0 ,则
,则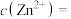
 ,常温下,有B离子的去除量、“调pH”为6.0后,
,常温下,有B离子的去除量、“调pH”为6.0后, 的去除率为
的去除率为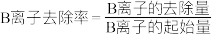 )
)(3)强碱(AOH)的化学式为
(4)写出“还原”过程中
 发生反应的化学方程式
发生反应的化学方程式(5)产品结构分析。晶体W的晶胞结构如图所示:

②W的化学式为
(6)产品纯度分析。称取
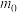 g
g  样品,用碱溶解,加入淀粉作指示剂,用浓度为
样品,用碱溶解,加入淀粉作指示剂,用浓度为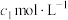 的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为
的碘标准溶液滴定As(Ⅲ)至As(Ⅴ),消耗体积为 mL,则制得的产品纯度为
mL,则制得的产品纯度为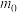 、
、 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
名校
解题方法
7 . 钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是V2O3、V2O4,含有的杂质有SiO2、FeS2及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
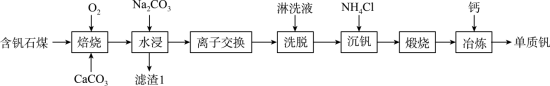
已知:①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
②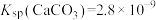 ,
,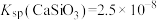 ,
,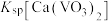 远大于
远大于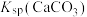 。
。
回答下列问题:
(1)基态Fe3+的价电子排布式为___________ 。
(2)为了提高“焙烧”效率,可采取的措施有___________ 、___________ 。
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)3,写出V2O4转化为Ca(VO3)3的化学方程式:___________ 。
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有___________ ;“水浸”加入过量Na2CO3不能使CaSiO3完全转化为CaCO3,原因是___________ 。(列式计算平衡常数分析该反应进行的趋势,一般认为,K>105时反应进行较完全,K<10-5时反应难以进行)
(5)“离子交换”与“洗脱”可表示为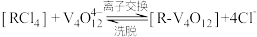 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂,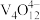 为VO
为VO 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用___________ 。
(6)“沉钒”过程析出NH4VO3晶体,需要加入过量NH4Cl,目的是___________ 。
(7)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是___________(填字母)。

已知:①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
| 金属离子 | Fe3+ | Mg2+ | Al3+ | Mn2+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 10.1 |
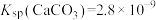 ,
,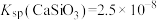 ,
,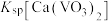 远大于
远大于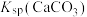 。
。回答下列问题:
(1)基态Fe3+的价电子排布式为
(2)为了提高“焙烧”效率,可采取的措施有
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)3,写出V2O4转化为Ca(VO3)3的化学方程式:
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有
(5)“离子交换”与“洗脱”可表示为
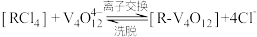 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂,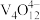 为VO
为VO 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用(6)“沉钒”过程析出NH4VO3晶体,需要加入过量NH4Cl,目的是
(7)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是___________(填字母)。
| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
名校
解题方法
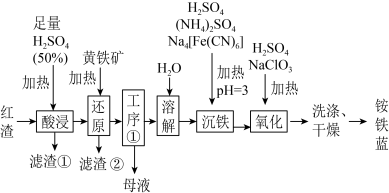
8 . 以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料生产制备铵铁蓝Fe(NH4)[Fe(CN)6]颜料的工艺流程如图:_______ (填化学式),滤渣①的主要成分是_______ (填化学式)。
(2)黄铁矿研细的目的是_______ 。
(3)工序①经过_______ 、过滤、洗涤得到一种含7个结晶水的晶体,该晶体为_______ (填化学式)。
(4)沉铁工序中生成一种白色沉淀为Fe(NH4)2[Fe(CN)6]。
①该物质的阴离子是由Fe2+和CN-结合形成的,CN-的电子式与氮气的电子式相似,请写出CN-的电子式:_______ 。
②该物质在酸性条件下加入NaClO3溶液,充分反应得到铵铁蓝,试补全下列离子方程式:_______ 。6Fe(NH4)2[Fe(CN)6]+ClO +_______=6FeNH4[Fe(CN)6]+ _______+_______NH
+_______=6FeNH4[Fe(CN)6]+ _______+_______NH +3H2O。
+3H2O。
(2)黄铁矿研细的目的是
(3)工序①经过
(4)沉铁工序中生成一种白色沉淀为Fe(NH4)2[Fe(CN)6]。
①该物质的阴离子是由Fe2+和CN-结合形成的,CN-的电子式与氮气的电子式相似,请写出CN-的电子式:
②该物质在酸性条件下加入NaClO3溶液,充分反应得到铵铁蓝,试补全下列离子方程式:
 +_______=6FeNH4[Fe(CN)6]+ _______+_______NH
+_______=6FeNH4[Fe(CN)6]+ _______+_______NH +3H2O。
+3H2O。
您最近一年使用:0次
2024-03-01更新
|
86次组卷
|
2卷引用:广东省两阳中学2023-2024学年高一下学期第一次月考化学试题
解题方法
9 . 镓( )是重要的稀有金属之一,主要应用于半导体行业。一种从砷化镓污泥(主要成分为
)是重要的稀有金属之一,主要应用于半导体行业。一种从砷化镓污泥(主要成分为 )中回收镓的工艺流程如图所示:
)中回收镓的工艺流程如图所示:
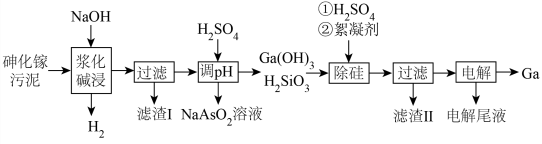
已知:Ⅰ. 是两性氢氧化物,既能溶于强酸又能溶于强碱;
是两性氢氧化物,既能溶于强酸又能溶于强碱;
Ⅱ. 为灰白色固体,易溶于水,具有还原性。
为灰白色固体,易溶于水,具有还原性。
回答下列问题:
(1)“浆化碱浸”过程中 反应的离子方程式为
反应的离子方程式为________ ;“滤渣Ⅰ”的成分为______ (填化学式)。
(2)中和“调 ”沉镓和硅的过程中,保持
”沉镓和硅的过程中,保持 约为6,若
约为6,若 过低镓的回收率将降低,其原因是
过低镓的回收率将降低,其原因是_______ 。
(3)“除硅”时,镓和硅在溶液中的含量如表所示,由表可知,“除硅”的 调节至
调节至______ 范围内,沉淀效果最好;此过程中,加入絮凝剂的目的是_______ 。
(4) 溶液经
溶液经_________ 、______ 、抽滤、洗涤、干燥得 晶体。
晶体。
(5)用惰性电极电解得到电解尾液和 ,电解尾液可在
,电解尾液可在______ (填操作单元名称)过程中循环使用,提高经济效益。
(6) 可生成
可生成 氮化镓等半导体材料,
氮化镓等半导体材料, 氮化镓晶胞结构如图,黑球代表
氮化镓晶胞结构如图,黑球代表 ,白球代表
,白球代表 ,晶胞参数为
,晶胞参数为 。
。
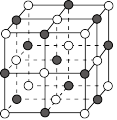
① 氮化镓晶体中每个
氮化镓晶体中每个 原子周围最近的
原子周围最近的 原子的个数为
原子的个数为_____ 。
②距离最近的两个 原子之间的距离为
原子之间的距离为_______  (用含
(用含 的代数式表示)。
的代数式表示)。
 )是重要的稀有金属之一,主要应用于半导体行业。一种从砷化镓污泥(主要成分为
)是重要的稀有金属之一,主要应用于半导体行业。一种从砷化镓污泥(主要成分为 )中回收镓的工艺流程如图所示:
)中回收镓的工艺流程如图所示:
已知:Ⅰ.
 是两性氢氧化物,既能溶于强酸又能溶于强碱;
是两性氢氧化物,既能溶于强酸又能溶于强碱;Ⅱ.
 为灰白色固体,易溶于水,具有还原性。
为灰白色固体,易溶于水,具有还原性。回答下列问题:
(1)“浆化碱浸”过程中
 反应的离子方程式为
反应的离子方程式为(2)中和“调
 ”沉镓和硅的过程中,保持
”沉镓和硅的过程中,保持 约为6,若
约为6,若 过低镓的回收率将降低,其原因是
过低镓的回收率将降低,其原因是(3)“除硅”时,镓和硅在溶液中的含量如表所示,由表可知,“除硅”的
 调节至
调节至 |  |  |
| 0.0 | 2500 | 1345 |
| 0.5 | 2456 | 1267 |
| 1.0 | 2438 | 81 |
| 1.5 | 2420 | 103 |
| 2.0 | 2200 | 804 |
| 2.5 | 1879 | 952 |
(4)
 溶液经
溶液经 晶体。
晶体。(5)用惰性电极电解得到电解尾液和
 ,电解尾液可在
,电解尾液可在(6)
 可生成
可生成 氮化镓等半导体材料,
氮化镓等半导体材料, 氮化镓晶胞结构如图,黑球代表
氮化镓晶胞结构如图,黑球代表 ,白球代表
,白球代表 ,晶胞参数为
,晶胞参数为 。
。
①
 氮化镓晶体中每个
氮化镓晶体中每个 原子周围最近的
原子周围最近的 原子的个数为
原子的个数为②距离最近的两个
 原子之间的距离为
原子之间的距离为 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解题方法
10 . 由软锰矿(主要成分为MnO2,含有少量CaO、MgO)制备MnO2的工艺流程如下:
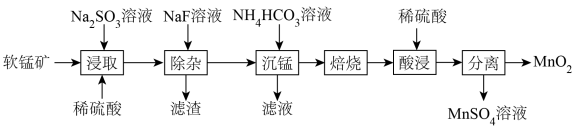
已知:“沉锰”所得MnCO3在空气中“焙烧”时转化为MnO2、Mn2O3、MnO的混合物。
回答下列问题:
(1)基态Mn的价电子排布式为_______ 。
(2)加快“浸取”速率可采取的措施为_______ (答出一种方法即可);“滤渣”的主要成分为_______ 。
(3)“浸取”步骤中发生的氧化还原反应的化学方程式为_______ 。
(4)可用惰性电极电解MnSO4溶液的方法制取MnO2,写出阳极的电极反应式:_______ 。
(5)① 、
、 两种离子的中心原子杂化方式分别为
两种离子的中心原子杂化方式分别为_______ 、_______ 。
②MgO的晶体结构与MnO的晶体结构相似,但MgO熔点高于MnO的熔点,其原因是_______ 。
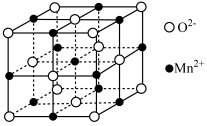
③MnO晶胞结构如图所示,平均每个晶胞中 组成的正四面体空隙有
组成的正四面体空隙有_______ 个,2个 之间的最近距离为acm,则MnO晶体的密度为
之间的最近距离为acm,则MnO晶体的密度为 =
=_______ g·cm-3。

已知:“沉锰”所得MnCO3在空气中“焙烧”时转化为MnO2、Mn2O3、MnO的混合物。
回答下列问题:
(1)基态Mn的价电子排布式为
(2)加快“浸取”速率可采取的措施为
(3)“浸取”步骤中发生的氧化还原反应的化学方程式为
(4)可用惰性电极电解MnSO4溶液的方法制取MnO2,写出阳极的电极反应式:
(5)①
 、
、 两种离子的中心原子杂化方式分别为
两种离子的中心原子杂化方式分别为②MgO的晶体结构与MnO的晶体结构相似,但MgO熔点高于MnO的熔点,其原因是
③MnO晶胞结构如图所示,平均每个晶胞中
 组成的正四面体空隙有
组成的正四面体空隙有 之间的最近距离为acm,则MnO晶体的密度为
之间的最近距离为acm,则MnO晶体的密度为 =
=
您最近一年使用:0次
2023-12-08更新
|
292次组卷
|
2卷引用:广东省佛山市2023-2024学年高三上学期12月月考化学试题



