解题方法
1 . 尿素还原法合成溴化锂,设备简单、产品质量好、无有毒气体排放、生产成本低。下图是制备无水溴化锂的工艺路线:
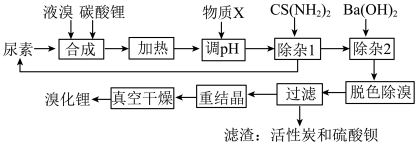
回答下列问题:
(1)Br位于周期表第________ 周期________ 族。
(2)常用焰色试验鉴别碳酸锂,火焰呈现________ 色。
(3)在溶解槽中,边搅拌边分次少量地将细粉末状的碳酸锂溶解于冷的溴水中至饱和为止,选用“冷”的溴水溶解碳酸锂的主要原因________ 。
(4)合成溴化锂的主要化学方程式________ 。
(5)合成时加入液溴会使pH降低,实际生产时需维持pH为4-5,为调节pH为4-5,从生产实际出发物质X最佳为________ 。
(6)加热体系的温度超过80℃会发生副反应:
3Br2+3H2O=5HBr+HBrO3
3HBrO=2HBr+HBrO3
Li2CO3+2HBrO3=2LiBrO3+H2O+CO2↑
还原溴酸锂需要选用硫脲,“除杂1”所发生的化学方程式是________ 。
(7)重结晶的操作为________ 。

温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
碳酸锂溶解度(g) | 1.51 | 1.43 | 1.33 | 1.26 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
(1)Br位于周期表第
(2)常用焰色试验鉴别碳酸锂,火焰呈现
(3)在溶解槽中,边搅拌边分次少量地将细粉末状的碳酸锂溶解于冷的溴水中至饱和为止,选用“冷”的溴水溶解碳酸锂的主要原因
(4)合成溴化锂的主要化学方程式
(5)合成时加入液溴会使pH降低,实际生产时需维持pH为4-5,为调节pH为4-5,从生产实际出发物质X最佳为
(6)加热体系的温度超过80℃会发生副反应:
3Br2+3H2O=5HBr+HBrO3
3HBrO=2HBr+HBrO3
Li2CO3+2HBrO3=2LiBrO3+H2O+CO2↑
还原溴酸锂需要选用硫脲,“除杂1”所发生的化学方程式是
(7)重结晶的操作为
您最近一年使用:0次
2024-04-02更新
|
341次组卷
|
2卷引用:湖北省2024届高三十一校第二次联考化学试题
解题方法
2 . 草酸钴主要用作制氧化钴的原料,也可用于制取其他钴化合物。利用废料铝钴膜(含有LiCoO2、Al、Fe)制备草酸钴的工艺如下:
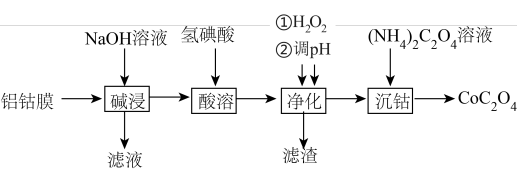
已知:①钴酸锂LiCoO2难溶于水,具有强氧化性。
②氢碘酸是强酸,酸溶后的溶液含有Li+、Fe2+、Co2+。
③金属离子沉淀开始和沉淀完全的pH:
(1)钴酸锂LiCoO2中钴元素的化合价为__________ 。
(2)“碱浸”的目的是溶解Al,写出“碱浸”过程发生反应的离子方程式__________ 。
(3)“酸溶”过程LiCoO2发生反应的离子方程式为__________ 。
(4)“净化”过程加入H2O2的目的是__________ 。
(5)调节pH的范围是__________ ,滤渣的成分是__________ (填化学式)。
(6)“沉钴”后过滤、洗涤,简述洗涤沉淀的方法__________ 。

已知:①钴酸锂LiCoO2难溶于水,具有强氧化性。
②氢碘酸是强酸,酸溶后的溶液含有Li+、Fe2+、Co2+。
③金属离子沉淀开始和沉淀完全的pH:
| Fe2+ | Fe3+ | Al3+ | Co2+ | |
| 沉淀开始的pH | 6.5 | 1.5 | 3.3 | 6.6 |
| 沉淀完全的pH | 9.7 | 3.2 | 4.7 | 9.2 |
(1)钴酸锂LiCoO2中钴元素的化合价为
(2)“碱浸”的目的是溶解Al,写出“碱浸”过程发生反应的离子方程式
(3)“酸溶”过程LiCoO2发生反应的离子方程式为
(4)“净化”过程加入H2O2的目的是
(5)调节pH的范围是
(6)“沉钴”后过滤、洗涤,简述洗涤沉淀的方法
您最近一年使用:0次
3 . 甲醇是一种基本的有机化工原料,用途十分广泛。应用CO2催化加氢规模化生产甲醇是综合利用CO2,实现“碳达峰”的有效措施之一、我国科学家研究发现二氧化碳电催化还原制甲醇的反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H,需通过以下两步实现:
I.CO2(g)+H2(g)⇌CO(g)+H2O(g) △H1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) △H2
反应过程中各物质的相对能量变化情况如图所示。
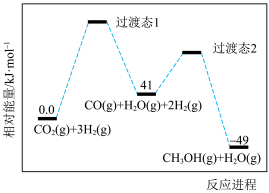
(1)
_______ ,稳定性:过渡态1_______ 过渡态2(填“大于”“小于”或“等于”)。
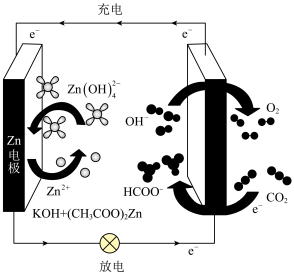
(2)基于催化剂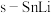 的CO2电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为
的CO2电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为_______ ,若电池工作t min,Zn电极的质量变化为 ,则理论上消耗CO2的物质的量为
,则理论上消耗CO2的物质的量为_______ 。
(3)+6价铬的化合物毒性较大,用甲醇酸性燃料电池电解处理酸性含铬废水(主要含有 )的原理示意图如下图所示。
)的原理示意图如下图所示。

①M极的电极反应式为_______ ,N极附近的pH_______ (填“变大”或“变小”或“不变”)。
②写出电解池中 转化为Cr3+的离子方程式
转化为Cr3+的离子方程式_______ 。
I.CO2(g)+H2(g)⇌CO(g)+H2O(g) △H1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) △H2
反应过程中各物质的相对能量变化情况如图所示。

(1)

(2)基于催化剂
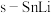 的CO2电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为
的CO2电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为 ,则理论上消耗CO2的物质的量为
,则理论上消耗CO2的物质的量为
(3)+6价铬的化合物毒性较大,用甲醇酸性燃料电池电解处理酸性含铬废水(主要含有
 )的原理示意图如下图所示。
)的原理示意图如下图所示。
①M极的电极反应式为
②写出电解池中
 转化为Cr3+的离子方程式
转化为Cr3+的离子方程式
您最近一年使用:0次
4 . 以银锰精矿(主要含Ag2S、MnS、FeS2)和氧化锰矿(主要含MnO2)为原料联合提取精银、Mn及MnO2的一种流程示意图如下。

已知:酸性条件下,MnO2的氧化性强于Fe3+。
(1)“浸锰”是在H2SO4溶液中使矿石中的锰元素浸出的过程,能同时去除FeS2,且有利于后续银的浸出,矿石中的银以Ag2S的形式残留于浸锰渣中。
①“浸锰”过程中,MnS发生反应的离子方程式是_______ 。
②在H2SO4溶液中,银锰精矿中的FeS2和氧化锰矿中的MnO2发生反应,则浸锰液中主要的金属阳离子有_______ 。
(2)“浸银”时,使用过量FeCl3、HCl、CaCl2的混合液作为浸出剂,将Ag2S中的银以 形式浸出。
形式浸出。
①将“浸银”反应的离子方程式补充完整:_______ 。
_______Fe3++Ag2S+_______⇌_______+_______[AgCl2]-+S
②浸出剂中H+的作用:_______ 。
(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,回答下列问题:
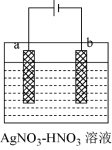
①_______ 极为“粗银电极”(填“a”或“b”)。
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为_______ ;当电路中通过0.025NA电子时,b极质量增加2.16g,则b极产生的气体在标况下的体积为_______ mL(保留三位有效数字)。

已知:酸性条件下,MnO2的氧化性强于Fe3+。
(1)“浸锰”是在H2SO4溶液中使矿石中的锰元素浸出的过程,能同时去除FeS2,且有利于后续银的浸出,矿石中的银以Ag2S的形式残留于浸锰渣中。
①“浸锰”过程中,MnS发生反应的离子方程式是
②在H2SO4溶液中,银锰精矿中的FeS2和氧化锰矿中的MnO2发生反应,则浸锰液中主要的金属阳离子有
(2)“浸银”时,使用过量FeCl3、HCl、CaCl2的混合液作为浸出剂,将Ag2S中的银以
 形式浸出。
形式浸出。①将“浸银”反应的离子方程式补充完整:
_______Fe3++Ag2S+_______⇌_______+_______[AgCl2]-+S
②浸出剂中H+的作用:
(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,回答下列问题:

①
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为
您最近一年使用:0次
5 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。
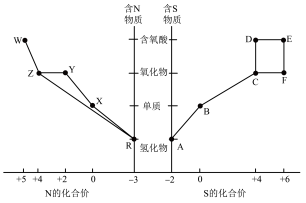
回答下列问题:
(1)写出物质R的电子式___________ 。
(2)下列有关图中所示含N、S物质的叙述,正确的是___________ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与 溶液反应,都是酸性氧化物
溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
(3)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是___________ 。
(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析, 中所含化学键类型为
中所含化学键类型为___________ ,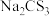 水溶液显
水溶液显___________ (填“酸性”、“碱性”或“中性”)。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: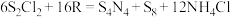 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有___________ ,该反应每生成 转移电子
转移电子___________ mol。

回答下列问题:
(1)写出物质R的电子式
(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与
 溶液反应,都是酸性氧化物
溶液反应,都是酸性氧化物e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
(3)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析,
 中所含化学键类型为
中所含化学键类型为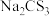 水溶液显
水溶液显(5)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: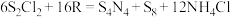 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有 转移电子
转移电子
您最近一年使用:0次
名校
解题方法
6 . 某同学欲探究H2O2的氧化还原性:
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,探究H2O2的氧化性可以选取的物质是:___________ (填序号)
①淀粉KI溶液(酸性) ②酸性KMnO4溶液 ③Cl2 ④HNO3溶液
任选一个你所选的物质进行实验,观察到___________ 现象,证明H2O2有氧化性,反应的离子方程式为___________ 。
(2)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。反应的离子方程式为___________ 。
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有___________ 性,能与H2O2反应产生MnO2
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
iii是ii和i的对照实验。
①X是___________ 。
②a是___________ 、b是___________ 。
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,探究H2O2的氧化性可以选取的物质是:
①淀粉KI溶液(酸性) ②酸性KMnO4溶液 ③Cl2 ④HNO3溶液
任选一个你所选的物质进行实验,观察到
(2)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。反应的离子方程式为
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
| 序号 | 实验 | 试剂 | 现象 |
| i | 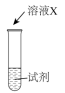 | a | 生成棕褐色固体,产生大量气泡 |
| ii | b | 有少量气泡 | |
| iii | H2O2溶液 | 有少量气泡 |
①X是
②a是
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
您最近一年使用:0次
名校
解题方法
7 . 氯碱工业是化工产业的重要基础,其装置示意图如下图。生产过程中产生的氯酸盐副产物需要处理。
已知:当 升高时,
升高时, 易歧化为
易歧化为 和
和 。
。
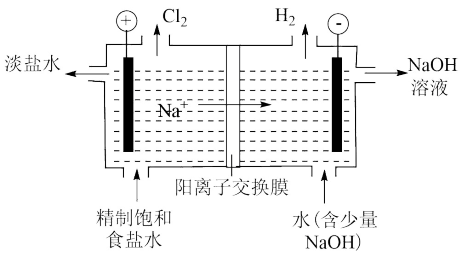
(1)电解饱和食盐水的阴极反应式为_____ 。
(2)下列关于 产生的说法中,合理的是
产生的说法中,合理的是_____ (填序号)。
a. 主要在阴极室产生
主要在阴极室产生
b. 在电极上放电,可能产生
在电极上放电,可能产生
c.阳离子交换膜破损导致 向阳极室迁移,可能产生
向阳极室迁移,可能产生
(3)测定副产物 含量的方法如下图。
含量的方法如下图。
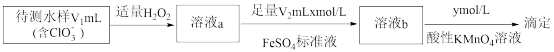
①加入 的目的是消耗水样中残留的
的目的是消耗水样中残留的 和
和 。若测定中未加入
。若测定中未加入 ,则水样中
,则水样中 的浓度将
的浓度将_____ (填“偏大”“偏小”或“不受影响”)。
②滴定测 含量消耗
含量消耗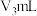 酸性
酸性 溶液,水样中
溶液,水样中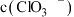 的计算式为
的计算式为_____ 。
(4)可用盐酸处理淡盐水中的 并回收
并回收
①反应的离子方程式为_____ 。
②处理 时,
时, 可能的作用是:
可能的作用是:
ⅰ.增大 ,使
,使 氧化性增强或
氧化性增强或 还原性增强;
还原性增强;
ⅱ.增大 ,
,_____ 。
③用如图装置验证ⅰ,请补全操作和现象:
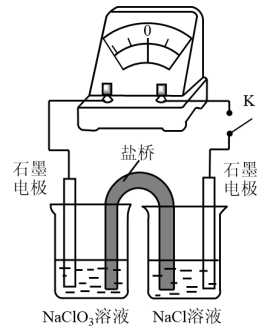
闭合 ,至指针读数稳定后
,至指针读数稳定后_____ 。
已知:当
 升高时,
升高时, 易歧化为
易歧化为 和
和 。
。
(1)电解饱和食盐水的阴极反应式为
(2)下列关于
 产生的说法中,合理的是
产生的说法中,合理的是a.
 主要在阴极室产生
主要在阴极室产生b.
 在电极上放电,可能产生
在电极上放电,可能产生
c.阳离子交换膜破损导致
 向阳极室迁移,可能产生
向阳极室迁移,可能产生
(3)测定副产物
 含量的方法如下图。
含量的方法如下图。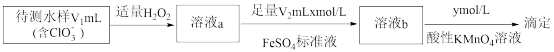
①加入
 的目的是消耗水样中残留的
的目的是消耗水样中残留的 和
和 。若测定中未加入
。若测定中未加入 ,则水样中
,则水样中 的浓度将
的浓度将②滴定测
 含量消耗
含量消耗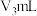 酸性
酸性 溶液,水样中
溶液,水样中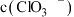 的计算式为
的计算式为(4)可用盐酸处理淡盐水中的
 并回收
并回收
①反应的离子方程式为
②处理
 时,
时, 可能的作用是:
可能的作用是:ⅰ.增大
 ,使
,使 氧化性增强或
氧化性增强或 还原性增强;
还原性增强;ⅱ.增大
 ,
,③用如图装置验证ⅰ,请补全操作和现象:

闭合
 ,至指针读数稳定后
,至指针读数稳定后
您最近一年使用:0次
名校
8 . 氯化钴( )在工业催化、涂料工业、干湿指示剂等领域具有广泛应用。
)在工业催化、涂料工业、干湿指示剂等领域具有广泛应用。
(1)某钴矿石的主要成分包括CoO、MnO、 和
和 。由该矿石制
。由该矿石制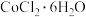 固体的方法如图(部分操作省略):
固体的方法如图(部分操作省略):

资料: 生成
生成 ,开始沉淀时
,开始沉淀时 ,完全沉淀时
,完全沉淀时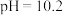 。
。
①上述矿石溶解过程中,能够加快化学反应速率的措施有_________ (写出一条即可)。
②CoO溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括 和
和________ 。
③调节溶液的pH至2.8时,得到的沉淀2可能是________ 。
④溶液2中含有 和
和 。
。
ⅰ.已知:常温时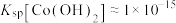 ,当
,当 时可认为
时可认为 完全沉淀。若向溶液2中加入碱溶液,常温下,当
完全沉淀。若向溶液2中加入碱溶液,常温下,当
_______ 时 完全沉淀。
完全沉淀。
由此可知,通过调节pH将 和
和 完全分离
完全分离_______ (填“可行”或“不可行”)。
ⅱ.溶液2中加入氨水和H2O2溶液,发生的反应为:________ (完成离子方程式)
___ ____
____ _____
_____ ____+____
____+____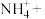 ____。
____。
(2)可用如下方法测定产品中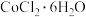 的质量分数(其他杂质不干扰测定):
的质量分数(其他杂质不干扰测定):
资料:ⅲ.Co2+与EDTA以物质的量比1:1反应,
取mg产品溶于水,向其中加入少量紫脲酸铵指示剂。再用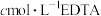 溶液滴定,消耗EDTA溶液的体积为VmL。产品中
溶液滴定,消耗EDTA溶液的体积为VmL。产品中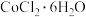 的质量分数为
的质量分数为________ (结果用m、v、c表示)。
 )在工业催化、涂料工业、干湿指示剂等领域具有广泛应用。
)在工业催化、涂料工业、干湿指示剂等领域具有广泛应用。(1)某钴矿石的主要成分包括CoO、MnO、
 和
和 。由该矿石制
。由该矿石制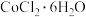 固体的方法如图(部分操作省略):
固体的方法如图(部分操作省略):
资料:
 生成
生成 ,开始沉淀时
,开始沉淀时 ,完全沉淀时
,完全沉淀时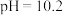 。
。①上述矿石溶解过程中,能够加快化学反应速率的措施有
②CoO溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括
 和
和③调节溶液的pH至2.8时,得到的沉淀2可能是
④溶液2中含有
 和
和 。
。ⅰ.已知:常温时
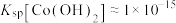 ,当
,当 时可认为
时可认为 完全沉淀。若向溶液2中加入碱溶液,常温下,当
完全沉淀。若向溶液2中加入碱溶液,常温下,当
 完全沉淀。
完全沉淀。由此可知,通过调节pH将
 和
和 完全分离
完全分离ⅱ.溶液2中加入氨水和H2O2溶液,发生的反应为:
___
 ____
____ _____
_____ ____+____
____+____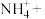 ____。
____。(2)可用如下方法测定产品中
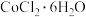 的质量分数(其他杂质不干扰测定):
的质量分数(其他杂质不干扰测定):资料:ⅲ.Co2+与EDTA以物质的量比1:1反应,

取mg产品溶于水,向其中加入少量紫脲酸铵指示剂。再用
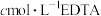 溶液滴定,消耗EDTA溶液的体积为VmL。产品中
溶液滴定,消耗EDTA溶液的体积为VmL。产品中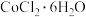 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
9 . 石油天然气开采和炼制过程中会产生大量含硫废水(其中S元素的主要化合价是-2价),对设备、环境等造成严重危害。
已知: 有剧毒;常温下溶解度为
有剧毒;常温下溶解度为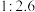 (体积)。
(体积)。
(1) 、
、 、
、 在水溶液中的物质的量分数随pH的分布曲线如图。
在水溶液中的物质的量分数随pH的分布曲线如图。

①当 时,含硫废水中最主要的含硫(-2价)微粒是
时,含硫废水中最主要的含硫(-2价)微粒是_________ 。
②通过图中数据可估算得 的
的______ (填“ ”或“
”或“ ”)。
”)。
(2)沉淀法处理含硫废水:
向 的含硫废水中加入适量
的含硫废水中加入适量 的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因:
的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因:_______ 。
(3)氧化还原法处理含硫废水:
向 的含硫废水中加入一定浓度的
的含硫废水中加入一定浓度的 溶液,加酸将溶液调为
溶液,加酸将溶液调为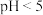 ,产生淡黄色沉淀。
,产生淡黄色沉淀。
①反应的离子方程式是________ 。
②不同pH时,硫化物去除率随时间的变化曲线如图。本工艺选择控制体系的 ,不选择
,不选择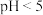 ,从环境保护的角度分析其主要原因:
,从环境保护的角度分析其主要原因:________ 。

(4)电浮选絮凝法处理含硫废水:
铝作阳极、石墨作阴极,以直流电电解含一定浓度 的
的 的含硫废水。阳极产生微小气泡,随后溶液中产生淡黄色浑浊,阳极附近生成的胶体吸附淡黄色浑浊。
的含硫废水。阳极产生微小气泡,随后溶液中产生淡黄色浑浊,阳极附近生成的胶体吸附淡黄色浑浊。
①用离子方程式表述产生淡黄色浑浊的可能原因:________ 。
②阴极产生的气泡把污水中的悬浮物(含阳极扩散的胶体)带到水面形成浮渣层,胶体的化学式:______ ,结合电极反应式解释浮渣层的形成过程:_______ 。
已知:
 有剧毒;常温下溶解度为
有剧毒;常温下溶解度为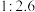 (体积)。
(体积)。(1)
 、
、 、
、 在水溶液中的物质的量分数随pH的分布曲线如图。
在水溶液中的物质的量分数随pH的分布曲线如图。
①当
 时,含硫废水中最主要的含硫(-2价)微粒是
时,含硫废水中最主要的含硫(-2价)微粒是②通过图中数据可估算得
 的
的 ”或“
”或“ ”)。
”)。(2)沉淀法处理含硫废水:
向
 的含硫废水中加入适量
的含硫废水中加入适量 的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因:
的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因:(3)氧化还原法处理含硫废水:
向
 的含硫废水中加入一定浓度的
的含硫废水中加入一定浓度的 溶液,加酸将溶液调为
溶液,加酸将溶液调为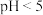 ,产生淡黄色沉淀。
,产生淡黄色沉淀。①反应的离子方程式是
②不同pH时,硫化物去除率随时间的变化曲线如图。本工艺选择控制体系的
 ,不选择
,不选择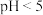 ,从环境保护的角度分析其主要原因:
,从环境保护的角度分析其主要原因:
(4)电浮选絮凝法处理含硫废水:
铝作阳极、石墨作阴极,以直流电电解含一定浓度
 的
的 的含硫废水。阳极产生微小气泡,随后溶液中产生淡黄色浑浊,阳极附近生成的胶体吸附淡黄色浑浊。
的含硫废水。阳极产生微小气泡,随后溶液中产生淡黄色浑浊,阳极附近生成的胶体吸附淡黄色浑浊。①用离子方程式表述产生淡黄色浑浊的可能原因:
②阴极产生的气泡把污水中的悬浮物(含阳极扩散的胶体)带到水面形成浮渣层,胶体的化学式:
您最近一年使用:0次
名校
解题方法
10 . 2019年诺贝尔化学奖颁给了日本吉野彰等三人,以表彰他们对锂离子电池研发的卓越贡献。工业中利用锂辉石(主要成分为 ,还含有
,还含有 、
、 、
、 等)制备钴酸锂(
等)制备钴酸锂( )的流程如图:
)的流程如图:

已知: ,
, ,
, 。
。
回答下列问题:
(1)锂辉石的主要成分为 ,其氧化物的形式为
,其氧化物的形式为___________ 。
(2)为提高“酸化焙烧”效率,常采取的措施是___________ 。
(3)向“浸出液”中加入 ,其目的是除去“酸化焙烧”中过量的硫酸,控制
,其目的是除去“酸化焙烧”中过量的硫酸,控制 使
使 完全沉淀,则
完全沉淀,则 至少为
至少为___________ (保留1位小数,已知:完全沉淀后离子浓度低于 )
)
(4)“滤渣II”的主要化学成分为___________ 。
(5)“沉锂”过程中加入的沉淀剂为饱和的___________ 溶液(填化学式);该过程所获得的“母液”中仍含有大量的 ,可将其加入到“
,可将其加入到“___________ ”步骤中。
(6) 与
与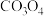 在敞口容器中高温下焙烧生成钴酸锂的化学方程式为
在敞口容器中高温下焙烧生成钴酸锂的化学方程式为___________ 。
 ,还含有
,还含有 、
、 、
、 等)制备钴酸锂(
等)制备钴酸锂( )的流程如图:
)的流程如图:
已知:
 ,
, ,
, 。
。回答下列问题:
(1)锂辉石的主要成分为
 ,其氧化物的形式为
,其氧化物的形式为(2)为提高“酸化焙烧”效率,常采取的措施是
(3)向“浸出液”中加入
 ,其目的是除去“酸化焙烧”中过量的硫酸,控制
,其目的是除去“酸化焙烧”中过量的硫酸,控制 使
使 完全沉淀,则
完全沉淀,则 至少为
至少为 )
)(4)“滤渣II”的主要化学成分为
(5)“沉锂”过程中加入的沉淀剂为饱和的
 ,可将其加入到“
,可将其加入到“(6)
 与
与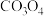 在敞口容器中高温下焙烧生成钴酸锂的化学方程式为
在敞口容器中高温下焙烧生成钴酸锂的化学方程式为
您最近一年使用:0次
2024-01-16更新
|
89次组卷
|
2卷引用:湖北省武汉市武钢三中2023-2024学年高二上学期12月月考化学试题



