1 . 由铁及其化合物可制得铁红(Fe2O3)、氧化铁、绿矾(FeSO4•7H2O)、高铁酸钾(K2FeO4)、铁黄(FeOOH)等物质。高铁酸钾是一种既能杀菌、消毒,又能絮凝净水的水处理剂,能与水反应生成氢氧化铁和氧气。铁黄可用作生产磁性材料、颜料的原料。工业制备K2FeO4的离子方程式为Fe(OH)3+ClO-+OH-→FeO +Cl-+H2O(未配平)。下列有关说法
+Cl-+H2O(未配平)。下列有关说法不正确 的是
 +Cl-+H2O(未配平)。下列有关说法
+Cl-+H2O(未配平)。下列有关说法| A.K2FeO4中Fe显+6价 |
B.ClO-的氧化性大于FeO |
| C.上述反应中氧化剂和还原剂的物质的量之比为3:2 |
| D.每1molK2FeO4与水反应,产生0.5molO2 |
您最近一年使用:0次
名校
2 . Cr2O 毒性较强,常用NaHSO3处理工业废水中的Cr2O
毒性较强,常用NaHSO3处理工业废水中的Cr2O ,反应的离子方程式为:H+ +Cr2O
,反应的离子方程式为:H+ +Cr2O +HSO
+HSO
 Cr3++SO
Cr3++SO +H2O(未配平),下列关于该反应的说法正确的是
+H2O(未配平),下列关于该反应的说法正确的是
 毒性较强,常用NaHSO3处理工业废水中的Cr2O
毒性较强,常用NaHSO3处理工业废水中的Cr2O ,反应的离子方程式为:H+ +Cr2O
,反应的离子方程式为:H+ +Cr2O +HSO
+HSO
 Cr3++SO
Cr3++SO +H2O(未配平),下列关于该反应的说法正确的是
+H2O(未配平),下列关于该反应的说法正确的是| A.氧化剂和还原剂的计量数之比为3:1 | B.Cr3+是氧化反应的产物 |
C. 发生还原反应 发生还原反应 | D.消耗5 molH+时转移6mol电子 |
您最近一年使用:0次
名校
3 . 利用工业废气NO生产 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中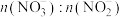 都为1∶1.下列说法错误的是
都为1∶1.下列说法错误的是
 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中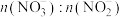 都为1∶1.下列说法错误的是
都为1∶1.下列说法错误的是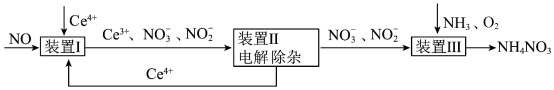
| A.装置江中若有5.6L(标准状况)NO参与反应,则转移1mol电子 |
B.装置Ⅰ中反应为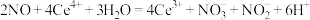 |
| C.装置Ⅲ中氧化剂和还原剂的物质的量之比为1∶2 |
D.装置Ⅲ中 和 和 的体积比3∶1时,可实现原子利用率最大化 的体积比3∶1时,可实现原子利用率最大化 |
您最近一年使用:0次
2024-04-10更新
|
101次组卷
|
2卷引用:山东省青岛第二中学2023-2024学年高一上学期第二次月考化学试卷
解题方法
4 . 某消毒液的主要成分为NaClO,还含有一定量的NaCl和NaOH。下列用来解释事实的离子方程式不合理的是
A.该消毒液可用NaOH溶液吸收 来制备: 来制备: |
B.HClO的酸性弱于 : :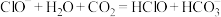 |
C.该消毒液与洁厕灵(主要成分为HCl)混用会产生有毒的 : : |
D.该消毒液加白醋会生成HClO,可增强漂白作用: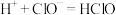 |
您最近一年使用:0次
解题方法
5 . 向铜屑、稀盐酸和铁盐的混合溶液中持续通入空气可制备氯化铜,其反应过程如图所示。下列说法不正确 的是
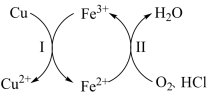

A.制备 的总反应为 的总反应为 |
B.反应Ⅰ中 作氧化剂 作氧化剂 |
C.反应Ⅱ中 作还原剂 作还原剂 |
D.还原性: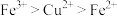 |
您最近一年使用:0次
6 . ClO2是可代替Cl2进行自来水消毒的新一代消毒剂。我国成功研制出制取ClO2的新方法,其反应的微观过程如图所示,下列有关该反应的叙述正确的是


| A.该反应属于置换反应 |
| B.该反应的化学方程式为Cl2+2NaClO2=2ClO2+2NaCl |
| C.NaClO2转化为ClO2的过程是还原反应 |
| D.Cl2既是氧化剂又是还原剂 |
您最近一年使用:0次
解题方法
7 . 利用烟气中的SO2可回收废水中的I-,实现碘单质的再生,其反应原理如图所示。下列说法正确的是
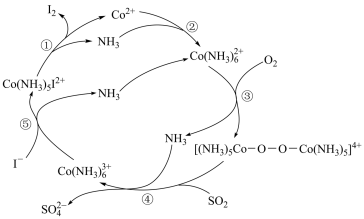

A.1mol SO 中含有电子的数目为48NA 中含有电子的数目为48NA |
| B.NH3溶于水能导电,NH3属于电解质 |
| C.反应①~⑤中均属于氧化还原反应 |
D.总反应离子方程式为: |
您最近一年使用:0次
8 . 已知在碱性溶液中可发生如下反应:2R(OH)3+3ClO﹣+4OH﹣=2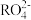 +3Cl﹣+5H2O。则
+3Cl﹣+5H2O。则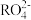 中R 的化合价是
中R 的化合价是
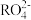 +3Cl﹣+5H2O。则
+3Cl﹣+5H2O。则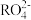 中R 的化合价是
中R 的化合价是| A.+3 | B.+4 | C.+6 | D.+5 |
您最近一年使用:0次
解题方法
9 . 锶(Sr)为第五周期IIA族元素,工业上常以天青石(主要成分为 ,含少量
,含少量 )为原料制备六水氯化锶(
)为原料制备六水氯化锶( ),生产流程如图所示(已知:“高温焙烧”时,
),生产流程如图所示(已知:“高温焙烧”时, 转化为SrS、BaS):
转化为SrS、BaS):

已知:25 ℃时, 的
的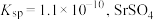 的
的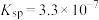 ;溶液中离子浓度小于或等于
;溶液中离子浓度小于或等于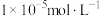 时,认为沉淀完全。
时,认为沉淀完全。
下列说法错误的是
 ,含少量
,含少量 )为原料制备六水氯化锶(
)为原料制备六水氯化锶( ),生产流程如图所示(已知:“高温焙烧”时,
),生产流程如图所示(已知:“高温焙烧”时, 转化为SrS、BaS):
转化为SrS、BaS):
已知:25 ℃时,
 的
的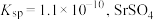 的
的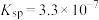 ;溶液中离子浓度小于或等于
;溶液中离子浓度小于或等于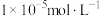 时,认为沉淀完全。
时,认为沉淀完全。下列说法错误的是
A.“高温焙烧”时 转化为SrS的化学方程式为 转化为SrS的化学方程式为 |
| B.“操作1”是蒸发浓缩、冷却结晶 |
C.为除去“溶液”中的 ,提高原料利用率,“滤液”中 ,提高原料利用率,“滤液”中 的浓度应小于 的浓度应小于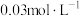 |
D.制取无水 时,一定要在无水氯化氢气流中加热 时,一定要在无水氯化氢气流中加热 至恒重 至恒重 |
您最近一年使用:0次
解题方法
10 . 乙醛是一种重要的工业原料,广泛应用于医药、农药、涂料、塑料、合成纤维、橡胶、树脂等领域。乙醛由乙烯在催化剂作用下直接氧化制得,乙烯氧化法制乙醛的原理如下图所示(部分相关离子未画出),下列说法正确的是


A. 在反应中是中间产物 在反应中是中间产物 |
B.乙烯催化氧化法制乙醛的化学方程式为 |
| C.转化过程中,Pd元素的化合价没有发生变化 |
| D.该转化过程中,有非极性键的断裂与极性键的形成 |
您最近一年使用:0次



