1 . 宏观辨识与微观探析是化学核心素养之一、下列物质性质与用途对应的离子方程式书写正确的是
A. 氧化海带灰酸性浸出液提取碘: 氧化海带灰酸性浸出液提取碘: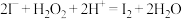 |
B. 与水反应用作潜水艇氧气来源: 与水反应用作潜水艇氧气来源: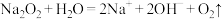 |
C.绿矾处理含 的酸性废水: 的酸性废水: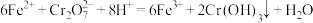 |
D.向 溶液中通入氨气可制备抗酸药 溶液中通入氨气可制备抗酸药 : :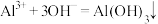 |
您最近一年使用:0次
名校
2 . 硫化氢的转化是资源利用和环境保护的重要研究课题。将 和空气的混合气体通入
和空气的混合气体通入 和
和 的混合溶液中回收S,反应历程如图。下列说法正确的是
的混合溶液中回收S,反应历程如图。下列说法正确的是
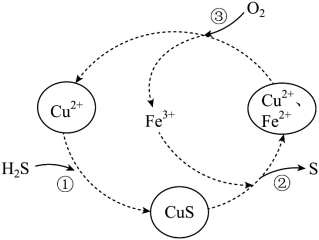
A.①反应的离子方程式为: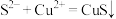 |
B.反应中, 、 、 可以循环利用 可以循环利用 |
C.由反应②③可知氧化性的强弱顺序: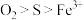 |
D.回收S的总反应为: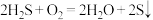 |
您最近一年使用:0次
名校
3 . 汽车剧烈碰撞时,安全气囊中发生反应:NaN3+KNO3→K2O+Na2O+N2↑(未配平)。对上述反应的描述错误的是
| A.NaN3是还原剂,KNO3是氧化剂 |
| B.该反应中只有1种元素的化合价发生变化 |
| C.配平后物质的化学计量数依次为10、2、1、5、16 |
| D.生成N2的个数与转移电子个数之比为4:5 |
您最近一年使用:0次
2024-03-22更新
|
105次组卷
|
2卷引用:山西省运城市康杰中学2023-2024学年高一下学期化学试题
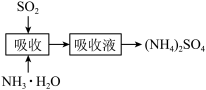
4 . 工业上常用氨水吸收SO2,实现尾气资源化利用。模拟工业过程如图所示。室温下,用0.1mol/L氨水溶液吸收SO2,若通入SO2所引起的溶液体积变化和NH3及H2O挥发可忽略,溶液中含硫物种的浓度 。H2SO3的电离平衡常数分别为
。H2SO3的电离平衡常数分别为 ,
, 。下列说法一定正确的是
。下列说法一定正确的是
 。H2SO3的电离平衡常数分别为
。H2SO3的电离平衡常数分别为 ,
, 。下列说法一定正确的是
。下列说法一定正确的是
A.吸收液pH=7时,溶液中 |
B.吸收液pH=5时测得 ,溶液中 ,溶液中 |
C.向吸收液中滴加 溶液生成白色沉淀,上层清液中 溶液生成白色沉淀,上层清液中 |
D.向吸收液中滴加 溶液,可能发生反应的离子方程式为: 溶液,可能发生反应的离子方程式为: |
您最近一年使用:0次
5 . 草酸(H2C2O4)是一种二元弱酸。实验室配制了0.0100mol•L﹣1Na2C2O4标准溶液,现对25℃时该溶液的性质进行探究,下列所得结论正确的是
A.测得0.0100mol•L﹣1Na2C2O4溶液pH为8.6,此时溶液中存在:c(Na+)>c( )>c( )>c( )>c(OH-) )>c(OH-) |
B.向该溶液中滴加稀盐酸至溶液pH=7,此时溶液中存在:c(Na+)=c( )+2c( )+2c( ) ) |
C.向该溶液中加入足量稀硫酸酸化后,再滴加KMnO4溶液,发生反应的离子方程式为 +4 +4 +14H+=2CO2↑+4Mn2++7H2O +14H+=2CO2↑+4Mn2++7H2O |
D.已知CaC2O4难溶于水,存在溶解平衡,25℃时饱和CaC2O4溶液的浓度为5×10﹣5mol•L﹣1,向该溶液中加入等体积0.0200mol•L﹣1CaCl2溶液,所得上层清液中c( )<5.00×10﹣5mol•L﹣1 )<5.00×10﹣5mol•L﹣1 |
您最近一年使用:0次
名校
解题方法
6 . 一种由湿法炼铜的低铜萃取余液(含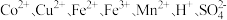 )回收金属的工艺流程如下:
)回收金属的工艺流程如下:
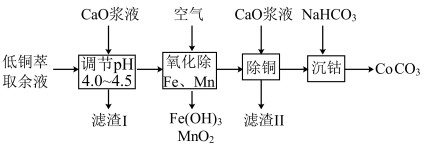
室温下,溶液中金属离子开始沉淀和完全沉淀的 如表所示。下列说法正确的是
如表所示。下列说法正确的是
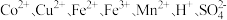 )回收金属的工艺流程如下:
)回收金属的工艺流程如下:
室温下,溶液中金属离子开始沉淀和完全沉淀的
 如表所示。下列说法正确的是
如表所示。下列说法正确的是| 金属离子 | 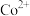 |  | 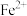 | 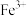 | 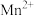 |
开始沉淀时的 | 7.8 | 5.5 | 5.8 | 1.8 | 8.3 |
完全沉淀时的 | 9.4 | 6.7 | 8.8 | 2.9 | 10.9 |
A.“滤渣I”的主要成份为 |
B.氧化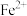 时发生反应的离子方程式为: 时发生反应的离子方程式为: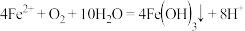 |
C.“沉钴”时,用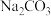 溶液代替 溶液代替 溶液可以提高 溶液可以提高 的纯度 的纯度 |
D. 溶液中存在:c(Na+)+c(H+)=c( 溶液中存在:c(Na+)+c(H+)=c( )+c( )+c( )+c(OH-) )+c(OH-) |
您最近一年使用:0次
解题方法
7 . 如图,是工业生产中除去电石渣浆(含CaO)中的 并制取硫酸盐的一种常用流程。下列说法错误的是
并制取硫酸盐的一种常用流程。下列说法错误的是
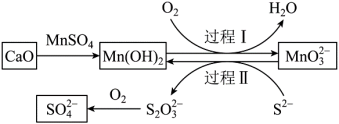
 并制取硫酸盐的一种常用流程。下列说法错误的是
并制取硫酸盐的一种常用流程。下列说法错误的是
A.碱性条件下,氧化性: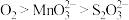 |
| B.过程Ⅰ中氧化剂和还原剂物质的量之比为1∶2 |
C.过程Ⅰ中,反应的离子方程式为 |
D.将1mol  转化为 转化为 理论上需要 理论上需要 的体积为22.4L(标准状况) 的体积为22.4L(标准状况) |
您最近一年使用:0次
解题方法
8 . 下列方程式错误的是
A.在弱碱性条件下,FeS与 反应: 反应: |
B.将少量浓氨水滴入盛有CaO的烧瓶制备 : : |
C.小苏打与明矾共溶于水,产生大量气泡: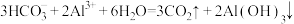 |
D.铅酸蓄电池正极反应: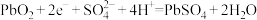 |
您最近一年使用:0次
解题方法
9 . 硫化氢的转化是资源利用和环境保护的重要研究课题。 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化关系如图所示(CuS不溶于水)。下列说法中不正确的是
的混合溶液中回收S,其转化关系如图所示(CuS不溶于水)。下列说法中不正确的是

 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化关系如图所示(CuS不溶于水)。下列说法中不正确的是
的混合溶液中回收S,其转化关系如图所示(CuS不溶于水)。下列说法中不正确的是
A.过程中①中生成CuS的反应为: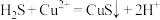 |
B.由图示的转化可得出氧化性的强弱顺序: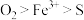 |
| C.在转化过程中化合价不变的元素只有:Cu和Cl |
D.回收S的总反应为: |
您最近一年使用:0次
10 . 实验室,以 为原料制备
为原料制备 、KOH的工艺流程如下图所示:
、KOH的工艺流程如下图所示:
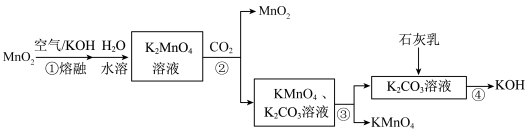
下列说法正确的是
 为原料制备
为原料制备 、KOH的工艺流程如下图所示:
、KOH的工艺流程如下图所示:
下列说法正确的是
| A.步骤①用烧杯作反应器 | B.步骤②中 只体现还原性 只体现还原性 |
| C.步骤③用到的玻璃仪器有漏斗、烧杯、玻璃棒等 | D.步骤④过程中有电子转移 |
您最近一年使用:0次



