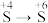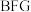1 . 已知 ,甲同学将
,甲同学将 、
、 混合气体通入稍过量
混合气体通入稍过量 溶液中制备
溶液中制备 (同等条件下
(同等条件下 的氧化性强于
的氧化性强于 ),为检验制得了
),为检验制得了 ,甲进行了以下实验:
,甲进行了以下实验:
下列说法不正确的是
 ,甲同学将
,甲同学将 、
、 混合气体通入稍过量
混合气体通入稍过量 溶液中制备
溶液中制备 (同等条件下
(同等条件下 的氧化性强于
的氧化性强于 ),为检验制得了
),为检验制得了 ,甲进行了以下实验:
,甲进行了以下实验:| 实验 | 实验现象 | |
| ① | 取 制备的稀溶液,加 制备的稀溶液,加 溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | 不变蓝 |
| ② | 取 制备的稀溶液,滴加几滴 制备的稀溶液,滴加几滴 至 至 ,加 ,加 溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | |
| ③ | 取 水,滴加几滴 水,滴加几滴 至 至 ,加 ,加 溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | 不变蓝 |
A.实验①说明 不能氧化 不能氧化 |
| B.实验②的实验现象是溶液变蓝 |
C.实验③的目的是验证当溶液 时,稀 时,稀 不能氧化 不能氧化 |
D.上述3组实验无法证明②中一定含 ,还需补充实验 ,还需补充实验 |
您最近一年使用:0次
2 . 某兴趣小组用 和浓盐酸制取氯气并探究氯、溴、碘的相关性质,设计装置图如图所示(夹持装置已略去)。已知:①氧化性:
和浓盐酸制取氯气并探究氯、溴、碘的相关性质,设计装置图如图所示(夹持装置已略去)。已知:①氧化性: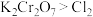 ;②酸性条件下,
;②酸性条件下, 被还原为
被还原为 。下列说法错误的是
。下列说法错误的是

 和浓盐酸制取氯气并探究氯、溴、碘的相关性质,设计装置图如图所示(夹持装置已略去)。已知:①氧化性:
和浓盐酸制取氯气并探究氯、溴、碘的相关性质,设计装置图如图所示(夹持装置已略去)。已知:①氧化性: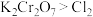 ;②酸性条件下,
;②酸性条件下, 被还原为
被还原为 。下列说法错误的是
。下列说法错误的是
A.装置A中发生反应的离子方程式: |
| B.若装置C发生堵塞,B中长颈漏斗内液面会上升 |
| C.为验证氯气是否具有漂白性,Ⅰ、Ⅱ、Ⅲ处分别放置湿润的有色布条、无水氯化钙、干燥的有色布条 |
D.通入足量的氯气,打开E的活塞,将溶液滴入D中,锥形瓶下层液体呈紫色即证明氧化性 |
您最近一年使用:0次
名校
解题方法
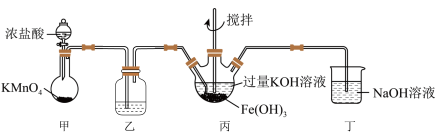
3 . 下图是实验室制备 的实验装置图,其中甲为制氯气的装置。(资料:
的实验装置图,其中甲为制氯气的装置。(资料: 为紫色固体,微溶于KOH,具有强氧化性)
为紫色固体,微溶于KOH,具有强氧化性)
下列说法不正确 的是
 的实验装置图,其中甲为制氯气的装置。(资料:
的实验装置图,其中甲为制氯气的装置。(资料: 为紫色固体,微溶于KOH,具有强氧化性)
为紫色固体,微溶于KOH,具有强氧化性)
下列说法
A.甲装置不需要加热即可以产生氯气,说明氧化性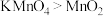 |
B.丙和丁中均会发生反应: |
C.丙中产生紫色固体,说明碱性条件下, 氧化性强于 氧化性强于 |
D.若取反应后丙中紫色溶液加入稀硫酸产生 ,可以证明 ,可以证明 具有氧化性 具有氧化性 |
您最近一年使用:0次
解题方法
4 . 硫元素广泛存在于自然界中,是植物生长不可缺少的元素。回答下列问题:
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A. 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液
D.稀硫酸 E.酸性 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝
实验i选择的试剂是E和______ (填字母),证明实现转化的现象是______ 。
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。
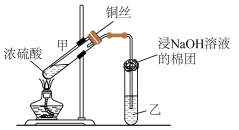
①试管甲中发生反应的化学方程式是__________ 。
②试管乙中的现象是_______ ;若实验结束后,将试管乙中的溶液加热,可以观察到的现象是______ 。
③下列关于 的说法,不正确的是
的说法,不正确的是__________ 。(填字母)
a.正常雨水的 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7
b.金属冶炼时产生的含 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸
c. 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
(1)某小组同学设计实验实现不同价态含硫物质的转化。
可选用的实验试剂如下:
A.
 溶液 B.浓硫酸 C.
溶液 B.浓硫酸 C. 溶液
溶液D.稀硫酸 E.酸性
 溶液 F.品红溶液 G.铜丝
溶液 F.品红溶液 G.铜丝实验序号 | 预期转化 | 选择试剂 | 证明实现转化的现象 |
i |
| ||
ii |
|
|
(2)该小组同学利用所选试剂,设计了如图所示装置研究实验ⅱ。

①试管甲中发生反应的化学方程式是
②试管乙中的现象是
③下列关于
 的说法,不正确的是
的说法,不正确的是a.正常雨水的
 等于7,酸雨因为溶解了
等于7,酸雨因为溶解了 ,其
,其 小于7
小于7b.金属冶炼时产生的含
 废气经回收后可用于制备硫酸
废气经回收后可用于制备硫酸c.
 在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成
您最近一年使用:0次
名校
解题方法
5 . 某化学兴趣小组利用以下装置制备干燥的氯气并对氯气的性质进行探究。
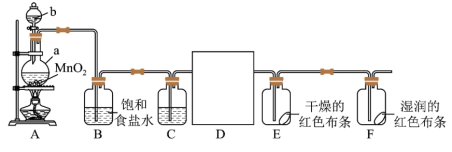
(1)仪器a的名称为_____ 。某同学认为该实验装置存在一处明显的不足,其改进措施为_____ 。
(2)仪器a中发生反应的化学方程式为_____ 。根据氯气的性质D中的收集装置可以选择_____ (填序号)。
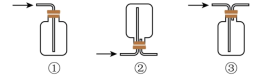
(3)下列有关该实验的说法中不正确的是_____ (填字母)。
a.将b中液体换为稀盐酸,同样可以产生氯气
b.C中试剂是浓硫酸,目的是干燥氯气
c.E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
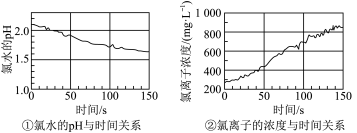
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如图曲线。请用化学方程式解释曲线中氯离子的浓度和pH变化的原因:_____ 。
(5)实验室还可用等物质的量的Cl2与Na2CO3的水溶液反应制取Cl2O,同时生成NaHCO3和NaCl,反应的离子方程式为_____ 。
(6)一定条件下,在一定量的NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中含有三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
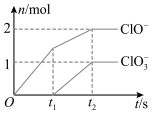
该过程中参加反应Cl2的物质的量是_____ mol,参加反应的NaOH的物质的量为_____ mol。

(1)仪器a的名称为
(2)仪器a中发生反应的化学方程式为

(3)下列有关该实验的说法中不正确的是
a.将b中液体换为稀盐酸,同样可以产生氯气
b.C中试剂是浓硫酸,目的是干燥氯气
c.E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如图曲线。请用化学方程式解释曲线中氯离子的浓度和pH变化的原因:

(5)实验室还可用等物质的量的Cl2与Na2CO3的水溶液反应制取Cl2O,同时生成NaHCO3和NaCl,反应的离子方程式为
(6)一定条件下,在一定量的NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中含有三种含氯元素的离子,其中ClO-、ClO
 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
该过程中参加反应Cl2的物质的量是
您最近一年使用:0次
名校
解题方法
6 . 我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。
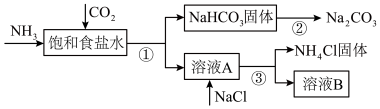
(1)饱和食盐水中通二氧化碳和氨气的化学方程式是_______
(2)下列说法中合理的是_______(填标号)。
(3)一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,在疫情期间外出需戴好口罩,返家后立即杀菌消毒。双氧水和84消毒液是日常生活常用的消毒剂,二氧化氯 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。
①某同学设计如下实验研究 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是_______ (填序号)
②某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
_______  (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为_______ mol。
③ 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式_______ ,将 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式_______ 。

(1)饱和食盐水中通二氧化碳和氨气的化学方程式是
(2)下列说法中合理的是_______(填标号)。
A.副产物 可用作氮肥 可用作氮肥 |
B.溶液B中的主要离子是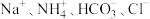 |
C.制碱流程中可回收并循环利用的物质只有碳酸氢钠分解产生的 |
| D.饱和食盐水中应该先通二氧化碳至饱和,再通入氨气至饱和 |
 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。①某同学设计如下实验研究
 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是| 序号 | 实验 | 实验现象 |
| 1 | 向 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色裉去;b.有大量气泡产生 |
| 2 | 向 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为③
 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
您最近一年使用:0次
2023-01-07更新
|
487次组卷
|
3卷引用:辽宁省沈阳市回民中学2022-2023学年高一上学期期末线上考试化学试题
7 . 某实验小组通过如图所示装置进行实验,验证CO2能与Na2O2反应产生O2。下列说法错误的是
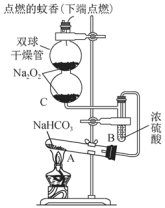

| A.试管可以用来直接加热,加热固体时试管口略向下倾斜 |
| B.将装置B撤掉也可以得到同样的实验结论 |
| C.蚊香燃烧更旺可以证明CO2与Na2O2反应产生了O2 |
| D.该反应过程中Na2O2既是氧化剂又是还原剂,O2为氧化产物 |
您最近一年使用:0次
名校
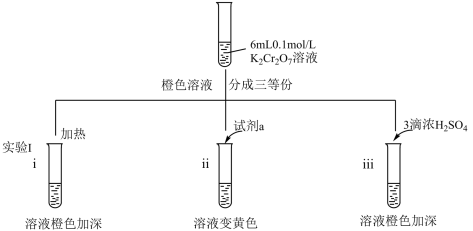
8 . 某兴趣小组以重铬酸钾(K2Cr2O7)溶液为研究对象,结合所学反应原理的知识改变条件使其发生“色彩变幻”。下列关于该实验的说法错误的是
已知:①K2Cr2O7溶液存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。
②含铬元素的离子在溶液中的颜色:Cr2O (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。
已知:①K2Cr2O7溶液存在平衡:Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+。
+2H+。 ②含铬元素的离子在溶液中的颜色:Cr2O
 (橙色);CrO
(橙色);CrO (黄色);Cr 3+ (绿色)。
(黄色);Cr 3+ (绿色)。 
A.i 可证明反应 Cr2O +H2O +H2O 2CrO 2CrO +2H+的正反应放热 +2H+的正反应放热 |
| B.ii 是验证“只降低生成物的浓度,该平衡正向移动”,试剂 a 可以是 NaOH |
| C.iii 平衡逆向移动仅仅是因为增大了生成物的浓度 |
| D.向 iii 所得橙色溶液中加入乙醇,溶液将由橙色变为绿色 |
您最近一年使用:0次
2023-08-26更新
|
402次组卷
|
4卷引用:湖北省新高考联盟2023-2024学年高二上学期8月开学联考化学试题
9 . 北京市施行的《北京市小规模食品生产经营管理规定》中明确规定:小规模食品生产经营者不得购进、存放、使用亚硝酸盐等易滥用的食品添加剂。
(1)根据物质组成上分类,亚硝酸钠 属于
属于_______  填序号
填序号
A.钠盐 B.硝酸盐 C.氧化物
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠,有关反应的化学方程式如下:

①上述两个反应中,属于氧化还原反应的是_______ (填“ ”或“
”或“ ”
” 。
。
②其中的氧化还原反应的氧化剂是_______  填化学式
填化学式 ,用双线桥法表示该氧化还原反应中电子转移情况:
,用双线桥法表示该氧化还原反应中电子转移情况:_______ 。
(3)亚硝酸钠外观与食盐相似,且均有咸味。
①若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是_______ 。
A.亚硝酸钠是还原剂 B.维生素C是氧化剂
C.维生素C能把铁离子还原成为亚铁离子 D.亚硝酸钠被还原
②鉴别方法如下:将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再滴加淀粉溶液如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠;如果溶液无变化,则可以证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可表示为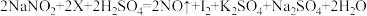 (已配平),其中X是
(已配平),其中X是_______ (填化学式)。
(1)根据物质组成上分类,亚硝酸钠
 属于
属于 填序号
填序号
A.钠盐 B.硝酸盐 C.氧化物
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠,有关反应的化学方程式如下:

①上述两个反应中,属于氧化还原反应的是
 ”或“
”或“ ”
” 。
。②其中的氧化还原反应的氧化剂是
 填化学式
填化学式 ,用双线桥法表示该氧化还原反应中电子转移情况:
,用双线桥法表示该氧化还原反应中电子转移情况:(3)亚硝酸钠外观与食盐相似,且均有咸味。
①若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是
A.亚硝酸钠是还原剂 B.维生素C是氧化剂
C.维生素C能把铁离子还原成为亚铁离子 D.亚硝酸钠被还原
②鉴别方法如下:将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再滴加淀粉溶液如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠;如果溶液无变化,则可以证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可表示为
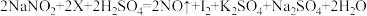 (已配平),其中X是
(已配平),其中X是
您最近一年使用:0次
解题方法
10 . 如图所示,向无色的 溶液中加入氯水,得到棕黄色溶液,下列说法不正确的是
溶液中加入氯水,得到棕黄色溶液,下列说法不正确的是

 溶液中加入氯水,得到棕黄色溶液,下列说法不正确的是
溶液中加入氯水,得到棕黄色溶液,下列说法不正确的是
| A.与氯水颜色相比较,溶液颜色发生变化,可证明已发生了反应 |
B.发生的氧化还原反应可表示为: |
C. 和 和 分子中都只含有非极性共价键 分子中都只含有非极性共价键 |
| D.该实验结果证明:氯元素的非金属性强于碘元素 |
您最近一年使用:0次