名校
1 . 亚硝酸钠(NaNO2)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生Na2O、N2和O2,其水溶液呈碱性,能与AgNO3溶液反应生成难溶于水、易溶于酸的AgNO2。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____NO +_____I-+______=____NO↑+_____I2+_____H2O。
+_____I-+______=____NO↑+_____I2+_____H2O。
(1)请完成该离子方程式并配平_______ 。
(2)从物质分类角度来看,NaNO2是_______ (填字母代号)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是_______ 。从环保角度来讲,要将NaNO2转化为氮气,所用物质的_______ (填“氧化性”或“还原性”)应该比KI更______ (填“强”或“弱”)。
(4)下列方法不能用来区分固体NaNO2和NaCl的是______ (填序号)。
(5)误食NaNO2会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,该过程中NaNO2表现出的性质与下列_______ (填序号)反应中H2O2表现出的性质相同。
A.2H2O2 2H2O+O2↑
2H2O+O2↑
B.H2O2+Cl2=2HCl+O2↑
C.H2O2+H2SO4+2KI=2H2O+I2+K2SO4
(6)S2O 可以与Fe2+反应制备Fe2O3纳米颗粒。若S2O
可以与Fe2+反应制备Fe2O3纳米颗粒。若S2O 与Fe2+的系数之比为1:2,配平该反应的离子方程式:_______Fe2++_______S2O
与Fe2+的系数之比为1:2,配平该反应的离子方程式:_______Fe2++_______S2O +_______H2O2+_______OH-=_______Fe2O3+_______S2O
+_______H2O2+_______OH-=_______Fe2O3+_______S2O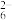 +_______H2O。
+_______H2O。_______
 +_____I-+______=____NO↑+_____I2+_____H2O。
+_____I-+______=____NO↑+_____I2+_____H2O。(1)请完成该离子方程式并配平
(2)从物质分类角度来看,NaNO2是
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
(4)下列方法不能用来区分固体NaNO2和NaCl的是
| A.分别溶于水,滴加酚酞试液 | B.分别溶于水并滴加HNO3酸化的AgNO3溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
A.2H2O2
 2H2O+O2↑
2H2O+O2↑B.H2O2+Cl2=2HCl+O2↑
C.H2O2+H2SO4+2KI=2H2O+I2+K2SO4
(6)S2O
 可以与Fe2+反应制备Fe2O3纳米颗粒。若S2O
可以与Fe2+反应制备Fe2O3纳米颗粒。若S2O 与Fe2+的系数之比为1:2,配平该反应的离子方程式:_______Fe2++_______S2O
与Fe2+的系数之比为1:2,配平该反应的离子方程式:_______Fe2++_______S2O +_______H2O2+_______OH-=_______Fe2O3+_______S2O
+_______H2O2+_______OH-=_______Fe2O3+_______S2O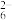 +_______H2O。
+_______H2O。
您最近一年使用:0次
2 . 稀土元素铈及其化合物在生产生活中有重要用途,如汽车尾气用稀土/钯三效催化剂处理,不仅可以降低催化剂的成本,还可以提高催化效能。以氟碳铈矿(主要成分为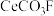 )为原料制备
)为原料制备 的一种工艺流程如图:
的一种工艺流程如图: ,滤渣2的主要成分是
,滤渣2的主要成分是 ;
; ,
, (a、b均大于0)。
(a、b均大于0)。
②当前工艺条件下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于 mol⋅L
mol⋅L )时的pH如下表:
)时的pH如下表:
回答下列问题:
(1)写出一条提高焙烧效率的方法:_______ 。
(2)加入盐酸和 进行浸取时有污染环境的气体产生,该气体为
进行浸取时有污染环境的气体产生,该气体为_______ (填化学式);操作1和操作2的名称为_______ 。
(3)调节滤液1的pH的范围为_______ ;滤渣3的主要成分为_______ (填化学式)。
(4)滤渣1经KCl溶液充分浸取后,测得反应体系中 的物质的量浓度为0.1 mol⋅L
的物质的量浓度为0.1 mol⋅L ,则
,则 的物质的量浓度为
的物质的量浓度为_______ mol⋅L (用含a、b的式子表示)。
(用含a、b的式子表示)。
(5)在空气中焙烧 的反应方程式为
的反应方程式为_______ 。
(6)某研究小组利用硫化锌锂电池在酸性环境下电解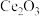 制
制 ,电解装置及硫化锌锂电池负极材料晶胞组成变化如图所示。
,电解装置及硫化锌锂电池负极材料晶胞组成变化如图所示。_______ ,随着电解反应的进行,为使电解液成分稳定,应不断补充_______ (填化学式)。
②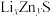 中
中
_______ ,若该晶胞边长为a nm, 为阿伏加德罗常数的值,则
为阿伏加德罗常数的值,则 晶体的密度为
晶体的密度为_______ g·cm 。
。
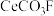 )为原料制备
)为原料制备 的一种工艺流程如图:
的一种工艺流程如图:
 ,滤渣2的主要成分是
,滤渣2的主要成分是 ;
; ,
, (a、b均大于0)。
(a、b均大于0)。②当前工艺条件下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于
 mol⋅L
mol⋅L )时的pH如下表:
)时的pH如下表:| 金属阳离子 |  |  |
| 开始沉淀时的pH | 1.3 | 7.7 |
| 完全沉淀时的pH | 3.1 | 9.2 |
(1)写出一条提高焙烧效率的方法:
(2)加入盐酸和
 进行浸取时有污染环境的气体产生,该气体为
进行浸取时有污染环境的气体产生,该气体为(3)调节滤液1的pH的范围为
(4)滤渣1经KCl溶液充分浸取后,测得反应体系中
 的物质的量浓度为0.1 mol⋅L
的物质的量浓度为0.1 mol⋅L ,则
,则 的物质的量浓度为
的物质的量浓度为 (用含a、b的式子表示)。
(用含a、b的式子表示)。(5)在空气中焙烧
 的反应方程式为
的反应方程式为(6)某研究小组利用硫化锌锂电池在酸性环境下电解
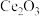 制
制 ,电解装置及硫化锌锂电池负极材料晶胞组成变化如图所示。
,电解装置及硫化锌锂电池负极材料晶胞组成变化如图所示。
②
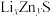 中
中
 为阿伏加德罗常数的值,则
为阿伏加德罗常数的值,则 晶体的密度为
晶体的密度为 。
。
您最近一年使用:0次
3 .  在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。
在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。
I. 的性质探究
的性质探究
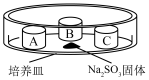
装置如下表(图)所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向 固体上滴加
固体上滴加 硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。
硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。
(1)70%浓硫酸溶液和 固体反应制备
固体反应制备 的化学方程式为
的化学方程式为________________________________ 。
(2)瓶盖A中发生反应的化学方程式为________________________________ 。
(3)瓶盖A中无明显变化,若要证明A中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是_______ (填字母)。
a. 溶液 b.
溶液 b. 溶液 c.石蕊溶液
溶液 c.石蕊溶液
(4)瓶盖_______ (填字母)中的实验现象能证明 具有还原性,反应的离子方程式为
具有还原性,反应的离子方程式为______________ 。
(5)综合上述实验信息可证明 具有还原性、
具有还原性、___________________________________ 等性质。
(6)增加瓶盖D可验证 具有氧化性,则D中盛装的试剂及现象是
具有氧化性,则D中盛装的试剂及现象是__________________________ 。
II.化石燃料燃烧会产生大量的 ,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。
,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。
(7)如果不对燃煤烟气脱硫,易形成硫酸型酸雨,酸雨一般指的是 小于
小于_______________ 的降雨。
(8)方法I中氨水吸收燃煤烟气中 的化学反应为:
的化学反应为: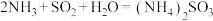 、
、__________ 。
(9)方法II中用 将
将 还原为S时,
还原为S时, 转化为
转化为_______________ (填化学式)。
(10)对方法III吸收 后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
后的溶液加热可使吸收液再生,其反应属于基本反应类型中的___________ 反应。
 在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。
在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。I.
 的性质探究
的性质探究装置如下表(图)所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向
 固体上滴加
固体上滴加 硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。
硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。实验装置 | 㼛盖 | 物质 | 实验现象 |
| A | 蒸馏水 | 无明显变化 |
B |
| 溶液褪色 | |
C | 蘸有品红溶液的棉花 | 品红溶液褪色 |
(1)70%浓硫酸溶液和
 固体反应制备
固体反应制备 的化学方程式为
的化学方程式为(2)瓶盖A中发生反应的化学方程式为
(3)瓶盖A中无明显变化,若要证明A中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是
a.
 溶液 b.
溶液 b. 溶液 c.石蕊溶液
溶液 c.石蕊溶液(4)瓶盖
 具有还原性,反应的离子方程式为
具有还原性,反应的离子方程式为(5)综合上述实验信息可证明
 具有还原性、
具有还原性、(6)增加瓶盖D可验证
 具有氧化性,则D中盛装的试剂及现象是
具有氧化性,则D中盛装的试剂及现象是II.化石燃料燃烧会产生大量的
 ,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。
,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。方法1 | 用氨水将 转化为 转化为 ,再氧化成 ,再氧化成 |
方法2 | 用生物质热解气(主要成分 、 、 、 、 )将 )将 在高温下还原成单质硫,其他生成物均可直接排放 在高温下还原成单质硫,其他生成物均可直接排放 |
方法3 | 用 溶液吸收 溶液吸收 ,再经电解转化为 ,再经电解转化为 |
(7)如果不对燃煤烟气脱硫,易形成硫酸型酸雨,酸雨一般指的是
 小于
小于(8)方法I中氨水吸收燃煤烟气中
 的化学反应为:
的化学反应为: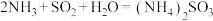 、
、(9)方法II中用
 将
将 还原为S时,
还原为S时, 转化为
转化为(10)对方法III吸收
 后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
您最近一年使用:0次
2024-01-17更新
|
120次组卷
|
2卷引用:福建省厦门第一中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
4 . 放热反应在生产、生活中用途广泛。
(1)已知 时,
时, 甲烷不完全燃烧生成
甲烷不完全燃烧生成 和液态水时放出
和液态水时放出 热量,则
热量,则 甲烷不完全燃烧的热化学方程式为
甲烷不完全燃烧的热化学方程式为___________ 。
(2)甲烷可以消除氮氧化物污染,发生的反应为 ,在体积固定的密闭容器中,每次实验均加入
,在体积固定的密闭容器中,每次实验均加入 和
和 ,使
,使 、
、 ,在不同条件下进行反应,测得
,在不同条件下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:
①实验1中,在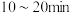 内,
内,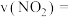
___________ ,40min时v(正)___________ v(逆)(填:“大于”、“小于”、“等于”)。
②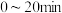 内,实验2比实验1反应速率快的原因可能是
内,实验2比实验1反应速率快的原因可能是___________ 。
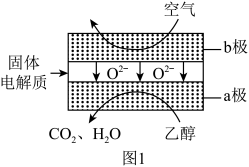
(3)乙醇应用于燃料电池,该电池采用可传导 的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为
的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为___________ 。
(4)硝酸铵在高温或猛烈撞击时易爆炸,放出大量的热。 高温分解不可能生成
高温分解不可能生成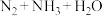 。理由是
。理由是___________ 。
(1)已知
 时,
时, 甲烷不完全燃烧生成
甲烷不完全燃烧生成 和液态水时放出
和液态水时放出 热量,则
热量,则 甲烷不完全燃烧的热化学方程式为
甲烷不完全燃烧的热化学方程式为(2)甲烷可以消除氮氧化物污染,发生的反应为
 ,在体积固定的密闭容器中,每次实验均加入
,在体积固定的密闭容器中,每次实验均加入 和
和 ,使
,使 、
、 ,在不同条件下进行反应,测得
,在不同条件下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:| 实验序号 | 时间/ 温度  浓度/℃ | 10 | 20 | 30 | 40 | 50 |
| 1 | 800 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
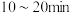 内,
内,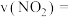
②
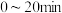 内,实验2比实验1反应速率快的原因可能是
内,实验2比实验1反应速率快的原因可能是(3)乙醇应用于燃料电池,该电池采用可传导
 的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为
的固体氧化物为电解质,其工作原理如图1所示。b极电极反应式为
(4)硝酸铵在高温或猛烈撞击时易爆炸,放出大量的热。
 高温分解不可能生成
高温分解不可能生成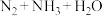 。理由是
。理由是
您最近一年使用:0次
名校
解题方法
5 . 氧化还原反应在日常生活和工业生产中有重要应用。
I.已知反应:
(1)该反应中被还原的元素是_____ ,氧化产物是_____ 。
(2)在该反应中 既表现还原性又表现
既表现还原性又表现_____ 性。
(3)用双线桥标出电子转移的数目_____ 。
Ⅱ.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
【化学式】
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着 减小,稳定性下降,与水反应放出氧气。
减小,稳定性下降,与水反应放出氧气。 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用
胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化 水投放
水投放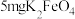 即可达到卫生标准
即可达到卫生标准
(4) 中铁元素的化合价为
中铁元素的化合价为_____ 。
(5)工业制备 需要在碱性环境下进行,现提供反应体系中7种物质,
需要在碱性环境下进行,现提供反应体系中7种物质,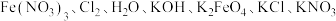 请写出制备
请写出制备 的化学反应方程式
的化学反应方程式_____ 。
I.已知反应:

(1)该反应中被还原的元素是
(2)在该反应中
 既表现还原性又表现
既表现还原性又表现(3)用双线桥标出电子转移的数目
Ⅱ.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
【化学式】

【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着
 减小,稳定性下降,与水反应放出氧气。
减小,稳定性下降,与水反应放出氧气。 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用
胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化
 水投放
水投放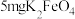 即可达到卫生标准
即可达到卫生标准(4)
 中铁元素的化合价为
中铁元素的化合价为(5)工业制备
 需要在碱性环境下进行,现提供反应体系中7种物质,
需要在碱性环境下进行,现提供反应体系中7种物质,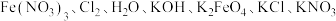 请写出制备
请写出制备 的化学反应方程式
的化学反应方程式
您最近一年使用:0次
6 . 氧化还原反应在生产、生活中有广泛的用途。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4═3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是_______ (填化学式,下同),还原剂是_______ ,氧化产物和还原产物的个数比是_______ 。
Ⅱ.工业废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+═6Fe3++2Cr3++7H2O。
+14H+═6Fe3++2Cr3++7H2O。
(2)在该反应中,被氧化的是_______ (填离子符号,下同),还原产物是_______ ,此反应可以推断物质还原性强弱顺序是__________ 。
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2 +____+5H2O。
+____+5H2O。
(3)请完成该化学方程式并配平_______ 。
(4)该反应中生成2个 转移的电子数为
转移的电子数为_______ 。
(5)氧化还原反应配平
①_______S+_______KOH═_______K2S+_______K2SO3+_______H2O
②_______Fe(OH)3+_______CH4+_______H+=_______Fe2++_______HCO +_______H2O
+_______H2O
①_______ 。
②_______ 。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4═3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是
Ⅱ.工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式如下:6Fe2++Cr2O +14H+═6Fe3++2Cr3++7H2O。
+14H+═6Fe3++2Cr3++7H2O。(2)在该反应中,被氧化的是
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2
 +____+5H2O。
+____+5H2O。(3)请完成该化学方程式并配平
(4)该反应中生成2个
 转移的电子数为
转移的电子数为(5)氧化还原反应配平
①_______S+_______KOH═_______K2S+_______K2SO3+_______H2O
②_______Fe(OH)3+_______CH4+_______H+=_______Fe2++_______HCO
 +_______H2O
+_______H2O①
②
您最近一年使用:0次
解题方法
7 . 钠元素在自然界中以多种化合物的形式存在。
(1)Na2O2、Na2CO3、NaHCO3是重要的化工原料,具有多种用途。
①Na2O2可在呼吸面具和潜水艇中作为氧气的来源,请写出Na2O2与CO2反应的化学方程式_______ 。
②将一定量的Na2O2固体投入到含有下列离子的溶液中:Cl-、HCO 、CO
、CO 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有_______ (填离子符号),上述离子中有一种离子数目明显减少,减少的原因是_______ (用离子方程式表示)。
③查阅资料知:Na2O2在一定条件下可以转化为NaNO2,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,误食NaNO2后可服用维生素C解毒。下列分析错误的是_______ (填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性:维生素C>Fe2+ D.NaNO2是还原剂
(2)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要工艺流程如下图所示(部分物质已略去)。
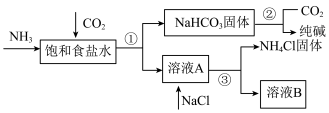
①实验室模拟“侯氏制碱法”,下列操作未涉及的是_______ (填字母)。
A.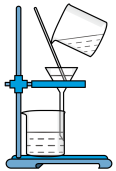 B.
B. C.
C. D.
D.
②下列联合制碱法流程说法正确的是_______ (填字母)。
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH 、Cl-
、Cl-
③该工艺制得的纯碱中往往会含有杂质NaCl,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,_______ 。
④为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,取5.00gNa2CO3样品充分加热,当固体质量不再变化时,再次称量固体质量为4.69g,写出加热时发生反应的化学方程式_______ ,该样品中Na2CO3的纯度是_______ 。
(1)Na2O2、Na2CO3、NaHCO3是重要的化工原料,具有多种用途。
①Na2O2可在呼吸面具和潜水艇中作为氧气的来源,请写出Na2O2与CO2反应的化学方程式
②将一定量的Na2O2固体投入到含有下列离子的溶液中:Cl-、HCO
 、CO
、CO 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有③查阅资料知:Na2O2在一定条件下可以转化为NaNO2,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,误食NaNO2后可服用维生素C解毒。下列分析错误的是
A.NaNO2被还原 B.维生素C具有还原性
C.还原性:维生素C>Fe2+ D.NaNO2是还原剂
(2)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要工艺流程如下图所示(部分物质已略去)。

①实验室模拟“侯氏制碱法”,下列操作未涉及的是
A.
 B.
B. C.
C. D.
D.
②下列联合制碱法流程说法正确的是
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH
 、Cl-
、Cl-③该工艺制得的纯碱中往往会含有杂质NaCl,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,
④为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,取5.00gNa2CO3样品充分加热,当固体质量不再变化时,再次称量固体质量为4.69g,写出加热时发生反应的化学方程式
您最近一年使用:0次
8 . Na2O2是重要的化工原料,具有多种用途。
(1)Na2O2可在呼吸面具和潜水艇中作为氧气的来源,请写出Na2O2与CO2反应的化学方程式_______ 。
(2)将一定量的Na2O2固体投入到含有下列离子的溶液中:Cl-、HCO 、CO
、CO 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有_______ (填离子符号)。
(3)查阅资料知:Na2O2在一定条件下可以转化为NaNO2,NaNO2易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
①已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。上述反应中氧化剂是_______ ,氧化产物是_______ ;HI在反应中体现了什么性质_______ 。
②根据上述反应鉴别NaNO2和NaCl,可选用的物质有_______ (填序号)。
A.食用白醋 B.碘化钾淀粉试纸 C.淀粉 D.白酒
③某厂废液中含有3%—6%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是_______ (填序号)。
A.浓硫酸 B.NH4Cl C.HNO3 D.KMnO4
(1)Na2O2可在呼吸面具和潜水艇中作为氧气的来源,请写出Na2O2与CO2反应的化学方程式
(2)将一定量的Na2O2固体投入到含有下列离子的溶液中:Cl-、HCO
 、CO
、CO 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有(3)查阅资料知:Na2O2在一定条件下可以转化为NaNO2,NaNO2易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒。请回答下列问题:
①已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。上述反应中氧化剂是
②根据上述反应鉴别NaNO2和NaCl,可选用的物质有
A.食用白醋 B.碘化钾淀粉试纸 C.淀粉 D.白酒
③某厂废液中含有3%—6%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是
A.浓硫酸 B.NH4Cl C.HNO3 D.KMnO4
您最近一年使用:0次
2023-11-07更新
|
352次组卷
|
2卷引用:黑龙江省大庆铁人中学2023-2024学年高一上学期10月月考化学试题
2023高三·全国·专题练习
9 . 氧化还原反应在工业生产、环保及科研中有广泛的应用,请根据以上信息,结合自己所掌握的化学知识,回答下列问题:
Ⅰ.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成CuH。CuH具有的性质:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是2Cu+=Cu2++Cu。
(1)写出CuH在氯气中燃烧的化学方程式:___________ 。
(2)CuH溶解在稀盐酸中生成的气体是___________ (填化学式)。
(3)将CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:___________ 。
Ⅱ.钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(4)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是___________ 。
(5)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应而被吸收,则 、Cl-、VO2+还原性由强到弱的顺序是
、Cl-、VO2+还原性由强到弱的顺序是___________ 。
Ⅰ.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成CuH。CuH具有的性质:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是2Cu+=Cu2++Cu。
(1)写出CuH在氯气中燃烧的化学方程式:
(2)CuH溶解在稀盐酸中生成的气体是
(3)将CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
Ⅱ.钒性能优良,用途广泛,有金属“维生素”之称。完成下列填空:
(4)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是
(5)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应而被吸收,则
 、Cl-、VO2+还原性由强到弱的顺序是
、Cl-、VO2+还原性由强到弱的顺序是
您最近一年使用:0次
10 . 物质的性质决定用途,下列物质的用途及原理正确的是
| A.瓷坩埚耐高温,可用于加热分解石灰石 |
| B.铝粉与NaOH溶液反应放热,可用于厨卫管道疏通 |
C. 具有强氧化性,可用于除去硬水中的 具有强氧化性,可用于除去硬水中的 、 、 |
| D.钛合金具有高强韧性,可用于制造载人潜水器的耐压舱 |
您最近一年使用:0次

 酸性溶液
酸性溶液

