名校
解题方法
1 . 某学习小组的同学用MnO2和浓盐酸反应来制备纯净的氯气并验证其有无漂白性,设计装置如图:

(1)A装置中反应的化学方程式:____________________________ ;D装置中现象:___________________ ;该套装置存在的缺陷:_________________________________ 。
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是_______________________ (用离子方程式表示)。
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了_______________ 。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为__________________ 。
(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是___________ ,CuO的作用是_____________ ,写出总反应的化学方程式,并用单线桥法标出该反应的电子转移情况______________________________ 。


(1)A装置中反应的化学方程式:
(2)取少量E装置中溶液与洁厕灵(含盐酸)混合产生有毒气体,原因是
(3)若将Cl2通入热的烧碱溶液中,可以发生如下两个反应:
Cl2+2NaOH=NaCl+NaClO+H2O和3Cl2+6NaOH=5NaCl+NaClO3+3H2O。
从氧化还原角度分析Cl2表现了
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(4)近年来,随着化学工业的快速发展,氯气的需求迅速增加。下图是制备氯气的原理示意图,其反应物是

您最近一年使用:0次
2022-12-14更新
|
395次组卷
|
3卷引用:四川省泸州市泸县2022-2023学年高一下学期开学考试化学试题
2 . 如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
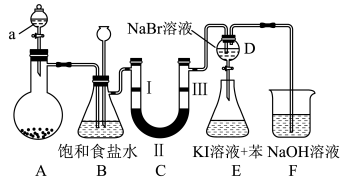
(1)仪器a的名称___________ 。
(2)制备氯气选用的药品为二氧化锰和浓盐酸,则相关的化学反应方程式为___________ 。
(3)装置B中饱和食盐水的作用是___________ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________ 。
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入___________ 。
(5)装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,反应的离子方程式为___________ ,打开活塞,将装置D中少量溶液加入装置E中,振荡、静置,观察到的现象为溶液分层,上层溶液为紫红色,下层几乎无色,根据实验得出氯、溴、碘单质的氧化性强弱为___________ 。
(6)装置F中用足量的 溶液吸收多余的氯气,试写出相应的离子方程式
溶液吸收多余的氯气,试写出相应的离子方程式___________ 。

(1)仪器a的名称
(2)制备氯气选用的药品为二氧化锰和浓盐酸,则相关的化学反应方程式为
(3)装置B中饱和食盐水的作用是
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| 选项 | a | b | c | d |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 浓硫酸 | 硅胶 | 无水氯化钙 | 碱石灰 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(6)装置F中用足量的
 溶液吸收多余的氯气,试写出相应的离子方程式
溶液吸收多余的氯气,试写出相应的离子方程式
您最近一年使用:0次
2022-01-27更新
|
532次组卷
|
6卷引用:四川省合江县马街中学校2023-2024学年高一上学期12月月考化学试题
四川省合江县马街中学校2023-2024学年高一上学期12月月考化学试题贵州省铜仁市2021-2022学年高一上学期期末考试化学试题(已下线)2.2.3 氯气的实验室制法 氯离子的检验-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)广东省广州市育才中学2022-2023学年高一上学期期中考试化学试题广东省广州市育才中学2022-2023学年高一上学期期中考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第二单元03巩固练
3 . 下列装置能达到实验目的的是
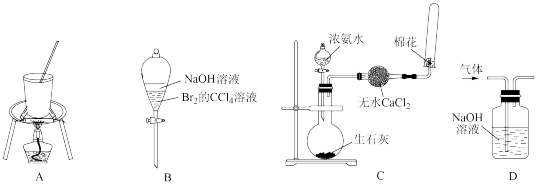

A.从盐水中提取 | B.除去 中的 中的 | C.制取收集氨 | D.除去 中的 中的 |
您最近一年使用:0次
2023-01-13更新
|
1243次组卷
|
3卷引用:四川省成都市2023届高三第一次诊断性检测理科综合化学试题
4 . 利用下列装置进行实验,不能达到相应实验目的的是


| A.利用装置①证明Cl2易被NaOH溶液吸收 |
| B.利用装置②检查装置的气密性 |
| C.利用装置③比较碳酸钠与碳酸氢钠的热稳定性 |
| D.利用装置④制取并收集干燥、纯净的NH3 |
您最近一年使用:0次
2022-04-06更新
|
117次组卷
|
2卷引用:四川省宜宾市叙州区第二中学校2022-2023学年高一上学期第三次月考试化学试题
名校
5 . 下列操作正确且能达到实验目的是
| 选项 | 实验操作 | 实验目的 |
| A | 将混合气体通过饱和的碳酸钠的洗气瓶 | 除去CO2中的HCl |
| B | 向25mL的沸水中逐滴滴加5~6滴饱和FeCl3溶液,继续加热至产生红褐色沉淀 | 制备Fe(OH)3胶体 |
| C | 将混合气体通过盛有碱石灰的干燥管 | 除去Cl2中的水蒸气 |
| D | 用棉花包裹Na2O2,放入充满CO2的集气瓶中 | 证明Na2O2与CO2反应是放热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-25更新
|
178次组卷
|
3卷引用:四川省南充市2020-2021学年高一上学期期末考试化学试题
6 . 某小组使用下图装置制取并收集干燥、纯净的氯气,请回答下列问题:
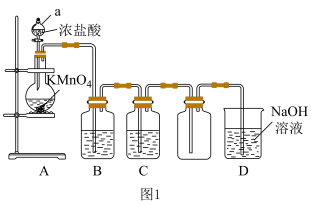
(1)①A装置中仪器a的名称是___________ ,KMnO4的作用是___________ 。
②已知KMnO4常温下即可与浓盐酸反应生成Cl2;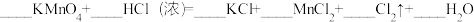 ,请配平化学方程式:
,请配平化学方程式:__________ ;其中做还原剂的HCl占参与反应的HCl的___________ (填分数)。
(2)B装置中盛放的试剂是___________ ,其作用是___________ 。D装置处理尾气时,使用NaOH溶液而不用澄清石灰水吸收氯气的原因是___________ 。若将图1收集到的氯气通入图2所示装置中,可观察到的现象为___________ 。
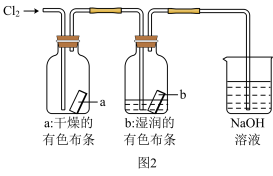
(3)查阅资料知次氯酸或氯气可被H2O2还原成Cl-,设计实验方案测定某氯水中氯元素质量:___________ 。

(1)①A装置中仪器a的名称是
②已知KMnO4常温下即可与浓盐酸反应生成Cl2;
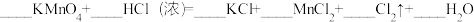 ,请配平化学方程式:
,请配平化学方程式:(2)B装置中盛放的试剂是

(3)查阅资料知次氯酸或氯气可被H2O2还原成Cl-,设计实验方案测定某氯水中氯元素质量:
您最近一年使用:0次
2023-11-06更新
|
175次组卷
|
3卷引用:四川省泸州市合江县马街中学校2023-2024学年高一上学期11月期中化学试题
23-24高三上·广东深圳·阶段练习
名校
7 . 某化学小组制取氯酸钾并进行有关探究实验。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:
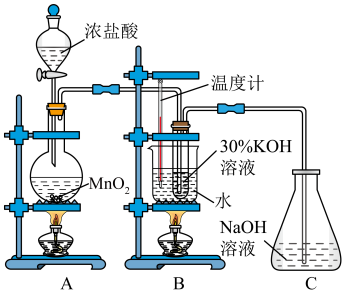
(1)装置C中盛装NaOH溶液仪器的名称是___________ 。
(2)装置A中发生反应的化学方程式为___________ 。
(3)若装置B中加热温度过低,所得主要氧化产物为___________ (填化学式)。已知氯酸钾和氯化钾的溶解度曲线如图所示,反应结束后,从装置B所得溶液中提取氯酸钾晶体的实验操作是___________ 、___________ 、过滤、干燥。

II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
①3号试管实验中x的值为___________ ;1号试管实验的作用是___________ 。
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为___________ 。
③由该系列实验可得出的结论是___________ 。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:

(1)装置C中盛装NaOH溶液仪器的名称是
(2)装置A中发生反应的化学方程式为
(3)若装置B中加热温度过低,所得主要氧化产物为

II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol·L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol·L-1H2SO4/mL | 0 | 3.0 | x | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 4.0 | 0 |
| 取少量反应后溶液滴加淀粉溶液 | 无现象 | 变蓝 | 变蓝 | 无现象 |
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为
③由该系列实验可得出的结论是
您最近一年使用:0次
8 . 氯及其化合物既是重要化工原料,又是高效、广谱消毒剂。回答下列问题:

(1)仪器Ⅰ中发生的化学反应方程式为___________ ,仪器中橡皮管的作用为___________
(2)若要利用装置Ⅱ收集纯净的 ,则需要先将装置Ⅰ中产生的气体依次通过盛装
,则需要先将装置Ⅰ中产生的气体依次通过盛装___________ (填试剂名称)、浓硫酸的洗气瓶除杂;收集 时,气体从集气瓶的
时,气体从集气瓶的___________ (选“m”或“n”)导管口进入。
(3)制得的 按照装置Ⅲ中箭头方向通入。
按照装置Ⅲ中箭头方向通入。
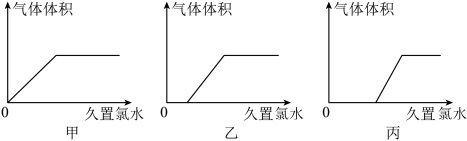
①若试剂X为水,则可制得氯水。将久置氯水滴入Na2CO3与NaHCO3的混合溶液中,以下图像能正确表示产生的气体体积与加入久置氯水的量之间的关系的是___________ (选填“甲”或“乙”或“丙”)
②若试剂X为 ,则可制得
,则可制得 的
的 溶液(
溶液( 可溶于
可溶于 ,且不与
,且不与 反应)。取稀盐酸、新制氯水、
反应)。取稀盐酸、新制氯水、 的
的 溶液,分别滴在三张红色纸条上,可观察到
溶液,分别滴在三张红色纸条上,可观察到___________ 现象,证明氯水中HClO具有漂白作用。
③若试剂X为石灰乳,则可制得漂白粉。漂白粉的有效成分为___________ ,漂白粉久置在空气中会发生变质,该过程发生反应的化学方程式为___________ 、___________ 。

(1)仪器Ⅰ中发生的化学反应方程式为
(2)若要利用装置Ⅱ收集纯净的
 ,则需要先将装置Ⅰ中产生的气体依次通过盛装
,则需要先将装置Ⅰ中产生的气体依次通过盛装 时,气体从集气瓶的
时,气体从集气瓶的(3)制得的
 按照装置Ⅲ中箭头方向通入。
按照装置Ⅲ中箭头方向通入。①若试剂X为水,则可制得氯水。将久置氯水滴入Na2CO3与NaHCO3的混合溶液中,以下图像能正确表示产生的气体体积与加入久置氯水的量之间的关系的是

②若试剂X为
 ,则可制得
,则可制得 的
的 溶液(
溶液( 可溶于
可溶于 ,且不与
,且不与 反应)。取稀盐酸、新制氯水、
反应)。取稀盐酸、新制氯水、 的
的 溶液,分别滴在三张红色纸条上,可观察到
溶液,分别滴在三张红色纸条上,可观察到③若试剂X为石灰乳,则可制得漂白粉。漂白粉的有效成分为
您最近一年使用:0次
9 . “绿色化学”走进课堂,某学习小组在老师的指导下,设计了“氯气与金属钠反应”的实验。实验操作:钠与氯气反应的装置可作如图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大小的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔化成小球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述错误的是
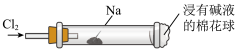

| A.浸有NaOH溶液的棉球主要用于防止空气中二氧化碳进来与钠反应 |
| B.反应生成的大量白烟是氯化钠晶体 |
| C.从实验现象上判断钠的熔点较低 |
| D.钠性质非常活泼,本质原因是钠原子的最外层只有1个电子,该电子很容易失去 |
您最近一年使用:0次
2023-03-22更新
|
191次组卷
|
2卷引用:四川省遂宁中学校2023-2024学年高一上学期期中(半期)考试化学试题
10 . 实验室里可用如下图所示的装置制取氯酸钾、次氯酸钠,并验证氯水的性质。

图中a为氯气发生装置,c的试管中盛有15mL30%的 溶液,并置于热水浴中,d的试管中盛有15mL 8%的
溶液,并置于热水浴中,d的试管中盛有15mL 8%的 溶液,并置于冰水浴中,f为
溶液,并置于冰水浴中,f为 的发生装置。
的发生装置。
(1)制取氯气时,在烧瓶中先加入一定量的 固体,再通过
固体,再通过___________ (填写仪器名称)向烧瓶中加入适量的浓盐酸。
(2)装置b的作用是___________ 。
(3)f装置中反应的化学方程式为___________ 。
(4)比较制取氯酸钾和次氯酸钠的条件,两者的差异是___________ 。
(5)反应完毕经冷却后,c装置的试管中有大量晶体析出,图中符合该晶体溶解度随温度变化规律的曲线是___________ (选填字母);从c装置的试管中分离该晶体的操作是___________ (填写实验操作名称)。

(6)将d中余气与f中产生的气体通入e中,产生的现象为___________ 。
(7)该实验有一处明显的缺点是___________ 。

图中a为氯气发生装置,c的试管中盛有15mL30%的
 溶液,并置于热水浴中,d的试管中盛有15mL 8%的
溶液,并置于热水浴中,d的试管中盛有15mL 8%的 溶液,并置于冰水浴中,f为
溶液,并置于冰水浴中,f为 的发生装置。
的发生装置。(1)制取氯气时,在烧瓶中先加入一定量的
 固体,再通过
固体,再通过(2)装置b的作用是
(3)f装置中反应的化学方程式为
(4)比较制取氯酸钾和次氯酸钠的条件,两者的差异是
(5)反应完毕经冷却后,c装置的试管中有大量晶体析出,图中符合该晶体溶解度随温度变化规律的曲线是

(6)将d中余气与f中产生的气体通入e中,产生的现象为
(7)该实验有一处明显的缺点是
您最近一年使用:0次
2022-01-23更新
|
202次组卷
|
2卷引用:四川省泸县第四中学2022-2023学年高一上学期第三次月考化学试题



