名校
解题方法
1 . 如图为钠和氯的价类二维图,请据图完成下列问题:
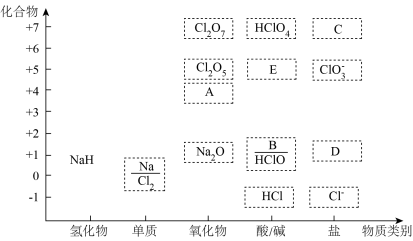
(1)NaH中的氢为___________ 价。可与水反应生成氢气,该反应中氧化产物和还原产物的质量比为___________ 。
(2)A是氯的氧化物,其化学式为___________ 。A可用于自来水消毒。其消毒效率是 的
的___________ 倍(还原产物都是 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。
(3)B属于碱,其水溶液与 反应生成D的离子方程式为
反应生成D的离子方程式为___________ 。
(4)C是高氯酸钠,受热分解可产生 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为___________ 。
(5) 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式___________ 。

(1)NaH中的氢为
(2)A是氯的氧化物,其化学式为
 的
的 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。(3)B属于碱,其水溶液与
 反应生成D的离子方程式为
反应生成D的离子方程式为(4)C是高氯酸钠,受热分解可产生
 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为(5)
 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式
您最近一年使用:0次
名校
2 . Cl2是一种重整的化工原料,在生产、生活和工业上均有很多用途。
(1)可与氢气化合制得盐酸。化学方程式为________________ 。
(2)可与NaOH溶液反应制得漂白液(84消毒液),离子方程式为_______________ 。
(3)可用于工业上制得高锰酸钾(KMnO4),KMnO4中Mn的化合价为_______________ 。其工业制备的部分工艺如下:
Ⅰ.将软锰矿(主要成分为MnO2)粉碎后,与KOH固体混合,通入氯气充分焙烧,生成暗绿色熔融态物质。
Ⅱ.冷却,将固体研细,用稀KOH溶液慢取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料: K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液源中易发生歧化反应(Mn的化合价既升高又降低)。
①Ⅰ中,粉碎软锰矿的目的是_____________ 。
②Ⅰ中,生成K2MnO4的化学方程式是____________ 。
③Ⅱ中,浸取时用稀KOH溶液的原因是_____________ 。
④Ⅲ中,CO2和K2MnO4在溶液中反应的离子方程式是:MnO +CO2 +H2O→MnO
+CO2 +H2O→MnO +MnO2 +HCO
+MnO2 +HCO (未配平),氧化产物和还原产物的物质的量之比为
(未配平),氧化产物和还原产物的物质的量之比为____________ 。
(1)可与氢气化合制得盐酸。化学方程式为
(2)可与NaOH溶液反应制得漂白液(84消毒液),离子方程式为
(3)可用于工业上制得高锰酸钾(KMnO4),KMnO4中Mn的化合价为
Ⅰ.将软锰矿(主要成分为MnO2)粉碎后,与KOH固体混合,通入氯气充分焙烧,生成暗绿色熔融态物质。
Ⅱ.冷却,将固体研细,用稀KOH溶液慢取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料: K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液源中易发生歧化反应(Mn的化合价既升高又降低)。
①Ⅰ中,粉碎软锰矿的目的是
②Ⅰ中,生成K2MnO4的化学方程式是
③Ⅱ中,浸取时用稀KOH溶液的原因是
④Ⅲ中,CO2和K2MnO4在溶液中反应的离子方程式是:MnO
 +CO2 +H2O→MnO
+CO2 +H2O→MnO +MnO2 +HCO
+MnO2 +HCO (未配平),氧化产物和还原产物的物质的量之比为
(未配平),氧化产物和还原产物的物质的量之比为
您最近一年使用:0次
名校
解题方法
3 . 完成下列问题。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是___________ (填化学式);用少量氯气消毒的自来水养金鱼时,通常需要先将自来水晒一晒,其原因是___________ (用化学方程式表示)。
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是___________ ;漂白粉也能用于消毒,其有效成分生效的化学方程是___________ 。
(1)氯气可直接用于自来水的消毒,氯气通入水中可用来杀菌消毒,其中杀菌消毒的物质是
(2)氯气可用来制取漂白粉,但干燥的氢氧化钙与氯气并不易发生反应,氯气只能被氢氧化钙所吸附。为此,在工业上采用加入少许水的消石灰来进行氯化,其原因是
您最近一年使用:0次
4 . 回答下列问题
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:_________________________ 。
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:__________________________ 。
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:__________________________ 。
(2)海水开发利用的部分过程如图所示:
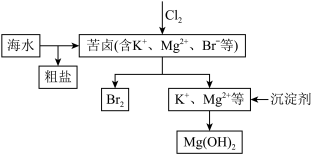
④向苦卤中通入氯气,发生反应的离子方程式是_____________________________________
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是______________________
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是_______ 。
(1)化学与生产生活联系密切,请书写对应的化学方程式:
①漂白粉中的
 能与空气中的
能与空气中的 和水蒸气发生反应:
和水蒸气发生反应:②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:
③常温下,将氯气通入氢氧化钠溶液中,可以得到一种漂白液:
(2)海水开发利用的部分过程如图所示:

④向苦卤中通入氯气,发生反应的离子方程式是
⑤工业生产中常选用石灰乳作为沉淀剂,相关反应的离子方程式是
⑥富集溴一般先用空气和水蒸气吹出单质溴,再用
 将其还原吸收,相关反应的化学方程式是
将其还原吸收,相关反应的化学方程式是
您最近一年使用:0次
解题方法
5 . 钠、氯及其化合物有如图转化关系,淡黄色物质M可在潜水艇中作为氧气的来源,常被用作供氧剂,N常用来杀菌消毒。请按要求填空:
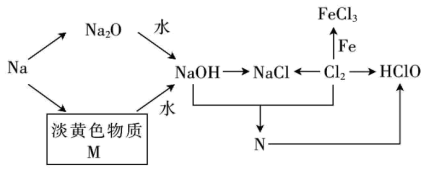
(1)淡黄色物质M是____ ,物质N是____ 。(填化学式)
(2)请描述一小块金属钠投入加酚酞的水中的现象:____ 。相关化学方程式为____ 。
(3)用化学方程式说明为什么M能够作为潜水艇中的供氧剂使用____ 。

(1)淡黄色物质M是
(2)请描述一小块金属钠投入加酚酞的水中的现象:
(3)用化学方程式说明为什么M能够作为潜水艇中的供氧剂使用
您最近一年使用:0次
2022-09-27更新
|
204次组卷
|
2卷引用:新疆乌鲁木齐市第三十一中学2021-2022学年高一上学期期中考试化学试题
名校
解题方法
6 . 按要求书写方程式
(1)NaHSO4在熔融状态的电离方程式___________
(2)碳酸钙溶解在醋酸中的离子反应方程式___________
(3)将“ ”改写为对应的化学方程式
”改写为对应的化学方程式___________
(4)除去Na2CO3粉末中混有少量NaHCO3的化学方程式___________
(5)氯气与烧碱溶液反应的化学方程式为___________
(6)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是___________
(7)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的 ,配平该反应的离子方程式:
,配平该反应的离子方程式:___________
_______MnO +_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
+_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
(1)NaHSO4在熔融状态的电离方程式
(2)碳酸钙溶解在醋酸中的离子反应方程式
(3)将“
 ”改写为对应的化学方程式
”改写为对应的化学方程式(4)除去Na2CO3粉末中混有少量NaHCO3的化学方程式
(5)氯气与烧碱溶液反应的化学方程式为
(6)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是
(7)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的
 ,配平该反应的离子方程式:
,配平该反应的离子方程式:_______MnO
 +_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
+_______H2C2O4+_______H+=_______CO2↑+_______Mn2++______H2O
您最近一年使用:0次
名校
7 .  和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯
和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯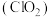 气体,该反应的化学方程式为
气体,该反应的化学方程式为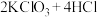 (浓)
(浓) 。
。
(1)该反应的氧化剂是___________ 还原产物是___________ (化学式)。氧化性
___________  (填< > =)。
(填< > =)。
(2)用双线桥在方程式中标出电子转移的情况:___________
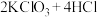 (浓)
(浓) 。
。
(3)以上反应中盐酸具有的性质是___________(填序号)。
(4)当发生二氧化氯泄漏和爆炸事故,人们逃离爆炸现场时,可用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的物质是___________(填序号)。
 和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯
和浓盐酸在一定温度下反应,会生成橙黄色的易爆物二氧化氯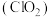 气体,该反应的化学方程式为
气体,该反应的化学方程式为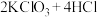 (浓)
(浓) 。
。(1)该反应的氧化剂是

 (填< > =)。
(填< > =)。(2)用双线桥在方程式中标出电子转移的情况:
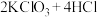 (浓)
(浓) 。
。(3)以上反应中盐酸具有的性质是___________(填序号)。
| A.只有还原性 | B.只有氧化性 |
| C.还原性和酸性 | D.氧化性和还原性,还有酸性 |
| A.NaOH | B.NaCl | C.KCl | D. |
您最近一年使用:0次
2021-10-22更新
|
415次组卷
|
2卷引用:黑龙江省哈尔滨市第六中学2021-2022学年高一上学期10月月考化学试题
名校
8 . 2020年突如其来的“新冠病毒”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉、二氧化氯都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是“84“消毒液,可以说化学让生活更美好。
图为“84”消毒液说明书。
请回答下列问题。
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按56.8g/L计算,该消毒液的NaClO的物质的量浓度是_______ 。
(2)常温下用石灰乳吸收Cl2制备漂白粉。写出该反应的化学方程式_______ , 若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO 和NaClO3的混合液。当混合液中Cl-和 的个数比为13 :2时,混合液中ClO-和
的个数比为13 :2时,混合液中ClO-和 的个数比为
的个数比为_______ 。
(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
(4)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业制备ClO2的反应为:2NaClO3 +4HCl =2ClO2↑+Cl2↑+2H2O+2NaCl
①用双线桥表示电子转移的方向和数目_______ 。
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐( ),需将其转化为C1-除去,下列试剂中可将
),需将其转化为C1-除去,下列试剂中可将 转化为C1-的是
转化为C1-的是_______ (填字母)。
a. O3 b. FeSO4 c. KI d. KMnO4
③工业上还可以利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为: +FeS2+H+
+FeS2+H+ 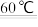 ClO2+Fe3++
ClO2+Fe3++  +H2O(未配平),请配平以上反应方程式
+H2O(未配平),请配平以上反应方程式_______ 。
图为“84”消毒液说明书。
 说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~ 60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物,浴缸等1: 200水溶液餐饮具,瓜果等1: 100 水溶液 |
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按56.8g/L计算,该消毒液的NaClO的物质的量浓度是
(2)常温下用石灰乳吸收Cl2制备漂白粉。写出该反应的化学方程式
 的个数比为13 :2时,混合液中ClO-和
的个数比为13 :2时,混合液中ClO-和 的个数比为
的个数比为(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
(4)二氧化氯(ClO2)被联合国世界卫生组织列为A1级高效安全灭菌消毒剂。工业制备ClO2的反应为:2NaClO3 +4HCl =2ClO2↑+Cl2↑+2H2O+2NaCl
①用双线桥表示电子转移的方向和数目
②ClO2在杀菌消毒过程中会产生少量副产物亚氯酸盐(
 ),需将其转化为C1-除去,下列试剂中可将
),需将其转化为C1-除去,下列试剂中可将 转化为C1-的是
转化为C1-的是a. O3 b. FeSO4 c. KI d. KMnO4
③工业上还可以利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。制备的离子方程式为:
 +FeS2+H+
+FeS2+H+ 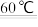 ClO2+Fe3++
ClO2+Fe3++  +H2O(未配平),请配平以上反应方程式
+H2O(未配平),请配平以上反应方程式
您最近一年使用:0次
名校
解题方法
9 . 按要求书写化学方程式或离子方程式。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为___________ 。
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为___________ 。
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为___________ 。
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的离子 方程式为___________ 。
(5)SO2能使氯水褪色,相应的离子 方程式为___________ 。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的
(5)SO2能使氯水褪色,相应的
您最近一年使用:0次
10 . 资料:“84”消毒液中含氯微粒主要有ClO-、Cl-、HClO,相同浓度时,HClO的氧化性强于ClO-。通常情况下,应将“84”消毒液原液稀释后使用,一般不用于衣服等纺织品的洗涤消毒。
(1)常温,将氯气通入NaOH溶液中可制得“84”消毒液,该反应的化学方程式为_______ 。
(2)已知某“84”消毒液瓶体部分标签如图所示,请回答下列问题。
①该“84”消毒液的物质的量浓度为_______ mol/L。
②“84”消毒液使用时需要稀释,某小组用上述“84”消毒液配制500 mL 0.2mol/L的稀溶液,需要用量筒量取该“84”消毒液体积为_______ mL。
③配制过程中,下列操作会造成新配制的稀溶液浓度偏低的是_______ 。
A.容量瓶使用时未干燥 B.没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线 D.定容后液面低于刻度线,再加蒸馏水至刻度线
(3)为研究“84”消毒液的性质与使用条件,进行下列实验:
向三支试管中分别加入2 mL“84”消毒液和5滴紫色石蕊。继续进行如下实验:
①实验1中NaClO溶液与空气中二氧化碳反应的离子方程式为_______ 。(已知酸性: )
)
②实验3中生成气体的离子方程式为_______ 。
③综合以上实验为提高单位时间内“84”消毒液的漂白效果,你的建议是_______ 。
(1)常温,将氯气通入NaOH溶液中可制得“84”消毒液,该反应的化学方程式为
(2)已知某“84”消毒液瓶体部分标签如图所示,请回答下列问题。
| “84”消毒液 有效成分:NaClO 规格:1000 mL 质量分数:25% 密度:1.192g/cm3 |
②“84”消毒液使用时需要稀释,某小组用上述“84”消毒液配制500 mL 0.2mol/L的稀溶液,需要用量筒量取该“84”消毒液体积为
③配制过程中,下列操作会造成新配制的稀溶液浓度偏低的是
A.容量瓶使用时未干燥 B.没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线 D.定容后液面低于刻度线,再加蒸馏水至刻度线
(3)为研究“84”消毒液的性质与使用条件,进行下列实验:
向三支试管中分别加入2 mL“84”消毒液和5滴紫色石蕊。继续进行如下实验:
| 实验 | 操作 | 现象 |
| 实验1 | 加入2 mL蒸馏水 | 短时间内未褪色,一段时间后蓝色褪去 |
| 实验2 | 加入2 mL 0.0002 mol/L的H2SO4溶液 | 蓝色迅速褪去,无气体产生 |
| 实验3 | 加入2 mL 2 mol/L的H2SO4溶液 | 蓝色迅速褪去,并产生大量刺激性的气体 |
 )
)②实验3中生成气体的离子方程式为
③综合以上实验为提高单位时间内“84”消毒液的漂白效果,你的建议是
您最近一年使用:0次



