解题方法
1 . 回答下列问题
(1)H2在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸,其反应的化学方程式为_______ 。
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶甲和盛有潮湿有色布条的广口瓶乙,可观察到的现象是_______ ,这是因为氯气通入水中发生化学反应,生成了具有漂白性的物质:_______ (填化学式),化学方程式为_______ 。
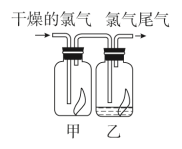
(3)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用_______ 溶液吸收多余的氯气,原理是_______ (用化学方程式表示)。
(4)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是_______ (填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体主要是_______ (用字母代号填)。
A.O2 B.Cl2 C.CO2 D.HClO
(1)H2在单质B中燃烧产生苍白色的火焰,产物溶于水得到常见的强酸,其反应的化学方程式为
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶甲和盛有潮湿有色布条的广口瓶乙,可观察到的现象是

(3)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用
(4)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是
A.O2 B.Cl2 C.CO2 D.HClO
您最近一年使用:0次
2 . Ⅰ.NaClO是“84”消毒液的有效成分。请回答下列问题:
(1)NaClO中Cl元素的化合价是_______ 。
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:_______ 。(已知酸性: )
)
(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
Ⅱ. 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。
(4)已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为_______ 。
(5)喷射石灰乳等碱性物质可以减轻少量 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是_______ 。
(1)NaClO中Cl元素的化合价是
(2)浸泡衣物时加入“84”消毒液,在空气中放置一段时间后漂白效果更好,结合离子方程式解释原因:
 )
)(3)若将“84”消毒液与洁厕灵(主要成分是HCl)混合使用,会产生黄绿色的有毒气体,其反应的离子方程式是
Ⅱ.
 是一种有毒气体,如果泄漏会造成严重的危害。
是一种有毒气体,如果泄漏会造成严重的危害。(4)已知
 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。该反应中被氧化和未被氧化的
是否泄漏。该反应中被氧化和未被氧化的 分子的个数比为
分子的个数比为(5)喷射石灰乳等碱性物质可以减轻少量
 泄漏造成的危害。
泄漏造成的危害。 和石灰乳反应的化学方程式是
和石灰乳反应的化学方程式是
您最近一年使用:0次
解题方法
3 . 氯气是一种非常重要的化工原料,可用于制造盐酸、漂白剂、农药等,但氯气有毒,使用或接触到有关物质时应注意安全。请回答下列问题:
(1)新制氯水中,含有氯元素的微粒有___________ (填微粒符号,下同,不考虑水中杂质与氯气的反应),其中使新制氯水显淡黄绿色的微粒是___________ 。
(2) 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为___________ L。
(3)标准状况下,氯气的密度为___________ 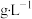 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是___________ (填序号)。
a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为___________ ;通常不用澄清石灰水吸收氯气的原因是___________ 。
(1)新制氯水中,含有氯元素的微粒有
(2)
 和
和 可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中
可用于生产农药、催化剂等。31g红磷在一定量的氯气中燃烧,红磷和氯气均完全反应,生成白色烟雾,其中 和
和 的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为
的物质的量之比为3:2,则消耗的氯气在标准状况下的体积为(3)标准状况下,氯气的密度为
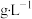 (结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是
(结果保留两位小数),比空气的密度大。某地施工时挖破了废弃自来水厂的储氯罐,导致氯气泄漏。当地居民逃生和自救的正确做法是a.逆风往高处跑 b.顺风往低处跑
c.用蘸有肥皂水的毛巾捂住口鼻 d.戴上用浓NaOH溶液处理过的口罩
(4)实验室制氯气时,要用NaOH溶液吸收尾气,反应的化学方程式为
您最近一年使用:0次
解题方法
4 . 生产生活中常用的干燥剂、净水剂有:
①固体氢氧化钠,②变色硅胶(主要成分是二氧化硅,添加少量的无水CoCl2作指示剂),③P2O5(五氧化二磷),④氯化钙,⑤浓硫酸,⑥碱石灰(主要成分是氢氧化钠、氧化钙),⑦明矾,⑧Fe(OH)3胶体。
(1)上述物质中,属于电解质的是_______ 。
(2)下列气体中,能用碱石灰干燥的是_______ 。
a.CO2 b.HCl c.H2 d.Cl2
(3)固体氢氧化钠不能干燥CO2,原因为_______ (用化学方程式表示)。
(4)往胶粒带有正电荷的Fe(OH)3胶体中加入电解质能使胶体凝聚。使一定量的胶体在一定时间内开始凝聚所需电解质的浓度(mmol·L-1),称作“聚沉值”,电解质的“聚沉值”越小,则表示其凝聚能力_______ (填“越强”或“越弱”),实验证明,凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,凝聚能力越强,则向Fe(OH)3胶体中加入下列电解质时,其“聚沉值”最小的为_______ 。
a.NaCl b.MgCl2 c.K2SO4 d.Na3PO4
①固体氢氧化钠,②变色硅胶(主要成分是二氧化硅,添加少量的无水CoCl2作指示剂),③P2O5(五氧化二磷),④氯化钙,⑤浓硫酸,⑥碱石灰(主要成分是氢氧化钠、氧化钙),⑦明矾,⑧Fe(OH)3胶体。
(1)上述物质中,属于电解质的是
(2)下列气体中,能用碱石灰干燥的是
a.CO2 b.HCl c.H2 d.Cl2
(3)固体氢氧化钠不能干燥CO2,原因为
(4)往胶粒带有正电荷的Fe(OH)3胶体中加入电解质能使胶体凝聚。使一定量的胶体在一定时间内开始凝聚所需电解质的浓度(mmol·L-1),称作“聚沉值”,电解质的“聚沉值”越小,则表示其凝聚能力
a.NaCl b.MgCl2 c.K2SO4 d.Na3PO4
您最近一年使用:0次
解题方法
5 . 回答下列问题:
(1)实验室需要用NaOH配制0.2mol/LNaOH溶液450mL。
①完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、胶头滴管、____ 。
②配制该溶液需称取NaOH____ g。
③称量完毕,将药品倒入烧杯中,溶解、冷却,转移、洗涤。
(2)取上述配制的NaOH溶液200mL制取消毒液:向该NaOH溶液通入Cl2,使得NaOH恰好完全反应。完成下列填空。
①该消毒液制备的化学方程式为____ ,该反应消耗的Cl2在标准状况下的体积为____ 。
②该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。若将二者混合,每产生1molCl2,转移电子个数约为____ 。
(1)实验室需要用NaOH配制0.2mol/LNaOH溶液450mL。
①完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、胶头滴管、
②配制该溶液需称取NaOH
③称量完毕,将药品倒入烧杯中,溶解、冷却,转移、洗涤。
(2)取上述配制的NaOH溶液200mL制取消毒液:向该NaOH溶液通入Cl2,使得NaOH恰好完全反应。完成下列填空。
①该消毒液制备的化学方程式为
②该消毒液不能与洁厕灵(主要成分为浓盐酸)混用,否则会产生中毒危险。若将二者混合,每产生1molCl2,转移电子个数约为
您最近一年使用:0次
6 . 氯气是一种化学性质活泼的气体。
(1)氯气是一种具有_______ 气味的气体,密度比空气的_______ (填“大”或“小”),若采用如图装置收集氯气,则氯气应由_______ 管(填“A”或“B”)通入。
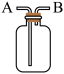
(2)氯气与NaOH溶液反应的化学方程式为_______ ,该反应可用于工业上制取漂白液,其有效成分是_______ 。
(1)氯气是一种具有

(2)氯气与NaOH溶液反应的化学方程式为
您最近一年使用:0次
7 . 12月23日凌晨,陕西省西安市下辖村、社区实行封闭式管理,“84消毒液”能有效杀灭新冠肺炎病毒,可用于物品表面的杀菌消毒。小铭同学购买了一瓶“84消毒液”,该消毒液通常稀释到100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如图信息:

(1)该“84消毒液”NaClO物质的量浓度约为____ (保留1位小数)。
(2)工业上可用Cl2与浓氢氧化钠溶液反应制取“84消毒液”,请写出反应的化学方程式____ 。
(3)一瓶上述“84消毒液”理论上能吸收空气中____ L的CO2(标准状况下)而变质。(已知:CO2+NaClO+H2O=NaHCO3+HClO)
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因____ ,某消毒小组人员用18.4mol•L-1的浓硫酸配制500mL2.3mol•L-1的稀硫酸用于增强“84消毒液”的消毒能力,需取用浓硫酸的体积为____ mL。

(1)该“84消毒液”NaClO物质的量浓度约为
(2)工业上可用Cl2与浓氢氧化钠溶液反应制取“84消毒液”,请写出反应的化学方程式
(3)一瓶上述“84消毒液”理论上能吸收空气中
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因
您最近一年使用:0次
2022-09-13更新
|
140次组卷
|
2卷引用:湖北省襄阳市第三中学2022-2023学年高一上学期12月月考化学试题
8 . 含氯化合物在日常生活中有多种用途,根据要求完成下列问题:
(1)漂白粉的有效成分是___________ ,家庭中使用漂白粉加水配置消毒液,与空气发生反应的化学方程式为___________ 。
(2)84消毒液的有效成分中NaClO中Cl的化合价为___________ ,请写出氯气与NaOH反应的化学方程式:___________ 。向NaOH溶液中通入11.2L(标准状况)氯气恰好完全反应生成三种含氯盐:0.7molNaCl、0.2molNaClO和X。则X是___________ 。
a.0.1molNaClO4 b.0.1molNaClO3 c.0.2molNaClO2 d.0.1molNaClO2
(3)日常生活中84消毒液若与洁厕灵(较浓的盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2+H2O,该反应的氧化剂为___________ ,被氧化的物质为___________ 。若反应中电子转移为2mol,生成的氯气为___________ mol。
(1)漂白粉的有效成分是
(2)84消毒液的有效成分中NaClO中Cl的化合价为
a.0.1molNaClO4 b.0.1molNaClO3 c.0.2molNaClO2 d.0.1molNaClO2
(3)日常生活中84消毒液若与洁厕灵(较浓的盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2+H2O,该反应的氧化剂为
您最近一年使用:0次
名校
9 . 化学与人类生活密切相关。请按要求,回答下列问题:
(1)氯气是重要的化工原料,实验室常用2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应制备氯气,该反应的氧化剂是_______ ;当生成的气体在标准状况下的体积为5.6L时转移的电子数约为_______ 个,此时被氧化的物质为_______ mol。
(2)。“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为_______ ,若有2mol氯气参与该反应,则此时转移的电子数为_______ NA。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为_______ 。
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为_______ 。
(5)葡萄糖(分子式C6H12O6)是人体活细胞的能量来源。已知1mol等于1000mmol,某体检单的一些指标如图,则每升该样品中含葡萄糖的质量为_______ g(请保留两位小数)。
(1)氯气是重要的化工原料,实验室常用2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O反应制备氯气,该反应的氧化剂是
(2)。“84”消毒液在生活中使用广泛,其有效成分是次氯酸钠。可在常温下将氯气通入NaOH溶液制得,该反应的离子方程式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
(4)长石是地表岩石最重要的造岩矿物。某种长石的化学组成KAlSi3O8则将其改写成氧化物的组合形式为
(5)葡萄糖(分子式C6H12O6)是人体活细胞的能量来源。已知1mol等于1000mmol,某体检单的一些指标如图,则每升该样品中含葡萄糖的质量为
| 9 | 白球比 | 1.6 | |
| 10 | 乳酸脱氢酶 | 161 | U/L |
| 11 | 磷酸肌酸激酶 | 56 | U/L |
| 12 | 甘油三酯 | 0.52 | mmol/L |
| 13 | 总胆固醇 | 4.27 | mmol/L |
| 14 | 高密度脂蛋白胆固醇 | 1.57 | mmol/L |
| 15 | 低密度脂蛋白胆固醇 | 1.40 | mmol/L |
| 16 | 葡萄糖 | 4.94 | mmol/L |
您最近一年使用:0次
10 . 如图所示是某学生设计的实验室制备干燥Cl2及吸收多余Cl2的实验装置图,根据图中的装置和有关试剂回答下列问题。
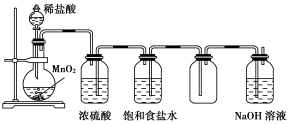
(1)指出图中的各处错误:
①____ ;
②____ ;
③____ ;
④____ 。
(2)在改过后的装置中,写出下列物质的作用:
①饱和食盐水____ ;
②浓硫酸____ ;
③NaOH溶液____ 。
(3)在改正过的装置中,制取氯气所发生反应的离子方程式:____ ,用NaOH溶液吸收多余尾气的离子方程式:____ 。

(1)指出图中的各处错误:
①
②
③
④
(2)在改过后的装置中,写出下列物质的作用:
①饱和食盐水
②浓硫酸
③NaOH溶液
(3)在改正过的装置中,制取氯气所发生反应的离子方程式:
您最近一年使用:0次



