2021高三·全国·专题练习
名校
解题方法
1 . 现有NaCl、Na2CO3·10H2O和NaHCO3三种固体组成的混合物,为了测定各组分的含量,设计如下实验,取一定质量的样品,测量反应前后②和③装置质量的变化,可以计算出各组分的含量。

(1)U形管①中装有碱石灰,作用是_______ ;
(2)U形管②的作用是_______ ;U形管③中装有_______ ;
(3)球形干燥管中盛装碱石灰的作用是_______ ,若取消球形干燥管,则会使_______ 的质量分数偏高。
(4)若将U形管①换成装有NaOH溶液的洗气瓶,则会使测得的NaCl的含量_______ (填“偏高、偏低、无影响”)。
(5)硬质玻璃管在加热前,应关闭_______ (填 a 或 b,下同),打开_______ ,再_______ ,至排出的气体不再使澄清石灰水变浑浊。
(6)若实验结束后,装置②增加5.4g,装置③增加8.8g,则可计算原混合物中Na2CO3·10H2O的质量为_______ g 。

(1)U形管①中装有碱石灰,作用是
(2)U形管②的作用是
(3)球形干燥管中盛装碱石灰的作用是
(4)若将U形管①换成装有NaOH溶液的洗气瓶,则会使测得的NaCl的含量
(5)硬质玻璃管在加热前,应关闭
(6)若实验结束后,装置②增加5.4g,装置③增加8.8g,则可计算原混合物中Na2CO3·10H2O的质量为
您最近一年使用:0次
2021-12-22更新
|
856次组卷
|
3卷引用:专题03 定量计算-【微专题·大素养】备战2022年高考化学核心突破(实验综合大题)
(已下线)专题03 定量计算-【微专题·大素养】备战2022年高考化学核心突破(实验综合大题)福建省莆田第四中学2021-2022学年高一上学期期末考试化学试题福建省福州外国语学校2022-2023学年高一上学期12月期中考试化学试题
名校
2 . 某纯碱样品只含NaCl杂质,为测定样品中 的含量进行如下实验。
的含量进行如下实验。
实验Ⅰ:甲小组称取样品5.00g,采用如下实验装置进行实验。实验结束时,分离③中所得固体,称其质量为7.88g。

(1)装置①的作用是___________ 。
(2)装置②中反应的离子方程式为___________ 。
(3)下列说法不正确的是___________(填标号)。
(4)样品中 的质量分数为
的质量分数为____ 。
实验Ⅱ:乙小组称取样品ag,采用如图实验装置进行实验。
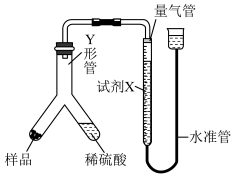
(5)试剂X应选择____ (填标号)。
A.饱和 溶液 B.饱和
溶液 B.饱和 溶液 C.饱和
溶液 C.饱和 溶液
溶液
(6)下列哪些因素会造成样品中 的含量偏低
的含量偏低___ (填标号)。
A.将稀硫酸替换为盐酸
B.读数时未冷却至室温
C.读数时水准管的液面高于量气管的液面
(7)实验结束时,所得气体体积为V mL。实验时的气体摩尔体积为 ,则样品
,则样品 的质量分数为
的质量分数为______ 。
 的含量进行如下实验。
的含量进行如下实验。实验Ⅰ:甲小组称取样品5.00g,采用如下实验装置进行实验。实验结束时,分离③中所得固体,称其质量为7.88g。

(1)装置①的作用是
(2)装置②中反应的离子方程式为
(3)下列说法不正确的是___________(填标号)。
| A.先通入空气一段时间,再滴加盐酸 |
| B.装置②、③间应增加除去HCl杂质的装置 |
| C.装置④的作用是吸收尾气,防止空气污染 |
| D.停止滴加盐酸后,还需继续通入空气一段时间 |
 的质量分数为
的质量分数为实验Ⅱ:乙小组称取样品ag,采用如图实验装置进行实验。

(5)试剂X应选择
A.饱和
 溶液 B.饱和
溶液 B.饱和 溶液 C.饱和
溶液 C.饱和 溶液
溶液(6)下列哪些因素会造成样品中
 的含量偏低
的含量偏低A.将稀硫酸替换为盐酸
B.读数时未冷却至室温
C.读数时水准管的液面高于量气管的液面
(7)实验结束时,所得气体体积为V mL。实验时的气体摩尔体积为
 ,则样品
,则样品 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
3 . 化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟侯氏制碱法制备NaHCO3,进一步处理得到产品Na2CO3和NH4Cl,并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I. Na2CO3的制备:实验流程如图:

步骤II.产品中NaHCO3含量测定
①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴酚酞,用0.1000mol·L-1盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸V1mL;
③在上述锥形瓶中再加入2滴指示剂甲基橙,继续用0.1000mol·L-1盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸V2mL;
④平行测定三次,V1平均值为22.45,V2平均值为23.51。
回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO3(考虑充分利用CO2),正确的连接顺序是______ (按气流方向,用小写字母表示)。
A. B.
B. C.
C. D.
D. E.
E.
(2)B中使用雾化装置的优点是___________ 。
(3)生成NaHCO3的总反应的化学方程式为___________ 。
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液。向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)=NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为___________ 、___________ 、过滤、洗涤、干燥。

(5)根据步骤II,产品中NaHCO3的质量分数为___________ (保留三位有效数字);
(6)第一滴定终点时,某同学俯视读数,其他操作均正确,则NaHCO3质量分数的计算结果___________ (填“偏大”“偏小”或“无影响”)。
步骤I. Na2CO3的制备:实验流程如图:

步骤II.产品中NaHCO3含量测定
①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴酚酞,用0.1000mol·L-1盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸V1mL;
③在上述锥形瓶中再加入2滴指示剂甲基橙,继续用0.1000mol·L-1盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸V2mL;
④平行测定三次,V1平均值为22.45,V2平均值为23.51。
回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO3(考虑充分利用CO2),正确的连接顺序是
A.
 B.
B. C.
C. D.
D. E.
E.
(2)B中使用雾化装置的优点是
(3)生成NaHCO3的总反应的化学方程式为
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液。向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)=NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为

(5)根据步骤II,产品中NaHCO3的质量分数为
(6)第一滴定终点时,某同学俯视读数,其他操作均正确,则NaHCO3质量分数的计算结果
您最近一年使用:0次
名校
4 . 现有NaCl、Na2CO3·10H2O和NaHCO3三种固体组成的混合物,为了测定各组分的含量,设计如下实验,取一定质量的样品,测量反应前后②和③装置质量的变化,可以计算出各组分的含量。

(1)U形管①中装有碱石灰,作用是___________ ;
(2)U形管②的作用是___________ ;U形管③中装有___________ ;
(3)球形干燥管中盛装碱石灰的作用是___________ ,若取消球形干燥管,则会使___________ 的质量分数偏高。
(4)若将U形管①换成装有NaOH溶液的洗气瓶,则会使测得的NaCl的含量___________ (填“偏高、偏低、无影响”)。
(5)硬质玻璃管在加热前,应关闭___________ (填 a 或 b,下同),打开___________ ,再___________ ,至排出的气体不再使澄清石灰水变浑浊。
(6)写出 NaHCO3 受热分解的反应式______
(7)若实验结束后,装置②增加5.4g,装置③增加8.8g,则可计算原混合物中Na2CO3·10H2O的质量为___________ g 。

(1)U形管①中装有碱石灰,作用是
(2)U形管②的作用是
(3)球形干燥管中盛装碱石灰的作用是
(4)若将U形管①换成装有NaOH溶液的洗气瓶,则会使测得的NaCl的含量
(5)硬质玻璃管在加热前,应关闭
(6)写出 NaHCO3 受热分解的反应式
(7)若实验结束后,装置②增加5.4g,装置③增加8.8g,则可计算原混合物中Na2CO3·10H2O的质量为
您最近一年使用:0次
名校
5 . 大苏打 、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
(1)工业上,将 和
和 以
以 的物质的量之比配成溶液。再通入
的物质的量之比配成溶液。再通入 可制取
可制取 ,同时放出
,同时放出 ,写出该反应的化学方程
,写出该反应的化学方程___________ 。 溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为
溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为___________ 。
(2) 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因
标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因___________ 。
(3)下列关于苏打和小苏打的说法正确的是___________ (选填字母序号)。
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
(4)向 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入
的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标况)如图所示。
的稀盐酸,产生气体体积(标况)如图所示。

请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是___________ (填写化学式)
②滴入 稀盐酸过程中,溶液导电性
稀盐酸过程中,溶液导电性___________ (填“增强”或“减弱”),试解释其原因___________ 。
③原 氢氧化钠溶液的浓度为
氢氧化钠溶液的浓度为___________ 。
 、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。
、苏打、小苏打被称为“苏氏三兄弟”。它们在生活、生产中有广泛应用。(1)工业上,将
 和
和 以
以 的物质的量之比配成溶液。再通入
的物质的量之比配成溶液。再通入 可制取
可制取 ,同时放出
,同时放出 ,写出该反应的化学方程
,写出该反应的化学方程 溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为
溶液在空气中久置,会生成浅黄色物质,经测定该物质具有与过氧化钠相似的结构,该物质的电子式为(2)
 标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因
标准溶液常用于滴定碘的含量,若滴定的溶液呈酸性,测定结果会偏高。用离子方程式表示其原因(3)下列关于苏打和小苏打的说法正确的是
A.纯碱是一种重要的化工原料,在玻璃、肥皂、造纸等工业中都有重要的应用
B.苏打和小苏打的相互转化属于可逆反应
C.苏打(含氯化钠杂质)可用滴定法测苏打的质量分数,使用石蕊溶液做指示剂更准确
D.牙膏中加入小苏打可以让小苏打颗粒直接摩擦牙齿,帮助清洁牙垢
(4)向
 的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入
的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标况)如图所示。
的稀盐酸,产生气体体积(标况)如图所示。
请回答下列问题
①通入二氧化碳后形成溶液的溶质成分是
②滴入
 稀盐酸过程中,溶液导电性
稀盐酸过程中,溶液导电性③原
 氢氧化钠溶液的浓度为
氢氧化钠溶液的浓度为
您最近一年使用:0次
2021-02-09更新
|
1015次组卷
|
7卷引用:河南省信阳市2021届高三上学期第二次教学质量检测化学试题
河南省信阳市2021届高三上学期第二次教学质量检测化学试题(已下线)专题06 钠及其化合物(限时精练)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)第07讲 钠及其重要化合物(精练)-2022年高考化学一轮复习讲练测河北省武安市第一中学2021-2022学年高三上学期第五次调研考试化学试题(已下线)第07讲 钠及其重要化合物(练)-2023年高考化学一轮复习讲练测(全国通用)新疆维吾尔自治区伊犁哈萨克自治州新源县第二中学2021-2022学年上学期高三第一次月考化学试题(已下线)第1讲 钠及其重要化合物
名校
解题方法
6 . 有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,实验班的某同学设计如图实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。(提示固体干燥剂主要有:碱石灰、无水CaCl2、P2O5等)
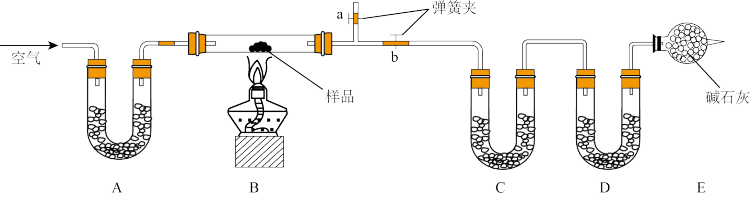
(1)装置A、C中盛放的试剂分别为A__ ,C___ 。
(2)E装置的作用是__ ,若无该装置,则测定结果中NaHCO3的含量将___ (填“偏高”、“偏低”或“无影响”,下同);若B中反应管右侧有水蒸气冷凝,则测定结果中NaHCO3的含量将___ 。
(3)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中NaHCO3质量分数为___ (用含w、m1g、m2g的代数式表示)

(1)装置A、C中盛放的试剂分别为A
(2)E装置的作用是
(3)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中NaHCO3质量分数为
您最近一年使用:0次
解题方法
7 . 为测定Na2CO3·10H2O、NaHCO3的混合物中NaHCO3的含量,设计如下实验:取一定质量的混合物,通过测量反应前后③装置质量的变化,测定该混合物中NaHCO3的质量分数。

完成下列问题:
(1)U形管①②③盛装的均为固态物质,可选试剂依次为___________ 、___________ 、___________ (选填编号)。U形管③吸收的气体为___________ 。
a.碱石灰 b.无水氯化钙 c.无水硫酸铜
(2)干燥管中无水硫酸铜的作用是___________ 。实验装置最后的干燥管中碱石灰的作用___________ 。
(3)实验停止加热后,继续通入空气一段时间的原因是___________ 。
(4)再设计一种测定上述混合物中NaHCO3含量的方案,并注明需要测定的物理量___________ 。

完成下列问题:
(1)U形管①②③盛装的均为固态物质,可选试剂依次为
a.碱石灰 b.无水氯化钙 c.无水硫酸铜
(2)干燥管中无水硫酸铜的作用是
(3)实验停止加热后,继续通入空气一段时间的原因是
(4)再设计一种测定上述混合物中NaHCO3含量的方案,并注明需要测定的物理量
您最近一年使用:0次
21-22高一上·浙江·阶段练习
解题方法
8 . 化学膨松剂可以使食品变得松软或酥脆。某兴趣小组为测定潮湿环境中长期存放的碳酸氢钠膨松剂中 的含量,设计了以下实验,并按如图所示连接装置(气密性良好,各装置中的试剂皆为足量)。
的含量,设计了以下实验,并按如图所示连接装置(气密性良好,各装置中的试剂皆为足量)。
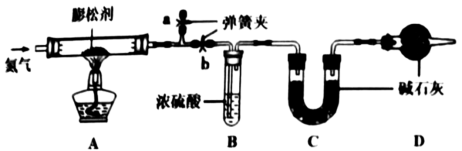
已知:在潮湿的环境中 会慢慢变为
会慢慢变为 。
。
(1)写出膨松剂中 受热分解的化学方程式
受热分解的化学方程式___________ ;停止加热后,应继续通入一段时间氮气的目的是___________ 。
(2)装置B中浓硫酸的作用是___________ 。
(3)若A装置中反应管右侧有水蒸气冷凝,则测得的 含量将
含量将___________ (填“偏高”、“偏低”或“无影响”);若撤去D装置,则测得的 含量将
含量将___________ (填“偏高”、“偏低”或“无影响”)。
(4)若膨松剂的质量为wg,反应后C装置增加的质量为mg,则膨松剂中 的质量分数为
的质量分数为___________ (用含w、m的代数式表示)。
 的含量,设计了以下实验,并按如图所示连接装置(气密性良好,各装置中的试剂皆为足量)。
的含量,设计了以下实验,并按如图所示连接装置(气密性良好,各装置中的试剂皆为足量)。
已知:在潮湿的环境中
 会慢慢变为
会慢慢变为 。
。(1)写出膨松剂中
 受热分解的化学方程式
受热分解的化学方程式(2)装置B中浓硫酸的作用是
(3)若A装置中反应管右侧有水蒸气冷凝,则测得的
 含量将
含量将 含量将
含量将(4)若膨松剂的质量为wg,反应后C装置增加的质量为mg,则膨松剂中
 的质量分数为
的质量分数为
您最近一年使用:0次
21-22高一上·浙江·阶段练习
名校
解题方法
9 . 化学膨松剂可以使食品变得松软或酥脆。某兴趣小组为测定潮湿环境中长期存放的碳酸氢钠膨松剂中 的含量,设计了以下实验,并按如图所示连接装置(气密性良好,各装置中的试剂皆为足量)。
的含量,设计了以下实验,并按如图所示连接装置(气密性良好,各装置中的试剂皆为足量)。

已知:在潮湿的环境中 会慢慢变为
会慢慢变为 。
。
(1)写出膨松剂中 受热分解的化学方程式
受热分解的化学方程式_______ ;停止加热后,应继续通入一段时间氮气的目的是_______ 。
(2)装置B、C中盛放的试剂分别为:B_______ ,C_______ 。
(3)若A装置中反应管右侧有水蒸气冷凝,则测得的 含量将
含量将_______ (填“偏高”、“偏低”或“无影响”);若撤去D装置,则测得的 含量将
含量将_______ (填“偏高”、“偏低”或“无影响”)。
(4)若膨松剂的质量为 ,反应后C装置增加的质量为
,反应后C装置增加的质量为 ,则膨松剂中
,则膨松剂中 的质量分数为
的质量分数为_______ (用含w、m的代数式表示)。
(5)兴趣小组还设计了下列实验方案,其中能测定出膨松剂中 含量的是
含量的是_______ 。
A.取a克膨松剂充分加热,质量减少b克
B.取a克膨松剂与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b克固体
C.取a克膨松剂与足量稀硫酸充分反应,逸出气体干燥后用碱石灰吸收,质量增加b克
D.取a克膨松剂与足量 溶液充分反应,得到b克溶液
溶液充分反应,得到b克溶液
 的含量,设计了以下实验,并按如图所示连接装置(气密性良好,各装置中的试剂皆为足量)。
的含量,设计了以下实验,并按如图所示连接装置(气密性良好,各装置中的试剂皆为足量)。
已知:在潮湿的环境中
 会慢慢变为
会慢慢变为 。
。(1)写出膨松剂中
 受热分解的化学方程式
受热分解的化学方程式(2)装置B、C中盛放的试剂分别为:B
(3)若A装置中反应管右侧有水蒸气冷凝,则测得的
 含量将
含量将 含量将
含量将(4)若膨松剂的质量为
 ,反应后C装置增加的质量为
,反应后C装置增加的质量为 ,则膨松剂中
,则膨松剂中 的质量分数为
的质量分数为(5)兴趣小组还设计了下列实验方案,其中能测定出膨松剂中
 含量的是
含量的是A.取a克膨松剂充分加热,质量减少b克
B.取a克膨松剂与足量稀盐酸充分反应,加热、蒸干、灼烧,得到b克固体
C.取a克膨松剂与足量稀硫酸充分反应,逸出气体干燥后用碱石灰吸收,质量增加b克
D.取a克膨松剂与足量
 溶液充分反应,得到b克溶液
溶液充分反应,得到b克溶液
您最近一年使用:0次
2021-04-12更新
|
686次组卷
|
4卷引用:【浙江新东方】在线化学55高一上
名校
10 . 为了测定NaCl、Na2CO3·10H2O和NaHCO3的混合物中各组分的含量,某同学设计如下实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法中正确的是


| A.②和③中应依次盛装碱石灰和无水CaCl2 |
| B.若将①装置换成盛有NaOH溶液的洗气瓶,则测得的NaCl含量偏小 |
| C.实验时应先点燃酒精灯,再关闭b、打开a,一段时间后测定②和③的质量变化 |
D.若测得②和③的增重分别为m2和m3,则混合物中Na2CO3·10H2O的质量为28.6×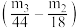 |
您最近一年使用:0次
2020-11-27更新
|
1135次组卷
|
3卷引用:浙江省宁波市效实中学2020-2021学年高一上学期期中考试化学试题
浙江省宁波市效实中学2020-2021学年高一上学期期中考试化学试题(已下线)专题卷三 钠及其化合物(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)河南省遂平县第一高级中学2023-2024学年高一上学期第一次月考化学试题



