名校
解题方法
1 . NaCl是一种化工原料,可以制备多种物质,如图所示。
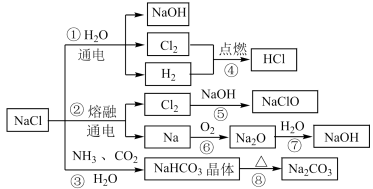
请回答下列问题:
(1)图所列物质中属于电解质的有_____ 种,转化反应中属于氧化还原反应的有_____ (填图中序号)
(2)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是_____________ 。
(3)反应④的现象是_____ ;反应⑤的化学方程式为_____ 。
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。某同学购买了一瓶某品牌的“84消毒液”,查看相关资料及包装说明可获得以下信息:原液净含量为600g、密度约为1.1 g/cm3、有效成分NaClO的质量分数约为1.9%(通过有效氯含量折算而得)。
该同学从中取出100 mL原液,按包装说明稀释30倍(体积之比)后用于家庭一般物体表面消毒,稀释后的溶液中c(NaClO)=_____ mol/L(结果保留两位小数);“84消毒液”不能与“洁厕灵(主要成分是HCl)”混合使用,否则会产生黄绿色的有毒气体引起安全事故,其反应的离子方程式是_________ 。
(5)反应③和⑧是工业制备纯碱的原理,我国化学工业科学家侯德榜提出了将氨碱法(又称索尔维法)制取碳酸钠和合成氨联合的改进工艺,这就是联合制碱法,也称侯氏制碱法。侯氏制碱法提高了食盐的转化率,缩短了生产流程,减少了对环境的污染,将制碱技术发展到了一个新的水平,赢得了国际化工界的高度评价。以下是这两种制碱法的工艺流程图:
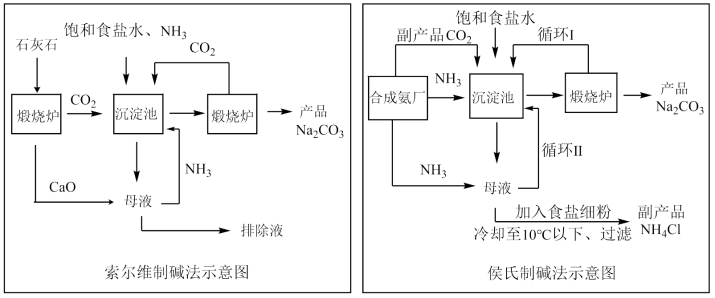
下列说法正确的是_____ (填序号)。
A.用NaCl制取纯碱的过程中,利用了物质溶解度的差异
B.沉淀池中NH3与CO2的通入顺序为先通入CO2,再通入NH3
C.索尔维制碱法所得“排出液”的主要成分为CaCl2
D.侯氏制碱法循环利用的物质主要是CO2和NH3
E.侯氏制碱法从母液中经过循环Ⅱ进入沉淀池的主要有NH3·H2O、NH4Cl、Na2CO3,从而使原料NaCl的利用率大大提升
F.侯氏制碱法在母液中加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
G.检验产品Na2CO3中是否含有NaCl的操作方法是取少量试样溶于水,加入过量的稀硝酸,再滴加硝酸银溶液,观察是否有白色沉淀生成

请回答下列问题:
(1)图所列物质中属于电解质的有
(2)工业上制取NaOH主要采用反应①,而不采用反应⑦的方法,主要原因是
(3)反应④的现象是
(4)NaClO是“84消毒液”的有效成分,在抗击新冠肺炎疫情中发挥了重要作用。某同学购买了一瓶某品牌的“84消毒液”,查看相关资料及包装说明可获得以下信息:原液净含量为600g、密度约为1.1 g/cm3、有效成分NaClO的质量分数约为1.9%(通过有效氯含量折算而得)。
该同学从中取出100 mL原液,按包装说明稀释30倍(体积之比)后用于家庭一般物体表面消毒,稀释后的溶液中c(NaClO)=
(5)反应③和⑧是工业制备纯碱的原理,我国化学工业科学家侯德榜提出了将氨碱法(又称索尔维法)制取碳酸钠和合成氨联合的改进工艺,这就是联合制碱法,也称侯氏制碱法。侯氏制碱法提高了食盐的转化率,缩短了生产流程,减少了对环境的污染,将制碱技术发展到了一个新的水平,赢得了国际化工界的高度评价。以下是这两种制碱法的工艺流程图:

下列说法正确的是
A.用NaCl制取纯碱的过程中,利用了物质溶解度的差异
B.沉淀池中NH3与CO2的通入顺序为先通入CO2,再通入NH3
C.索尔维制碱法所得“排出液”的主要成分为CaCl2
D.侯氏制碱法循环利用的物质主要是CO2和NH3
E.侯氏制碱法从母液中经过循环Ⅱ进入沉淀池的主要有NH3·H2O、NH4Cl、Na2CO3,从而使原料NaCl的利用率大大提升
F.侯氏制碱法在母液中加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
G.检验产品Na2CO3中是否含有NaCl的操作方法是取少量试样溶于水,加入过量的稀硝酸,再滴加硝酸银溶液,观察是否有白色沉淀生成
您最近一年使用:0次
2020-11-24更新
|
258次组卷
|
2卷引用:湖湘教育三新探索协作体 2020-2021学年高一11月联考化学试题
名校
2 . 为了测定NaCl、Na2CO3·10H2O和NaHCO3的混合物中各组分的含量,某同学设计如下实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法错误的是
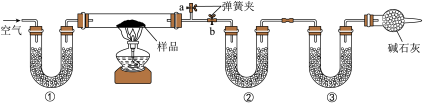

| A.①、②、③中可以依次盛装碱石灰、无水CaCl2、碱石灰 |
| B.若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏大 |
| C.硬质玻璃管加热前,应关闭b,打开a,缓缓通入空气,直至a处出来的空气不再使澄清石灰水变浑浊为止 |
| D.实验结束时先停止通入空气,再停止加热 |
您最近一年使用:0次
2020-09-13更新
|
295次组卷
|
3卷引用:江苏省无锡江阴市2021届高三暑期作业开学检测化学试题
解题方法
3 . 碳酸氢钠是重要的化工产品。用标准盐酸溶液滴定可测定碳酸氢钠样品中碳酸氢钠含量。已知碳酸氢钠受热易分解,且在250℃~270℃分解完全。
完成下列填空:
(1)测定碳酸氢钠含量的实验步骤:用电子天平称取碳酸氢钠样品(准确到_____ g),加入锥形瓶中,加入使之完全溶解;加入甲基橙指示剂,用标准盐酸溶液滴定。当滴定至溶液由_____ 色变为_____ 色,半分钟不变色为滴定终点,记录读数。该实验不能用酚酞作指示剂的原因是_____ 。
(2)若碳酸氢钠样品质量为0.840g,用0.5000mol/L的标准盐酸溶液滴定至终点,消耗标准盐酸溶液19.50mL。样品中NaHCO3的质量分数为_____ (保留3位小数)。
(3)如果滴定尖嘴部分在滴定过程中出现气泡,且滴定终点读数时气泡未消失,会导致测定结果____ (选填“偏高”、“偏低”或“不受影响”)。
(4)碳酸氢钠样品含有少量水分(<0.5%)和氯化钠。以下是测定碳酸氢钠样品中水分的实验方案(样品中NaHCO3含量已知)。
①在恒重的坩埚中称取碳酸氢钠样品,样品和坩埚的质量为m1g。
②将样品和坩埚置于电热炉内,在250℃~270℃加热分解至完全,经恒重,样品和坩埚的质量为m2g。
③……。
该实验方案中,质量差(m1-m2)是_____ 的质量。若所称取样品中NaHCO3的质量为m3g,则样品中水分的质量m=_____ (用含m、m1、m2的代数式表示)。
完成下列填空:
(1)测定碳酸氢钠含量的实验步骤:用电子天平称取碳酸氢钠样品(准确到
(2)若碳酸氢钠样品质量为0.840g,用0.5000mol/L的标准盐酸溶液滴定至终点,消耗标准盐酸溶液19.50mL。样品中NaHCO3的质量分数为
(3)如果滴定尖嘴部分在滴定过程中出现气泡,且滴定终点读数时气泡未消失,会导致测定结果
(4)碳酸氢钠样品含有少量水分(<0.5%)和氯化钠。以下是测定碳酸氢钠样品中水分的实验方案(样品中NaHCO3含量已知)。
①在恒重的坩埚中称取碳酸氢钠样品,样品和坩埚的质量为m1g。
②将样品和坩埚置于电热炉内,在250℃~270℃加热分解至完全,经恒重,样品和坩埚的质量为m2g。
③……。
该实验方案中,质量差(m1-m2)是
您最近一年使用:0次
名校
4 . 计算题
(1)某地产石灰石所含杂质不溶于水也不与盐酸反应。为测定该石灰石中碳酸钙的含量,现进行下列实验:称取25g石灰石放在质量为145g的烧杯中,向其中加入100g稀盐酸,反应恰好完全,此时称量烧杯及其中溶液,总质量为261.2g,求:
①石灰石中碳酸钙的质量为__________ 克。
②反应后溶液中溶质的质量分数为__________ (保留两位有效数字)。
(2)某厂的某钢样粉末28.36 g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3 g白色沉淀。
①计算可得此钢样粉末中铁和碳的质量之比为__________ 。
②再取三份不同质量的钢样粉末分别加到50g质量分数相同的硫酸中,充分反应后,测得的实验数据如下表所示:(标准状况下,2克 H2的体积为22.4L)
根据表中的数据计算,硫酸溶液中H2SO4溶质的质量分数是__________
(1)某地产石灰石所含杂质不溶于水也不与盐酸反应。为测定该石灰石中碳酸钙的含量,现进行下列实验:称取25g石灰石放在质量为145g的烧杯中,向其中加入100g稀盐酸,反应恰好完全,此时称量烧杯及其中溶液,总质量为261.2g,求:
①石灰石中碳酸钙的质量为
②反应后溶液中溶质的质量分数为
(2)某厂的某钢样粉末28.36 g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3 g白色沉淀。
①计算可得此钢样粉末中铁和碳的质量之比为
②再取三份不同质量的钢样粉末分别加到50g质量分数相同的硫酸中,充分反应后,测得的实验数据如下表所示:(标准状况下,2克 H2的体积为22.4L)
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量 / g | 2.836 | 5.672 | 8.508 |
| 生成气体的体积(标准状况)/ L | 1.12 | 2.24 | 2.80 |
根据表中的数据计算,硫酸溶液中H2SO4溶质的质量分数是
您最近一年使用:0次
5 . 有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。
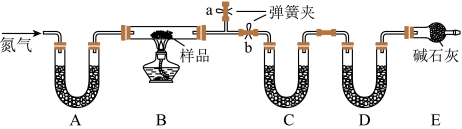
(1)加热前通入氮气的目的是_____________ ,操作方法为____________ 。
(2)装置A、C、D中盛放的试剂分别为A_______ ,C________ ,D_______ 。
(3)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl的含量将_______ (填“偏高”、“偏低”或“无影响”,下同);若B中反应管右侧有水蒸气冷凝,则测定结果中NaHCO3的含量将________ ;
(4)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中Na2CO3·10H2O的质量分数为_______ (用含w、m1、m2的代数式表示)

(1)加热前通入氮气的目的是
(2)装置A、C、D中盛放的试剂分别为A
(3)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl的含量将
(4)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中Na2CO3·10H2O的质量分数为
您最近一年使用:0次
9-10高二下·江苏盐城·期末
6 . 油条是一种深受群众喜爱的传统食品,在百姓早餐桌上一直占有重要位置。但油条中铝含量超标问题十分普遍,是影响群众健康的食品安全隐患。从2009年5月下旬开始,浙江省的油条加工停用含铝食品的添加剂,逐步转换为无铝添加剂配方和工艺,从而保证百姓吃上安全、放心的油条。油条无铝配方由碳酸氢钠(小苏打)、碳酸氢铵(臭粉)组成。为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验。

实验过程:
①按图组装仪器,检查装置的气密性;
②将试样m1g放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3g;
③打开活塞a,通N2一段时间后,关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
④称得装置B的质量为m4g、装置C的质量为m5g。
请回答以下问题:
(1)装置A中发生反应的化学方程式为_______ ,_______ 。
(2)装置D的作用为防止空气中_______ 进入装置C中。装置C的作用为_______ 。
(3)实验过程中第二次通入N2的目的是把装置中产生的_______ 排出,使其被装置B和装置C完全吸收。
(4)用下列各项所提供的数据能计算出w(NaHCO3)的是_______ (填写序号)
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的w(NaHCO3)_______ (填“能”或“不能”)。

实验过程:
①按图组装仪器,检查装置的气密性;
②将试样m1g放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3g;
③打开活塞a,通N2一段时间后,关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
④称得装置B的质量为m4g、装置C的质量为m5g。
请回答以下问题:
(1)装置A中发生反应的化学方程式为
(2)装置D的作用为防止空气中
(3)实验过程中第二次通入N2的目的是把装置中产生的
(4)用下列各项所提供的数据能计算出w(NaHCO3)的是
| 序号 | a | b | c | d | e |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m3、m5 |
您最近一年使用:0次
11-12高三上·山东济宁·阶段练习
7 . 有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。
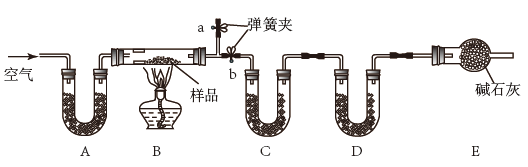
(1)实验时,B中发生反应的化学方程式为______ ,______ 。
(2)装置C、D中盛放的试剂分别为:C______ ,D______ (供选试剂为:浓硫酸、无水CaCl2、碱石灰)
(3)E装置中的仪器名称是______ ,它在该实验中的主要作用是______
(4)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量将______ (填“偏高”、“偏低”或“无影响”)。
(5)若样品的质量为m g,反应后C、D的质量差分别为m1g、m2g,则该混合物中Na2CO3·10H2O的质量分数为:______ (结果用分数表示,可不化简)。

(1)实验时,B中发生反应的化学方程式为
(2)装置C、D中盛放的试剂分别为:C
(3)E装置中的仪器名称是
(4)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量将
(5)若样品的质量为m g,反应后C、D的质量差分别为m1g、m2g,则该混合物中Na2CO3·10H2O的质量分数为:
您最近一年使用:0次
名校
8 . 为了测定NaCl、Na2CO3·10H2O和NaHCO3的混合物中各组分的含量,某同学设计如下实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说法错误的是
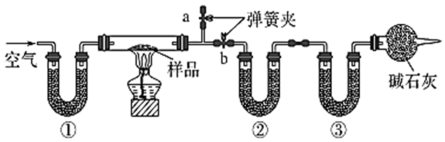

| A.①、②、③中可以依次盛装碱石灰、无水CaCl2、碱石灰 |
| B.硬质玻璃管加热前,应关闭b,打开a,缓缓通入空气,直至a 处出来的空气不再使澄清石灰水变浑浊为止 |
| C.若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏大 |
| D.实验过程中一直通入空气,停止加热后再停止通入空气 |
您最近一年使用:0次
2018-01-20更新
|
643次组卷
|
7卷引用:河南省安阳市2018届高三第一次模拟考试理综化学试题
河南省安阳市2018届高三第一次模拟考试理综化学试题安徽省舒城中学2020-2021学年高一上学期期中考试化学试题(已下线)【教材实验热点】03 碳酸钠和碳酸氢钠性质的研究(已下线)专题02 海水中的重要元素——钠和氯-2023年高考化学一轮复习小题多维练(全国通用)新疆维吾尔自治区喀什第二中学2021-2022学年高三上学期10月月考化学试题河北省石家庄市第四中学2022-2023学年高三上学期十月月考化学试题第三章 金属及其化合物 热点强化5 钠的化合物组成成分的测定
9 . 样品中Al的质量分数为__________________ (用小数表示,小数点后保留两位)。
该小组为了测定其中Al2O3的含量,从上面反应后的100mL溶液中,取出10mL溶液,逐滴加入1mol/L的盐酸,当滴到5.00mL时开始产生沉淀,继续滴加盐酸,至25.00mL时沉淀恰好全部溶解。
该小组为了测定其中Al2O3的含量,从上面反应后的100mL溶液中,取出10mL溶液,逐滴加入1mol/L的盐酸,当滴到5.00mL时开始产生沉淀,继续滴加盐酸,至25.00mL时沉淀恰好全部溶解。
您最近一年使用:0次
10 . 我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献.他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱.有关反应的化学方程式为:
NH3+CO2+H2O=NH4HCO3;
NH4HCO3+NaCl=NaHCO3↓+NH4Cl;
2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
回答下列问题:
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是__________ (填字母标号)。
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
(Ⅰ)一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
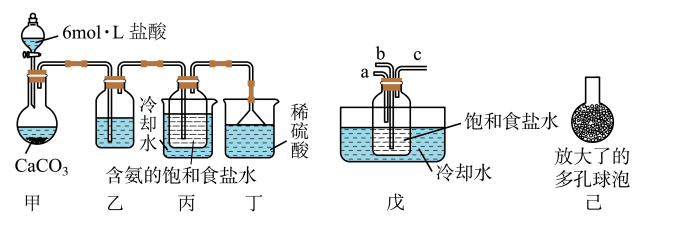
试回答下列有关问题:
①乙装置中的试剂是_____________ 。
②丁装置的作用是____________________ 。
(Ⅱ)另一位同学用图中戊装置(其它装置未画出)进行实验。
①实验时,须先从a管通入___________ 气体(填气体分子式),再从b管通入__________ 气体(填气体分子式)。
②有同学建议在戊装置的b管下端连接己装置,理由是__________________________ 。
(3)探究小苏打样品(含少量NaCl)中碳酸氢钠的含量:
称取1.840 g小苏打样品(含少量NaCl),配置成250 mL溶液,取出25.00 mL用0.1000mol·L-1盐酸滴定,消耗盐酸21.50 mL。
①实验中所需要的定量仪器除滴定管外,还有______________________________ 。
②样品中NaHCO3质量分数为__________________________ 。
(4)将一定质量小苏打样品(只考虑含少量NaCl)溶于足量盐酸,蒸干后称量固体质量,也可测定小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果_____________ 。(选填“偏高”、“偏低”或“不受影响”)
NH3+CO2+H2O=NH4HCO3;
NH4HCO3+NaCl=NaHCO3↓+NH4Cl;
2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O回答下列问题:
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
(Ⅰ)一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。

试回答下列有关问题:
①乙装置中的试剂是
②丁装置的作用是
(Ⅱ)另一位同学用图中戊装置(其它装置未画出)进行实验。
①实验时,须先从a管通入
②有同学建议在戊装置的b管下端连接己装置,理由是
(3)探究小苏打样品(含少量NaCl)中碳酸氢钠的含量:
称取1.840 g小苏打样品(含少量NaCl),配置成250 mL溶液,取出25.00 mL用0.1000mol·L-1盐酸滴定,消耗盐酸21.50 mL。
①实验中所需要的定量仪器除滴定管外,还有
②样品中NaHCO3质量分数为
(4)将一定质量小苏打样品(只考虑含少量NaCl)溶于足量盐酸,蒸干后称量固体质量,也可测定小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果
您最近一年使用:0次



