10-11高三上·江西吉安·阶段练习
1 . 500mL某浓度的NaOH溶液恰好与标准状况下11.2LCO2完全反应生成正盐,则
①原溶液中NaOH的物质的量浓度为___________ ,
②若在原溶液中通入16.8L(标准状况下)CO2则生成的产物是__________________ 。
③若在②中的产物中加足量的盐酸,则需要盐酸的物质的量为_______________ 。
①原溶液中NaOH的物质的量浓度为
②若在原溶液中通入16.8L(标准状况下)CO2则生成的产物是
③若在②中的产物中加足量的盐酸,则需要盐酸的物质的量为
您最近一年使用:0次
10-11高一上·江西九江·阶段练习
2 . ⑴加热10.0g碳酸钠和碳酸氢钠的混合物至质量不再变化,剩余固体的质量为8.45g,求混合物中碳酸钠的质量分数。(列出计算过程)______
⑵过氧化钠与铝粉混合物共18.3g,加入100ml 水,充分反应后混合物完全溶解,并收集到5.6L气体(标准状况).则收集到的气体成份是______________ ,体积比是____ 。
⑵过氧化钠与铝粉混合物共18.3g,加入100ml 水,充分反应后混合物完全溶解,并收集到5.6L气体(标准状况).则收集到的气体成份是
您最近一年使用:0次
10-11高三上·浙江杭州·阶段练习
3 . 某天然碱可以看作是CO2和NaOH反应后的产物组成的一种物质。为了测定该物质的成分,进行如下实验:⑴称取3.32g天然碱样品,加入30mL过量稀盐酸,产生672mL CO2气体(标准状况);⑵另称取3.32g天然碱样品,在300℃下加热至分解完全,产生CO2 112mL(标准状况)和0.45g水。试通过计算,确定天然碱的化学式。
您最近一年使用:0次
10-11高一上·重庆·阶段练习
4 . 天然碱是一种重要的矿物质,盛产于我国的青海湖地区。某天然碱样品的成分可以看成是碳酸钠、碳酸氢钠和水按物质的量之比1:1:2形成的结晶水合物。请回答下列问题:
(1)这种天然碱中碳酸钠、碳酸氢钠和水三者的质量比为___________ 。
(2)45.2 g此天然碱与100 mL密度为1.1 g/cm3的中等浓度盐酸恰好完全反应,产生a mol CO2,则a=_______ ,盐酸中溶质的质量分数ω(HCl)=_______ %。
(3)用一个化学方程式表示该天然碱与盐酸的反应:
___________________________ 。
(1)这种天然碱中碳酸钠、碳酸氢钠和水三者的质量比为
(2)45.2 g此天然碱与100 mL密度为1.1 g/cm3的中等浓度盐酸恰好完全反应,产生a mol CO2,则a=
(3)用一个化学方程式表示该天然碱与盐酸的反应:
您最近一年使用:0次
5 . 将a mol的Na2O2和b mol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应。
(1)当剩余固体为Na2CO3,排出气体为O2,H2O时,a:b的值为________ 。
(2)当剩余固体为Na2CO3,NaOH,排出气体为O2时,a:b的值为________ 。
(3)当a:b>1时,剩余固体为________ ,排出气体为________ 。
(4)当排出的O2和H2O为等物质的量时,则a:b的值为________ 。
(1)当剩余固体为Na2CO3,排出气体为O2,H2O时,a:b的值为
(2)当剩余固体为Na2CO3,NaOH,排出气体为O2时,a:b的值为
(3)当a:b>1时,剩余固体为
(4)当排出的O2和H2O为等物质的量时,则a:b的值为
您最近一年使用:0次
10-11高一上·山西·阶段练习
6 . 将一定量的 Na2CO3和NaHCO3的混合物,跟足量盐酸反应共消耗0.8 mol HCl,生成0.5mol二氧化碳。求原混合物中NaHCO3的质量分数为多少?
您最近一年使用:0次
10-11高三上·辽宁沈阳·阶段练习
7 . 取物质的量浓度相等的NaOH溶液两份甲和乙,每份50 mL,分别向甲、乙中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的HCl溶液,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如下图所示,试回答下列问题:
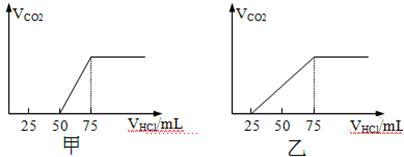
试分析NaOH在吸收CO2气体后,在甲所得溶液中存在的溶质是_________ ,其物质的量之比是_________ , 产生的CO2气体体积(标况)是___________ . 在乙所得溶液中存在的溶质是_________ ,其物质的量之比是___________ , 产生的CO2气体体积(标况)是_________ .

试分析NaOH在吸收CO2气体后,在甲所得溶液中存在的溶质是
您最近一年使用:0次
8 . 小苏打、胃舒、平达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.5g NaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是___________ mol。
(2)胃舒平每片含0.245g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平_____ 片。
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比。________
②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的化学式。
________
(1)小苏打片每片含0.5g NaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是
(2)胃舒平每片含0.245g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比。
②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的化学式。
您最近一年使用:0次



