解题方法
1 . 下列关于物质或者离子检验的试剂(反应条件可以加热)说法错误的是
A.检验 固体是否在空气中变质的试剂是盐酸和 固体是否在空气中变质的试剂是盐酸和 溶液 溶液 |
| B.检验纯碱固体中是否含有小苏打的试剂是澄清石灰水 |
C.检验氯气中是否含有HCl气体的试剂是稀 和 和 溶液 溶液 |
D.检验 气体中是否混有 气体中是否混有 气体的试剂是品红溶液 气体的试剂是品红溶液 |
您最近一年使用:0次
名校
2 . 下列实验装置合理且能达到实验目的的是

A.用装置甲制备 |
B.用装置乙比较 和 和 的热稳定性 的热稳定性 |
| C.用装置丙测定醋酸浓度 |
D.用装置丁制备并收集 |
您最近一年使用:0次
2024-03-03更新
|
163次组卷
|
2卷引用:河北省衡水董子高级中学等校2023-2024学年高三下学期2月 入校考试 化学试题
名校
解题方法
3 . 下列关于钠的化合物的说法中不正确的是
①热稳定性:碳酸钠>碳酸氢钠
②与盐酸反应的剧烈程度:碳酸钠>碳酸氢钠
③氧化钠和过氧化钠晶体中阴、阳离子的数目比相同,均为1∶2
④等质量的固体与足量盐酸反应放出气体的质量:碳酸钠>碳酸氢钠
⑤分别向碳酸钠和碳酸氢钠的水溶液中滴加BaCl2溶液,均可产生白色沉淀
①热稳定性:碳酸钠>碳酸氢钠
②与盐酸反应的剧烈程度:碳酸钠>碳酸氢钠
③氧化钠和过氧化钠晶体中阴、阳离子的数目比相同,均为1∶2
④等质量的固体与足量盐酸反应放出气体的质量:碳酸钠>碳酸氢钠
⑤分别向碳酸钠和碳酸氢钠的水溶液中滴加BaCl2溶液,均可产生白色沉淀
| A.②④⑤ | B.①②④ | C.②③⑤ | D.③④⑤ |
您最近一年使用:0次
名校
4 . 室温下,下列实验探究方案能够边到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 将 溴丁烷与 溴丁烷与 的乙醇溶液混合后加热,生成的气体通入 的乙醇溶液混合后加热,生成的气体通入 的 的 溶液中,观察现象 溶液中,观察现象 |  溴丁烷能否发生消去反应生成烯烃 溴丁烷能否发生消去反应生成烯烃 |
| B | 将 气体通入紫色石蕊溶液中,观察溶液颜色变化 气体通入紫色石蕊溶液中,观察溶液颜色变化 |  是否具有漂白性 是否具有漂白性 |
| C | 向饱和 溶液中通入足量 溶液中通入足量 气体,观察现象 气体,观察现象 | 比较 与 与 在水中溶解度的大小 在水中溶解度的大小 |
| D | 向 溶液中滴加淀粉,再通入 溶液中滴加淀粉,再通入 气体,观察现象 气体,观察现象 | 比较 与 与 氧化性的强弱 氧化性的强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-01更新
|
732次组卷
|
2卷引用:江苏省无锡市锡东高级中学2023-2024学年高三下学期4月月考化学试题
名校
解题方法
5 . 在一定条件下含有相同元素的物质的转化是有规律的。某金属单质A及其化合物间的转化关系如图(某些产物和反应条件已略去),其中C为淡黄色的固体,D是一种无色无味的气体,能使澄清石灰水变浑浊,常温下E为液体,完成下列问题:
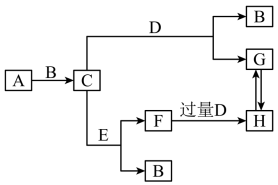
(1)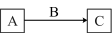 实验现象是
实验现象是___________ 。
(2)写出C+D=B+G的化学方程式:___________ 。
(3)C可在呼吸面具中作为氧气来源,假设每人每分钟消耗0.448LO2(标准状况),且所需的O2全部由Na2O2来提供,则某消防员工作1小时所需Na2O2的质量为___________ g。
(4)写出F+H=E+G反应的离子方程式:___________ 。
(5)向G的饱和溶液中通入过量D会生成H沉淀,其原因有①生成的H质量大于原溶液中G质量;②在相同条件下,___________ ;③溶剂H2O质量减少。
(6)下列有关G和H的性质比较,叙述正确的是___________(填字母)。
(7)加热5.00gG和H的固体混合物,使H完全分解,固体混合物的质量减少了1.24g,则原混合物中G的质量为___________ g。

(1)
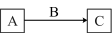 实验现象是
实验现象是(2)写出C+D=B+G的化学方程式:
(3)C可在呼吸面具中作为氧气来源,假设每人每分钟消耗0.448LO2(标准状况),且所需的O2全部由Na2O2来提供,则某消防员工作1小时所需Na2O2的质量为
(4)写出F+H=E+G反应的离子方程式:
(5)向G的饱和溶液中通入过量D会生成H沉淀,其原因有①生成的H质量大于原溶液中G质量;②在相同条件下,
(6)下列有关G和H的性质比较,叙述正确的是___________(填字母)。
| A.分别向固体G和H中滴入少量水,前者温度升高,后者温度下降 |
| B.分别向等物质的量浓度的G和H溶液中滴加酚酞,后者红色更深 |
| C.二者热稳定性不同,G的热稳定性强于H |
| D.同一温度下,与同浓度的盐酸反应时,固体G比固体H更剧烈 |
您最近一年使用:0次
名校
解题方法
6 . 碳元素及其化合物在自然界广泛存在且具有重要应用。 具有较大的燃烧热
具有较大的燃烧热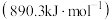 ,是常见燃料。用
,是常见燃料。用 溶液吸收
溶液吸收 生成
生成 溶液是
溶液是 “固定”再利用的方法之一、电解
“固定”再利用的方法之一、电解 溶液可获得
溶液可获得 ;向
;向 溶液中加入铁粉,反应初期产生
溶液中加入铁粉,反应初期产生 并生成
并生成 迅速转化为活性
迅速转化为活性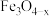 ,活性
,活性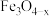 催化
催化 加氢生成
加氢生成 。“侯氏制碱法”是以
。“侯氏制碱法”是以 为原料制备
为原料制备 。下列化学反应表示正确的是
。下列化学反应表示正确的是
 具有较大的燃烧热
具有较大的燃烧热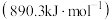 ,是常见燃料。用
,是常见燃料。用 溶液吸收
溶液吸收 生成
生成 溶液是
溶液是 “固定”再利用的方法之一、电解
“固定”再利用的方法之一、电解 溶液可获得
溶液可获得 ;向
;向 溶液中加入铁粉,反应初期产生
溶液中加入铁粉,反应初期产生 并生成
并生成 迅速转化为活性
迅速转化为活性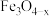 ,活性
,活性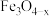 催化
催化 加氢生成
加氢生成 。“侯氏制碱法”是以
。“侯氏制碱法”是以 为原料制备
为原料制备 。下列化学反应表示正确的是
。下列化学反应表示正确的是A.甲烷的燃烧: |
B.铁粉和 溶液反应制 溶液反应制 |
C. 通入氨的饱和食盐水中: 通入氨的饱和食盐水中: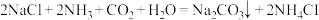 |
D.催化电解 生成 生成 的阳极反应式: 的阳极反应式: |
您最近一年使用:0次
名校
解题方法
7 . 小组同学探究 和
和 的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是
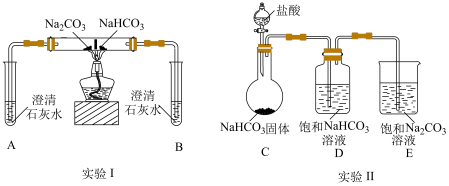
的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是
 和
和 的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是
的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是
| A.实验Ⅰ,A中澄清石灰水无明显变化,B中澄清石灰水变浑浊 |
B.实验Ⅱ,C中发生反应的离子方程式为: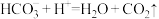 |
C.实验Ⅱ中,一段时间之后,可观察到 中有细小晶体析出 中有细小晶体析出 |
D.等物质的量的 、 、 分别与足量盐酸反应, 分别与足量盐酸反应, 生成的 生成的 更多 更多 |
您最近一年使用:0次
名校
解题方法
8 . 某实验小组欲探究 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为___________ 。
(2)称取两种固体各2g,分别加入烧杯甲、乙中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①烧杯甲中的固体完全溶解,而烧杯乙中的固体有剩余,由此得出结论:___________ 。
②同学们在两烧杯中还观察到以下现象。其中,盛放 的烧杯中出现的现象是
的烧杯中出现的现象是___________ (填字母序号)。
a.溶液温度升高 b.溶液温度下降 c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置I和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。
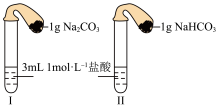
①两试管中均产生气体,___________ 的反应程度更为剧烈。(填“I”或“Ⅱ”)
②反应结束后,恢复至室温,下列说法正确的是___________ 。
a.装置I的气球体积较大 b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:
实施实验后,发现操作1的现象与预测有差异:产生白色沉淀和二氧化碳气体。则该条件下, 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为
(2)称取两种固体各2g,分别加入烧杯甲、乙中,再各加10mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①烧杯甲中的固体完全溶解,而烧杯乙中的固体有剩余,由此得出结论:
②同学们在两烧杯中还观察到以下现象。其中,盛放
 的烧杯中出现的现象是
的烧杯中出现的现象是a.溶液温度升高 b.溶液温度下降 c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)如图所示,在气密性良好的装置I和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。

①两试管中均产生气体,
②反应结束后,恢复至室温,下列说法正确的是
a.装置I的气球体积较大 b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算 d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成
 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:| 实验方案 | 预测现象 | 预测依据 |
操作1:向2mL 溶液中滴加1mL 溶液中滴加1mL  溶液 溶液 | 无白色沉淀 |  溶液中的 溶液中的 浓度很小,不能与 浓度很小,不能与 反应 反应 |
操作2:向2mL 溶液中滴加1mL 溶液中滴加1mL  溶液 溶液 | 有白色沉淀 |  溶液中的 溶液中的 浓度较大,能与 浓度较大,能与 发生反应 发生反应 |
 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
名校
9 . 下列关于钠及其化合物的叙述,正确的是
| A.Na2O与Na2O2都能和H2O、CO2反应,它们都是化合反应 |
| B.Na2CO3溶液和NaHCO3溶液都能跟稀CaCl2溶液反应得到白色沉淀 |
| C.向酚酞溶液中加入Na2O粉末,溶液变红 |
| D.金属Na在空气中燃烧,发出黄色火焰,产物是Na2O |
您最近一年使用:0次
名校
解题方法
10 . Ⅰ. 和
和 是两种常见的钠盐。
是两种常见的钠盐。
向 和
和 的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
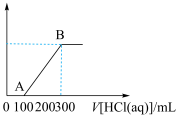
(1)OA段发生反应的离子方程式:________ 。
(2)原溶液中碳酸钠和碳酸氢钠的物质的量之比为_______ 。
Ⅱ.实验室中需0.2 mol/L的 溶液80 mL,请回答下列问题。
溶液80 mL,请回答下列问题。
(3)配制上述溶液所需的玻璃 仪器有:玻璃棒、烧杯和______ ,用托盘天平称取 固体,其质量是
固体,其质量是_______ g。
(4)实验时下图所示操作的先后顺序为______ (填编号)。
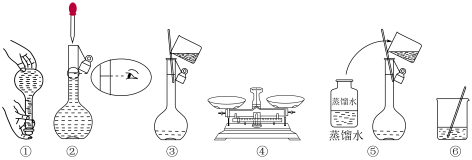
(5)取用任意体积的该 溶液时,下列物理量不随所取体积的多少而变化的是
溶液时,下列物理量不随所取体积的多少而变化的是______ 。
a.溶液中 的物质的量 b.溶液的浓度
的物质的量 b.溶液的浓度
c.溶液中 的数目 d.溶液的密度
的数目 d.溶液的密度
(6)下列操作中,会造成溶液浓度有何变化(填偏高,偏低,无影响)。
①定容时,俯视刻度线________ 。
②没有洗涤烧杯和玻璃棒_______ 。
③配制前容量瓶中残留少量蒸馏水______ 。
④摇匀后,发现液面低于刻度线_______ 。
⑤用天平称量时, 和砝码位置放颠倒了
和砝码位置放颠倒了_____ 。
⑥未冷却至室温就开始定容________ 。
(7)若需要0.05mol/L的 ,可用量筒量取
,可用量筒量取____ mL所配 溶液。
溶液。
 和
和 是两种常见的钠盐。
是两种常见的钠盐。向
 和
和 的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
的混合溶液中逐滴滴加盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
(1)OA段发生反应的离子方程式:
(2)原溶液中碳酸钠和碳酸氢钠的物质的量之比为
Ⅱ.实验室中需0.2 mol/L的
 溶液80 mL,请回答下列问题。
溶液80 mL,请回答下列问题。(3)配制上述溶液所需的
 固体,其质量是
固体,其质量是(4)实验时下图所示操作的先后顺序为

(5)取用任意体积的该
 溶液时,下列物理量不随所取体积的多少而变化的是
溶液时,下列物理量不随所取体积的多少而变化的是a.溶液中
 的物质的量 b.溶液的浓度
的物质的量 b.溶液的浓度c.溶液中
 的数目 d.溶液的密度
的数目 d.溶液的密度(6)下列操作中,会造成溶液浓度有何变化(填偏高,偏低,无影响)。
①定容时,俯视刻度线
②没有洗涤烧杯和玻璃棒
③配制前容量瓶中残留少量蒸馏水
④摇匀后,发现液面低于刻度线
⑤用天平称量时,
 和砝码位置放颠倒了
和砝码位置放颠倒了⑥未冷却至室温就开始定容
(7)若需要0.05mol/L的
 ,可用量筒量取
,可用量筒量取 溶液。
溶液。
您最近一年使用:0次
2024-02-14更新
|
65次组卷
|
2卷引用:天津市第四十二中学2023-2024学年高一上学期第二次月考化学试题



