名校
1 . 某溶液中含有 、
、 、
、 、
、 、M,且离子的物质的量之比为2:3:1:3:1,则微粒M为
、M,且离子的物质的量之比为2:3:1:3:1,则微粒M为
 、
、 、
、 、
、 、M,且离子的物质的量之比为2:3:1:3:1,则微粒M为
、M,且离子的物质的量之比为2:3:1:3:1,则微粒M为A. | B.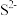 | C.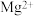 | D. |
您最近一年使用:0次
2022-08-25更新
|
264次组卷
|
6卷引用:重庆市实验中学校等七校2023-2024学年高一上学期11月期中联考化学试题
名校
解题方法
2 . 某学习小组为认识铁及其化合物的性质做了如下一组综合实验,根据实验流程回答相关问题:
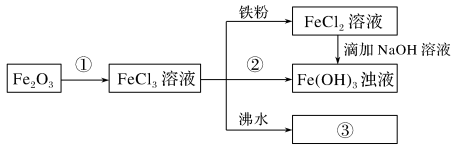
(1)物质②为_______ 。
(2)请写出FeCl3与铁粉反应的离子方程式_______ 。
(3)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为_______ ,此过程中发生的氧化还原反应为(用化学方程式表达)_______ 。
(4)检验溶液中Fe3+存在的试剂是_______ ,证明Fe3+存在的现象是_______ 。

(1)物质②为
(2)请写出FeCl3与铁粉反应的离子方程式
(3)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为
(4)检验溶液中Fe3+存在的试剂是
您最近一年使用:0次
名校
解题方法
3 . 下列物质不能由化合反应制取的是
| A.Fe(OH)3 | B.Al(OH)3 | C.FeCl3 | D.FeCl2 |
您最近一年使用:0次
2022-07-13更新
|
462次组卷
|
12卷引用:重庆实验外国语学校2022-2023学年高一上学期1月期末考试化学试题
重庆实验外国语学校2022-2023学年高一上学期1月期末考试化学试题【全国百强校】黑龙江省哈尔滨市第三中学2018-2019学年高一上学期期末考试化学试题天津市耀华中学2019-2020学年度高一上学期期末考试化学试题天津市耀华中学2019-2020学年高一下学期期末化学试题吉林省吉化第一高级中学校2020-2021学年高一上学期第一次月考化学试题(已下线)练习9 铁的多样性-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)上海市川沙中学2021-2022学年高一下学期期末考试化学试题云南省玉溪市通海县第一中学2021—2022学年高一上学期期末考试化学试题广东实验中学2022-2023学年高一上学期12月月考化学试题上海南汇中学2022-2023学年高一下学期期末考试化学试题吉林省梅河口市第五中学2022-2023学年高一下学期期末期末考试化学试题辽宁省鞍山市台安县高级中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
4 . 按下列要求所发生的化学反应,其离子方程式的书写不正确的是
A.向Na2SiO3溶液中通入过量CO2气体: 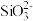 +CO2 +H2O=H2SiO3 ↓+ +CO2 +H2O=H2SiO3 ↓+ |
B.向Ba(OH)2溶液中滴入NaHSO4溶液至Ba2+恰好完全沉淀: H++ +Ba2++OH- =BaSO4↓+H2O +Ba2++OH- =BaSO4↓+H2O |
C.向AlCl3溶液中加入过量氨水: Al3+ + 3NH3·H2O=Al(OH)3↓+ 3 |
D.将过量铁粉加入稀硝酸中(还原产物只有NO): 3Fe+ 8H+ + 2 = 3Fe2++ 2NO↑+ 4H2O = 3Fe2++ 2NO↑+ 4H2O |
您最近一年使用:0次
名校
5 . 下列溶液中离子能大量存在的是
A.Mg2+、Fe2+、Cl-、 | B.Na+、 、Cl-、OH- 、Cl-、OH- |
C.K+、 、Mg2+、H+ 、Mg2+、H+ | D.Cu2+、SCN-、Na+、Fe3+ |
您最近一年使用:0次
2022-04-23更新
|
190次组卷
|
2卷引用:重庆市万州第二高级中学2021-2022学年高一下学期期中考试化学试题
6 . 某研究小组利用某硫酸厂产生的烧渣(主要含Fe2O3、FeO、SiO2,其中SiO2及少量其他杂质不参与反应且难溶于水)制备绿矾(FeSO4•7H2O),其流程如图所示:
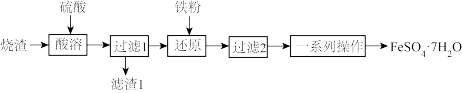
(1)“滤渣1”的主要成分是____ (填化学式)。
(2)“还原”时,主要反应的离子方程式为____ 。
(3)检验“过滤2”所得滤液中不含Fe3+的最佳试剂是____ (填化学式)。
(4)“一系列操作”中包含的操作依次有蒸发浓缩、____ 、过滤、洗涤、干燥等。
(5)利用绿矾配制的FeSO4溶液制备Fe(OH)2沉淀,其实验装置如图所示。植物油层的目的是____ 。若将制得的Fe(OH)2沉淀露置于空气中,则最终变为红褐色,则反应的化学方程式为____ 。


(1)“滤渣1”的主要成分是
(2)“还原”时,主要反应的离子方程式为
(3)检验“过滤2”所得滤液中不含Fe3+的最佳试剂是
(4)“一系列操作”中包含的操作依次有蒸发浓缩、
(5)利用绿矾配制的FeSO4溶液制备Fe(OH)2沉淀,其实验装置如图所示。植物油层的目的是

您最近一年使用:0次
2022-04-06更新
|
280次组卷
|
2卷引用:重庆实验外国语学校2022-2023学年高一上学期1月期末考试化学试题
名校
7 . 某校研究性学习小组用一些大部分已经锈蚀(成分为Fe2O3)的废铁屑制备绿矾(FeSO4·7H2O),实验操作过程如图:
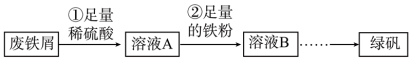
已知:杂质不溶于稀硫酸。
请回答下列问题:
(1)铁的原子结构示意图为_______ 。
(2)步骤①中,稀硫酸与 Fe2O3反应的离子方程式为_______ ,废铁屑用硫酸处理后,还含有不溶性杂质,为获取澄清的A溶液,需进行的操作名称是_______ 。
(3)步骤②中溶液A与铁粉反应的离子方程式为_______ 。
(4)检验溶液 B 中是否还存在杂质金属阳离子的方法是_______ 。

已知:杂质不溶于稀硫酸。
请回答下列问题:
(1)铁的原子结构示意图为
(2)步骤①中,稀硫酸与 Fe2O3反应的离子方程式为
(3)步骤②中溶液A与铁粉反应的离子方程式为
(4)检验溶液 B 中是否还存在杂质金属阳离子的方法是
您最近一年使用:0次
名校
8 . 下列除去杂质(括号中的物质为杂质)的方法中,正确的是
| A.Cu(Fe):加足量FeCl3溶液 | B.CO2(HCl):通过Na2CO3溶液 |
| C.FeCl3溶液(FeCl2):通入适量Cl2 | D.Cl2(O2):通过灼热的铜丝网 |
您最近一年使用:0次
2022-04-05更新
|
675次组卷
|
7卷引用:重庆市南开中学校2021--2022学年高一上学期期末化学试题
9 . 铁及其化合物在生产生活中具有重要的应用,高铁酸钾(K2FeO4)是一种高效水处理剂,紫色固体。已知K2FeO4具有下列性质:①可溶于水,溶液为紫色,微溶于浓KOH溶液;②在0℃~5℃、强碱性溶液中比较稳定。某实验小组制备并探究K2FeO4性质,回答下列问题:
(1)制备K2FeO4(夹持装置略):

①A为氯气发生装置,其中仪器a的名称是_______ ,固体甲的化学式为_______ ,浓盐酸在该反应中表现的性质为_______ ;将Cl2通过装置B可除去杂质,以免影响实验,B中的试剂是_______ 。
②C为制备K2FeO4的装置,采用冰水浴的原因是_______ ,KClO与Fe(OH)3在碱性环境中反应生成K2FeO4,该氧化还原反应中氧化剂与还原剂的物质的量之比为_______ 。
③D为尾气处理装置,发生反应的离子方程式为_______ 。
(2)探究K2FeO4的性质:
根据实验1和2的现象,写出K2FeO4在酸性条件下发生反应的离子方程式_______ 。
(1)制备K2FeO4(夹持装置略):

①A为氯气发生装置,其中仪器a的名称是
②C为制备K2FeO4的装置,采用冰水浴的原因是
③D为尾气处理装置,发生反应的离子方程式为
(2)探究K2FeO4的性质:
| 实验1 | 取少量C中紫色溶液,加入过量稀硫酸,迅速产生大量气体,该气体能使带火星的木条复燃。 |
| 实验2 | 取实验1中的溶液,滴加KSCN溶液至过量,溶液呈红色。 |
您最近一年使用:0次
2022-04-04更新
|
655次组卷
|
2卷引用:重庆市第八中学校2021-2022学年高一上学期期末考试化学试题
名校
10 . 下列离子方程式书写正确的是
A.AlCl3溶液中加入过量氨水:Al3++4NH3•H2O= +4 +4 +2H2O +2H2O |
| B.FeCl3溶液中加入铁粉:Fe3++Fe=2Fe2+ |
C.Na2CO3溶液中滴加少量盐酸: +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| D.FeBr2溶液中通入足量的氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
您最近一年使用:0次



