19-20高一·全国·课时练习
名校
1 . 某工程师为了从腐蚀废液(含有 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,准备采用如图所示方案:
溶液,准备采用如图所示方案:
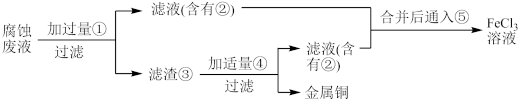
(1)请写出上述实验中加入或生成的有关物质的化学式:①________ ,②______ ,③_______ ,④________ ,⑤________ 。
(2)请写出相关反应的化学方程式:__________ 。
 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,准备采用如图所示方案:
溶液,准备采用如图所示方案:
(1)请写出上述实验中加入或生成的有关物质的化学式:①
(2)请写出相关反应的化学方程式:
您最近一年使用:0次
2020-10-02更新
|
644次组卷
|
3卷引用:第3章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)
(已下线)第3章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物 教材帮辽宁省沈阳市浑南区东北育才学校2023届高三一模化学试题
2 . 硫酸亚铁晶体(FeSO4•7H2O)在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如图所示:

请回答下列问题:
(1)向步骤①的滤液中滴加KSCN溶液后,溶液变为红色,则该滤液中含有___ (填离子符号),证明该补血剂__ (填“已经”或“没有”)变质。
(2)步骤②中反应的离子方程式:___ 。
(3)步骤③中反应的离子方程式:___ 。
(4)步骤④中一系列的操作步骤;过滤、__ 、灼烧、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为__ g。(用含a的代数式表示)

请回答下列问题:
(1)向步骤①的滤液中滴加KSCN溶液后,溶液变为红色,则该滤液中含有
(2)步骤②中反应的离子方程式:
(3)步骤③中反应的离子方程式:
(4)步骤④中一系列的操作步骤;过滤、
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为
您最近一年使用:0次
3 . 在一种酸性溶液中可能存在Fe3+、NO 、Cl-、I-中的一种或几种,向该溶液中加入溴水,再加入淀粉溶液,溶液变蓝。由此可推断溶液中( )
、Cl-、I-中的一种或几种,向该溶液中加入溴水,再加入淀粉溶液,溶液变蓝。由此可推断溶液中( )
 、Cl-、I-中的一种或几种,向该溶液中加入溴水,再加入淀粉溶液,溶液变蓝。由此可推断溶液中( )
、Cl-、I-中的一种或几种,向该溶液中加入溴水,再加入淀粉溶液,溶液变蓝。由此可推断溶液中( )| A.一定含有I-,不能确定是否含有Cl- |
B.可能含有NO 、Cl-和I- 、Cl-和I- |
C.可能含有NO |
| D.一定含有Fe3+ |
您最近一年使用:0次
2020-09-23更新
|
272次组卷
|
2卷引用:高一必修第一册(鲁科2019)第3章 章末综合检测卷
19-20高一·全国·课时练习
名校
解题方法
4 . 一些高档茶叶、点心等食品的包装盒中有一个小袋,将小袋打开,可以看到黑色粉末,部分已变成棕褐色。将上述粉末溶于稀盐酸,取上层清液,滴入几滴氯水,再滴加KSCN溶液,溶液立即变为红色。下列说法不正确的是
| A.小袋中原来装有氧化铁 | B.小袋中原来装有铁粉 |
| C.该黑色粉末不可食用 | D.该黑色粉末做抗氧化剂 |
您最近一年使用:0次
2020-09-23更新
|
693次组卷
|
3卷引用:【知识图鉴】单元讲练测必修第一册第三单元02基础练
19-20高二下·四川绵阳·期中
名校
5 . 配制FeCl3溶液时,将FeCl3固体溶解在较浓的盐酸中,再加水稀释。下列说法错误的是
| A.较浓盐酸可有效抑制Fe3+水解 |
| B.稀释过程中FeCl3水解程度增大,c(H+)增大 |
| C.FeCl3溶液中加入NaHCO3溶液有气体和红褐色沉淀产生 |
| D.FeCl3溶液中滴加KSCN溶液,溶液出现血红色 |
您最近一年使用:0次
解题方法
6 . (1)用 配制
配制 溶液时,为防止
溶液时,为防止 被氧化,需加入稀硫酸和稍过量的
被氧化,需加入稀硫酸和稍过量的____ 。
(2)在 溶液中滴入稀硫酸,再滴入几滴
溶液中滴入稀硫酸,再滴入几滴 溶液,溶液立即变黄。上述反应的离子方程式为
溶液,溶液立即变黄。上述反应的离子方程式为_____ 。
(3)为检验(2)中的氧化产物,甲同学取少许反应后的溶液,加入______ 溶液,溶液变血红色,证明氧化产物为 ;乙同学取少许反应后的溶液,加入
;乙同学取少许反应后的溶液,加入____ 溶液,溶液变蓝,证明氧化产物为 ,该反应的离子方程式为
,该反应的离子方程式为_____________ 。
(4)为证明(2)中反应后的溶液中仍存在 ,可向其中滴加
,可向其中滴加____ 溶液。
 配制
配制 溶液时,为防止
溶液时,为防止 被氧化,需加入稀硫酸和稍过量的
被氧化,需加入稀硫酸和稍过量的(2)在
 溶液中滴入稀硫酸,再滴入几滴
溶液中滴入稀硫酸,再滴入几滴 溶液,溶液立即变黄。上述反应的离子方程式为
溶液,溶液立即变黄。上述反应的离子方程式为(3)为检验(2)中的氧化产物,甲同学取少许反应后的溶液,加入
 ;乙同学取少许反应后的溶液,加入
;乙同学取少许反应后的溶液,加入 ,该反应的离子方程式为
,该反应的离子方程式为(4)为证明(2)中反应后的溶液中仍存在
 ,可向其中滴加
,可向其中滴加
您最近一年使用:0次
解题方法
7 . 铁、铝是重要的金属材料,铁、铝及其化合物有非常重要的用途。
(1)下列说法正确的是____________ (填序号)。
①配制氯化铁溶液,先将FeCl3固体溶于较浓盐酸,再用蒸馏水稀释到所需浓度
②FeCl2只能通过置换反应生成,FeCl3只能通过化合反应生成
③利用氯水和KSCN溶液可以检验Fe3+中有无Fe2+
④加热蒸干Fe2(SO4)3溶液获得Fe2(SO4)3固体
⑤由于金属铝性质稳定,所以Al在空气中能稳定存在
(2)高铁酸钾 (K2FeO4)是一种高效多功能水处理剂,其作用原理为___________ 。
(3)以铝土矿(主要成分为Al2O3、Fe2O3和SiO2)为原料制备铝的一种工艺流程如下:

①滤渣主要成分为__________________ 。
②在实验室灼烧操作应选择的主要实验仪器为__________________ 。
③反应Ⅱ中,加入NaHCO3一段时间才有沉淀生成,写出加入少量NaHCO3时发生反应的离子方程式:______________________________________________ 。
(4)已知25℃时Ksp[Cu(OH)2]=2.2×10-20 mol3·L-3,Ksp[Fe(OH)3]=4.0×10-38 mol4·L-4,Ksp[Al(OH)3]=1×10-33 mol4·L-4。
①在25℃下,向浓度均为 0.1mol/L的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成沉淀
0.1mol/L的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成沉淀______ (填化学式)。
②溶液中某离子物质的量浓度小于等于1.0×10-5mol/L时,可认为该离子已沉淀完全。现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测得c(Al3+)=0.2mol/L。此时所得沉淀中___________ (填“含有”或“不含”)Al(OH)3。
(1)下列说法正确的是
①配制氯化铁溶液,先将FeCl3固体溶于较浓盐酸,再用蒸馏水稀释到所需浓度
②FeCl2只能通过置换反应生成,FeCl3只能通过化合反应生成
③利用氯水和KSCN溶液可以检验Fe3+中有无Fe2+
④加热蒸干Fe2(SO4)3溶液获得Fe2(SO4)3固体
⑤由于金属铝性质稳定,所以Al在空气中能稳定存在
(2)高铁酸钾 (K2FeO4)是一种高效多功能水处理剂,其作用原理为
(3)以铝土矿(主要成分为Al2O3、Fe2O3和SiO2)为原料制备铝的一种工艺流程如下:

①滤渣主要成分为
②在实验室灼烧操作应选择的主要实验仪器为
③反应Ⅱ中,加入NaHCO3一段时间才有沉淀生成,写出加入少量NaHCO3时发生反应的离子方程式:
(4)已知25℃时Ksp[Cu(OH)2]=2.2×10-20 mol3·L-3,Ksp[Fe(OH)3]=4.0×10-38 mol4·L-4,Ksp[Al(OH)3]=1×10-33 mol4·L-4。
①在25℃下,向浓度均为
 0.1mol/L的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成沉淀
0.1mol/L的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成沉淀②溶液中某离子物质的量浓度小于等于1.0×10-5mol/L时,可认为该离子已沉淀完全。现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测得c(Al3+)=0.2mol/L。此时所得沉淀中
您最近一年使用:0次
2020-09-14更新
|
1200次组卷
|
3卷引用:高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三章素养检测
18-19高一·全国·课时练习
名校
解题方法
8 . 已知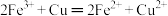 。向
。向 、
、 的混合溶液中加入一定量的铁粉,充分反应后仍有固体存在,则下列判断不正确的是
的混合溶液中加入一定量的铁粉,充分反应后仍有固体存在,则下列判断不正确的是
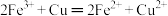 。向
。向 、
、 的混合溶液中加入一定量的铁粉,充分反应后仍有固体存在,则下列判断不正确的是
的混合溶液中加入一定量的铁粉,充分反应后仍有固体存在,则下列判断不正确的是A.加入 溶液可能变红色 溶液可能变红色 | B.溶液中一定含 |
C.剩余固体中一定含 | D.溶液中一定含 |
您最近一年使用:0次
2020-09-10更新
|
503次组卷
|
3卷引用:第03章 物质在水溶液中的行为 (B卷能力提升卷) -2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)
(已下线)第03章 物质在水溶液中的行为 (B卷能力提升卷) -2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第1节 铁的多样性福建省莆田第二十五中学2021届高三上学期月考二化学试题
名校
9 . 为除去下列括号内的杂质,所选用的试剂或方法不正确的是
A. 溶液( 溶液( ):加入过量铁粉,过滤 ):加入过量铁粉,过滤 |
B. 溶液( 溶液( ):通入过量的 ):通入过量的 气体 气体 |
C. 固体( 固体( ):加入过量的 ):加入过量的 溶液,过滤 溶液,过滤 |
D. 溶液( 溶液( ):加入适量的 ):加入适量的 溶液 溶液 |
您最近一年使用:0次
2020-09-08更新
|
1399次组卷
|
2卷引用:人教版(2019)高一必修第一册 第三章素养检测
名校
10 . 下列有关铁及其化合物的说法正确的是
A.铁的氧化物有 、 、 、 、 ,它们都是黑色的固体 ,它们都是黑色的固体 |
B. 、 、 的混合物可能是灰绿色 的混合物可能是灰绿色 |
C.鉴别 中混有的 中混有的 ,可先加入氯水,再加入 ,可先加入氯水,再加入 溶液 溶液 |
| D.生铁含碳量低于钢 |
您最近一年使用:0次
2020-09-08更新
|
1129次组卷
|
4卷引用:人教版(2019)高一必修第一册 第三章素养检测



