名校
解题方法
1 . 印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费。可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5 mol/L,FeCl2 3.0 mol/L,FeCl3 1.0 mol/L,HCl 3.0 mol/L。取废腐蚀液200 mL按如下流程在实验室进行实验:

回答下列问题:
(1)取少量废腐蚀液于试管中,滴入1~2滴KSCN溶液,若溶液显_______ (填“红色”或“蓝色”、“紫色”),证明废液含有FeCl3。
(2)上述方法获得的铜粉中含有杂质,除杂所需试剂是_______ (填化学式)。
(3)操作Ⅰ是_______ ,该操作需用到的玻璃仪器有烧杯、普通漏斗和_______ 。
(4)FeCl2溶液中通入氯气,发生反应的离子方程式为_______ 。
(5)已知氧化性:Fe3+>Cu2+ >H+>Fe2+;往上述200 mL废腐蚀液中加入20g铁粉,边加边搅拌,是否有氢气产生_______ (填“是”、“否”)。

回答下列问题:
(1)取少量废腐蚀液于试管中,滴入1~2滴KSCN溶液,若溶液显
(2)上述方法获得的铜粉中含有杂质,除杂所需试剂是
(3)操作Ⅰ是
(4)FeCl2溶液中通入氯气,发生反应的离子方程式为
(5)已知氧化性:Fe3+>Cu2+ >H+>Fe2+;往上述200 mL废腐蚀液中加入20g铁粉,边加边搅拌,是否有氢气产生
您最近一年使用:0次
名校
2 . 石墨在材料领域有重要应用,某初级石墨中含 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
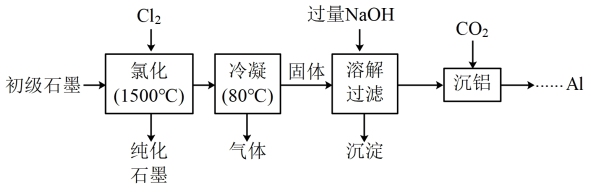
已知:①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
② 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。
(1)“氯化”时,先向反应器中通入 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是_______ 。
(2)“冷凝”后,所得“气体"的成分有 和
和_______ (填化学式)。
(3)“溶解过滤”时,加过量NaOH溶液的目的是_______ ;取少量滤液于试管中,_______ (实验操作及现象),证明沉淀已完全。
(4)“沉铝”得到的产物为 ,工业上由
,工业上由 得到Al,需发生两步反应,写出方程式:
得到Al,需发生两步反应,写出方程式: 、
、_______ 。
(5)写出Al的一种用途_______ 。
(6)100kg初级石墨最多可获得Al的质量为_______ kg。
 (7.8%)、
(7.8%)、 (5.1%)和
(5.1%)和 (3.1%)等杂质,提纯与综合利用工艺流程如下:
(3.1%)等杂质,提纯与综合利用工艺流程如下:
已知:①氯化后,石墨中氧化物杂质均转变为相应的氯化物;
②
 的沸点为57.6℃,金属氯化物的沸点均高于150℃。
的沸点为57.6℃,金属氯化物的沸点均高于150℃。(1)“氯化”时,先向反应器中通入
 一段时间,再加热,主要目的是
一段时间,再加热,主要目的是(2)“冷凝”后,所得“气体"的成分有
 和
和(3)“溶解过滤”时,加过量NaOH溶液的目的是
(4)“沉铝”得到的产物为
 ,工业上由
,工业上由 得到Al,需发生两步反应,写出方程式:
得到Al,需发生两步反应,写出方程式: 、
、(5)写出Al的一种用途
(6)100kg初级石墨最多可获得Al的质量为
您最近一年使用:0次
2022-07-05更新
|
375次组卷
|
3卷引用:广东省东莞市2021-2022学年高一下学期期末教学质量检查化学试题
3 . 已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验。
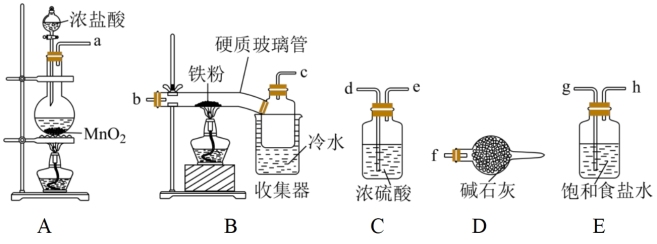
(1)装置接口的连接顺序为a→_______ 。
(2)B中收集器里盛放冷水的作用是_______ 。D中碱石灰的作用是_______ 、_______ 。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸,充分反应后,进行如下实验:
固体混合物 淡黄色溶液
淡黄色溶液 淡红色溶液
淡红色溶液 深红色溶液
深红色溶液 红色褪去
红色褪去
①试剂X为_______ (填化学式)。
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是_______ 。
(4)该小组同学对上述溶液红色褪去的原因进行探究。
①取褪色后的溶液三份,分别进行以下实验,研究溶液中存在的微粒。
a.一份中滴加FeCl3溶液无明显变化,说明_______ ;
b.另一份滴加试剂X,溶液出现红色,说明_______ ;
c.还有一份滴加稀盐酸和BaCl2溶液,产生白色沉淀,说明_______ 。
②另取FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。实验②的目的是_______ ;得出结论:_______ 。

(1)装置接口的连接顺序为a→
(2)B中收集器里盛放冷水的作用是
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸,充分反应后,进行如下实验:
固体混合物
 淡黄色溶液
淡黄色溶液 淡红色溶液
淡红色溶液 深红色溶液
深红色溶液 红色褪去
红色褪去①试剂X为
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是
(4)该小组同学对上述溶液红色褪去的原因进行探究。
①取褪色后的溶液三份,分别进行以下实验,研究溶液中存在的微粒。
a.一份中滴加FeCl3溶液无明显变化,说明
b.另一份滴加试剂X,溶液出现红色,说明
c.还有一份滴加稀盐酸和BaCl2溶液,产生白色沉淀,说明
②另取FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。实验②的目的是
您最近一年使用:0次
2022-07-02更新
|
1022次组卷
|
3卷引用:上海市控江中学2021-2022学年高一下学期期末考试化学试题
名校
解题方法
4 . A、B、C、D是4种中学化学常见的纯净物,其中A为单质。A、B、C、D存在如图所示转化关系:
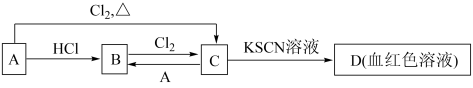
回答下列问题:
(1)C的化学式为_______ 。
(2)A在氧气中燃烧的产物_______ (填“是”或“不是”)碱性氧化物。
(3)写出B →C的化学方程式:_______ 。
(4)往B的水溶液中滴加NaOH溶液,现象为_______ 。

回答下列问题:
(1)C的化学式为
(2)A在氧气中燃烧的产物
(3)写出B →C的化学方程式:
(4)往B的水溶液中滴加NaOH溶液,现象为
您最近一年使用:0次
2022-07-01更新
|
637次组卷
|
4卷引用:云南师范大学附属中学2023届高考适应性月考卷(一)化学试题
名校
5 . 常见金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间存在如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。其中B是地壳中含量居第一的金属元素。请回答下列问题:

(1)气体丙的电子式为_______ 。
(2)写出下列反应的离子方程式:③_______ ;⑤_______ 。
(3)金属C在一定条件下与水蒸气反应的化学方程式为_______ 。
(4)溶液F中加入溶液D后的现象是_______ ,所发生反应的化学方程式为_______ ,_______ 。
(5)溶液F放置于空气中容易变质,检验溶液F是否变质的方法是_______ 。

(1)气体丙的电子式为
(2)写出下列反应的离子方程式:③
(3)金属C在一定条件下与水蒸气反应的化学方程式为
(4)溶液F中加入溶液D后的现象是
(5)溶液F放置于空气中容易变质,检验溶液F是否变质的方法是
您最近一年使用:0次
解题方法
6 . 某小组用下图所示装置(夹持装置省略)制备 ,并探究
,并探究 与
与 溶液的反应。
溶液的反应。

(1)盛放70%硫酸的仪器名称是_______ ,装置I中反应的化学方程式为_______ 。
(2)多孔球泡的作用有防倒吸和_______ 。
(3)向装置I中加入70%硫酸,待装置II中溶液由黄色变为浅绿色后关闭活塞。有同学认为此时该溶液中含有 ,并进行以下实验验证:
,并进行以下实验验证:
(4)为检验装置II中生成的 ,需进行的操作和现象为
,需进行的操作和现象为_______ 。
(5) 浓度的测定:
浓度的测定:
①取装置II中反应后的溶液25.00mL于锥形瓶中,加入少量稀硫酸酸化后,逐渐滴加 的
的 溶液,至恰好完全反应,记录消耗的
溶液,至恰好完全反应,记录消耗的 溶液的体积。重复上述操作2~3次,平均消耗
溶液的体积。重复上述操作2~3次,平均消耗 溶液20.00mL。发生的反应为:
溶液20.00mL。发生的反应为: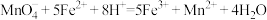 。则反应后装置II中
。则反应后装置II中 的浓度为
的浓度为_______ 。
②研究小组同学认为根据以上步骤测定的 浓度偏高,理由是
浓度偏高,理由是_______ 。
 ,并探究
,并探究 与
与 溶液的反应。
溶液的反应。
(1)盛放70%硫酸的仪器名称是
(2)多孔球泡的作用有防倒吸和
(3)向装置I中加入70%硫酸,待装置II中溶液由黄色变为浅绿色后关闭活塞。有同学认为此时该溶液中含有
 ,并进行以下实验验证:
,并进行以下实验验证:| 操作 | 现象 | 结论 |
取少量装置II中溶液于试管中,先滴加 溶液,振荡 溶液,振荡 | 先无明显现象,加入 溶液后,现象是 溶液后,现象是 | 溶液中含有 |
 ,需进行的操作和现象为
,需进行的操作和现象为(5)
 浓度的测定:
浓度的测定:①取装置II中反应后的溶液25.00mL于锥形瓶中,加入少量稀硫酸酸化后,逐渐滴加
 的
的 溶液,至恰好完全反应,记录消耗的
溶液,至恰好完全反应,记录消耗的 溶液的体积。重复上述操作2~3次,平均消耗
溶液的体积。重复上述操作2~3次,平均消耗 溶液20.00mL。发生的反应为:
溶液20.00mL。发生的反应为: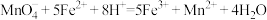 。则反应后装置II中
。则反应后装置II中 的浓度为
的浓度为②研究小组同学认为根据以上步骤测定的
 浓度偏高,理由是
浓度偏高,理由是
您最近一年使用:0次
21-22高一下·上海浦东新·期末
名校
7 . 为探索工业含铝、铁、铜合金废料的再利用,某同学实设计的回收利用方案如下:
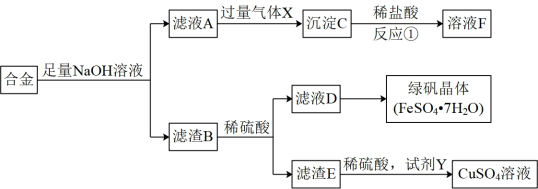
(1)滤渣B的主要成分为_______ ,溶液F的主要成分为_______ 。
(2)检验滤液D是否含有 的方法为
的方法为_______ 。
(3)从滤液D得到绿矾晶体,须进行的操作为:_______ 、_______ 、过滤洗涤、干燥。
(4)试剂Y可能为_______ 。
A.NO B. C.
C. D.
D.
与直接用浓硫酸与E反应制备 相比,用稀硫酸和试剂Y更符合“绿色化学”,的要求,原因是
相比,用稀硫酸和试剂Y更符合“绿色化学”,的要求,原因是_______ 、_______ 。
(5)若气体X为 ,请写出“滤液A”与过量气体X反应的离子方程式:
,请写出“滤液A”与过量气体X反应的离子方程式:_______ 。

(1)滤渣B的主要成分为
(2)检验滤液D是否含有
 的方法为
的方法为(3)从滤液D得到绿矾晶体,须进行的操作为:
(4)试剂Y可能为
A.NO B.
 C.
C. D.
D.
与直接用浓硫酸与E反应制备
 相比,用稀硫酸和试剂Y更符合“绿色化学”,的要求,原因是
相比,用稀硫酸和试剂Y更符合“绿色化学”,的要求,原因是(5)若气体X为
 ,请写出“滤液A”与过量气体X反应的离子方程式:
,请写出“滤液A”与过量气体X反应的离子方程式:
您最近一年使用:0次
名校
解题方法
8 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态及其含量,设计并进行了如下实验:
【查阅资料】
Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为 价。
价。
实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)试剂1是_______ ,试剂2是_______ (写出物质名称)。
(2)加入试剂2后溶液变为浅红色,此现象说明溶液①中含有_______ (填微粒符号)。
(3)能证明溶液①中含有 的实验现象是
的实验现象是_______ 。
(4)写出上述条件下 与
与 发生反应的离子方程式:
发生反应的离子方程式:_______ 。
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的 与
与 发生了化学反应。甲同学猜测的理论依据是
发生了化学反应。甲同学猜测的理论依据是_______ 。
实验Ⅱ.测定该补铁剂中铁元素的含量。

(6)计算每片该补铁剂含铁元素的质量为_______ g。
【查阅资料】
Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为
 价。
价。实验Ⅰ.检验该补铁剂中铁元素的价态。

(1)试剂1是
(2)加入试剂2后溶液变为浅红色,此现象说明溶液①中含有
(3)能证明溶液①中含有
 的实验现象是
的实验现象是(4)写出上述条件下
 与
与 发生反应的离子方程式:
发生反应的离子方程式:(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的
 与
与 发生了化学反应。甲同学猜测的理论依据是
发生了化学反应。甲同学猜测的理论依据是实验Ⅱ.测定该补铁剂中铁元素的含量。

(6)计算每片该补铁剂含铁元素的质量为
您最近一年使用:0次
21-22高一·全国·假期作业
9 . 已知:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验。请回答下列问题:
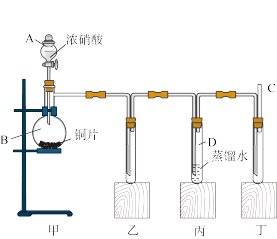
(1)装置甲中盛放浓硝酸的仪器A的名称是_______ 。
(2)实验过程中,装置乙、丙中出现的现象分别是:_______ 、_______ ;装置丙中的试管内发生反应的离子方程式为_______ 。
(3)为了探究NO的还原性,可以在装置丁的导气管C中通入一种气体,通入的这种气体的名称是_______ 。
(4)为了探究NO2的氧化性,取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为_______ 色,为了证明铁元素在该反应中的产物,可以再在溶液中滴加KSCN溶液,溶液变为_______ 色。

(1)装置甲中盛放浓硝酸的仪器A的名称是
(2)实验过程中,装置乙、丙中出现的现象分别是:
(3)为了探究NO的还原性,可以在装置丁的导气管C中通入一种气体,通入的这种气体的名称是
(4)为了探究NO2的氧化性,取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为
您最近一年使用:0次
名校
10 . 铝、铁是生产、生活中常见的金属,其合金与盐在各领域都有着广泛的应用。
(1)铝合金是一种建筑装潢材料,它具有坚硬、轻巧、耐用的特性。铝合金的下列性质与这些特性无关的是
(2)铝元素在周期表中的位置是_______ 。写出 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式_______ 。铁粉与水蒸气在高温条件下反应,生成的固态产物是_______ 。
(3)焊接金属时常用的焊接液为氯化铵,其作用是消除焊接金属表面的铁锈。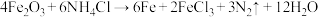 ;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为
;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为_______ 个,有同学认为,该反应产物中不应该有Fe生成,他的理由是(用化学方程式表示原因)_______ 。
(4)现有仪器和药品:试管和胶头滴管,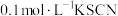 溶液、
溶液、 酸性
酸性 溶液、
溶液、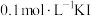 溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:
溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:
(1)铝合金是一种建筑装潢材料,它具有坚硬、轻巧、耐用的特性。铝合金的下列性质与这些特性无关的是
| A.不易生锈 | B.导电性好 | C.密度小 | D.硬度大 |
 与稀硫酸反应的离子方程式
与稀硫酸反应的离子方程式(3)焊接金属时常用的焊接液为氯化铵,其作用是消除焊接金属表面的铁锈。
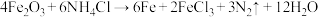 ;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为
;上述反应中当生成3.36L氮气(标准状况)时,转移的电子数为(4)现有仪器和药品:试管和胶头滴管,
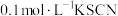 溶液、
溶液、 酸性
酸性 溶液、
溶液、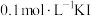 溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:
溶液、氯水等。请你设计一个简单实验,探究铁与稀硝酸完全反应后铁可能的价态,填写下列实验报告:| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试管中滴入几滴 溶液。 溶液。 | |
| 第二步 |  。 。 |
您最近一年使用:0次
2022-06-28更新
|
223次组卷
|
2卷引用:上海市宜川中学2021-2022学年高一下学期期末考试化学试题



