名校
1 . 高锰酸钾生产过程中产生的废锰渣(主要成分为 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
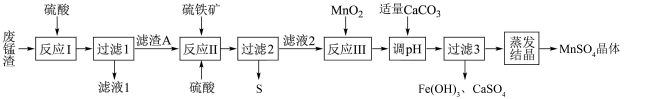
已知:硫铁矿的主要成分为二硫化亚铁( ,杂质不参与反应)。
,杂质不参与反应)。
回答下列问题:
(1)二硫化亚铁中S元素的化合价为_______ 。
(2)①滤渣A的主要成分是_______ (填化学式);
②“反应II”生成 、
、 等物质的离子方程式为
等物质的离子方程式为_______ 。
③“反应III”中还原剂和氧化剂物质的量之比为_______ ;
④“调 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为_______ 。
 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
已知:硫铁矿的主要成分为二硫化亚铁(
 ,杂质不参与反应)。
,杂质不参与反应)。回答下列问题:
(1)二硫化亚铁中S元素的化合价为
(2)①滤渣A的主要成分是
②“反应II”生成
 、
、 等物质的离子方程式为
等物质的离子方程式为③“反应III”中还原剂和氧化剂物质的量之比为
④“调
 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为
您最近一年使用:0次
名校
解题方法
2 . 某工厂的废金属屑中主要成分为 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如图
,为探索工业废料的再利用,某化学兴趣小组设计了如图 所示实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体
所示实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体 和胆矾晶体。
和胆矾晶体。
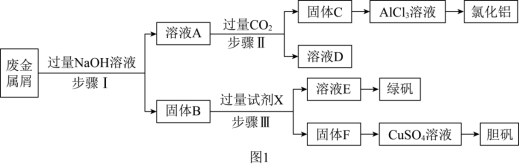
请回答下列问题:
(1)试剂X是_______ 。
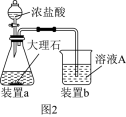
(2)在步骤Ⅱ过程,生成固体C发生的化学反应方程式为_______ ,若用如图 装置制取
装置制取 并通入溶液
并通入溶液 中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免沉淀减少,可采取的改进措施是
中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免沉淀减少,可采取的改进措施是_______ 。
(3)检验溶液 中的金属阳离子时,滴加
中的金属阳离子时,滴加_______ ,溶液无明显现象,说明溶液中不存在Fe3+,用离子方程式解释其可能的原因_______ 。
(4)由绿矾晶体(FeSO4•7H2O)固体配制240mL 0.10mol•L-1FeSO4溶液,需要用到的仪器有药匙、玻璃棒、量筒、烧杯、托盘天平、胶头滴管、_______ 。以下操作会导致所配溶液浓度偏低的是_______ 。
A.容量瓶中原有少量蒸馏水
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
C.定容时俯视刻度线
D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如图
,为探索工业废料的再利用,某化学兴趣小组设计了如图 所示实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体
所示实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体 和胆矾晶体。
和胆矾晶体。
请回答下列问题:
(1)试剂X是
(2)在步骤Ⅱ过程,生成固体C发生的化学反应方程式为
 装置制取
装置制取 并通入溶液
并通入溶液 中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免沉淀减少,可采取的改进措施是
中,一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免沉淀减少,可采取的改进措施是
(3)检验溶液
 中的金属阳离子时,滴加
中的金属阳离子时,滴加(4)由绿矾晶体(FeSO4•7H2O)固体配制240mL 0.10mol•L-1FeSO4溶液,需要用到的仪器有药匙、玻璃棒、量筒、烧杯、托盘天平、胶头滴管、
A.容量瓶中原有少量蒸馏水
B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
C.定容时俯视刻度线
D.定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
您最近一年使用:0次
2023-03-18更新
|
238次组卷
|
2卷引用:内蒙古鄂尔多斯市西四旗2023-2024学年高一上学期期末考试化学试题



