名校
解题方法
1 . 高纯氧化铁(Fe2O3)又称“引火铁”,可作催化剂,在现代工业上有广泛应用前景。以下是用废铁屑(含Fe单质约35%、Fe2O3约30%、Fe3O4约29%,含其它不含铁元素的杂质约6%)为原料,制备高纯氧化铁的生产流程示意图。

已知氨水呈碱性(主要成分NH3·H2O是一种碱):(NH4)2CO3溶液呈碱性,40℃以上易分解。
(1)写出高温时废铁屑中的Fe3O4与CO发生反应的化学方程式___________ 。
(2)加适量氨水的目的是___________ ,使加入的(NH4)2CO3能顺利发生复分解反应而生成FeCO3,则②处反应的化学方程式为___________ 。
(3)加入(NH4)2CO3后,该反应必须控制的条件是___________ 。
(4)用蒸馏水洗涤FeCO3的目的是除去表面附着的杂质,洗涤干净的标志是:取最后一次洗涤液,向其中加入少量的BaCl2溶液,___________ (填现象),即为洗涤干净。
(5)ag废铁经上述制备流程,可得到高纯氧化铁的质量最多是___________ g(用含a的式子表示)。

已知氨水呈碱性(主要成分NH3·H2O是一种碱):(NH4)2CO3溶液呈碱性,40℃以上易分解。
(1)写出高温时废铁屑中的Fe3O4与CO发生反应的化学方程式
(2)加适量氨水的目的是
(3)加入(NH4)2CO3后,该反应必须控制的条件是
(4)用蒸馏水洗涤FeCO3的目的是除去表面附着的杂质,洗涤干净的标志是:取最后一次洗涤液,向其中加入少量的BaCl2溶液,
(5)ag废铁经上述制备流程,可得到高纯氧化铁的质量最多是
您最近一年使用:0次
2 . 钛白粉( )广泛用于颜料、油漆和造纸等。某小组以钛铁矿粉(
)广泛用于颜料、油漆和造纸等。某小组以钛铁矿粉( )和金红石粉(
)和金红石粉( )为原料制备高纯度
)为原料制备高纯度 的流程如图所示:
的流程如图所示:

已知: 遇水极易水解。
遇水极易水解。
(1)在实验室进行操作A,装固体的仪器是___________ (填“坩埚”或“蒸发皿”)。
(2)写出钛铁矿与焦炭、氯气在高温下反应的化学方程式:___________ 。
(3)测定样品中 的纯度。取2.000g
的纯度。取2.000g 样品,在酸性条件下充分溶解,加入适量铝粉将
样品,在酸性条件下充分溶解,加入适量铝粉将 还原为T13+。过滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液,取25.00mL该溶液于锥形瓶中,滴入几滴KSCN溶液,用0.1000
还原为T13+。过滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液,取25.00mL该溶液于锥形瓶中,滴入几滴KSCN溶液,用0.1000
 标准溶液滴定,将
标准溶液滴定,将 转化成
转化成 ,消耗23.00mL标准溶液,杂质在整个过程中不反应。
,消耗23.00mL标准溶液,杂质在整个过程中不反应。
①该样品中 的质量分数为
的质量分数为___________ 。
②若开始时俯视滴定管读数,滴定终点时仰视滴定管读数,测得结果会___________ (填“偏高”“偏低”或“无影响”)。
(4)通过直接氯化法, 能用于制备
能用于制备 粗产品,其制备装置如图所示。
粗产品,其制备装置如图所示。

①若用 和浓盐酸制备氯气,写出装置A中反应的离子方程式:
和浓盐酸制备氯气,写出装置A中反应的离子方程式:___________ 。
②装置B中试剂的名称是___________ 。
③从环境保护角度考虑,本实验不足之处是___________ 。
 )广泛用于颜料、油漆和造纸等。某小组以钛铁矿粉(
)广泛用于颜料、油漆和造纸等。某小组以钛铁矿粉( )和金红石粉(
)和金红石粉( )为原料制备高纯度
)为原料制备高纯度 的流程如图所示:
的流程如图所示:
已知:
 遇水极易水解。
遇水极易水解。(1)在实验室进行操作A,装固体的仪器是
(2)写出钛铁矿与焦炭、氯气在高温下反应的化学方程式:
(3)测定样品中
 的纯度。取2.000g
的纯度。取2.000g 样品,在酸性条件下充分溶解,加入适量铝粉将
样品,在酸性条件下充分溶解,加入适量铝粉将 还原为T13+。过滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液,取25.00mL该溶液于锥形瓶中,滴入几滴KSCN溶液,用0.1000
还原为T13+。过滤并洗涤,将所得滤液和洗涤液合并配制成250mL溶液,取25.00mL该溶液于锥形瓶中,滴入几滴KSCN溶液,用0.1000
 标准溶液滴定,将
标准溶液滴定,将 转化成
转化成 ,消耗23.00mL标准溶液,杂质在整个过程中不反应。
,消耗23.00mL标准溶液,杂质在整个过程中不反应。①该样品中
 的质量分数为
的质量分数为②若开始时俯视滴定管读数,滴定终点时仰视滴定管读数,测得结果会
(4)通过直接氯化法,
 能用于制备
能用于制备 粗产品,其制备装置如图所示。
粗产品,其制备装置如图所示。
①若用
 和浓盐酸制备氯气,写出装置A中反应的离子方程式:
和浓盐酸制备氯气,写出装置A中反应的离子方程式:②装置B中试剂的名称是
③从环境保护角度考虑,本实验不足之处是
您最近一年使用:0次
解题方法
3 . 氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,另含少量杂质FeCO3和SiO2等)为原料制备高纯氧化镁的实验流程如下:
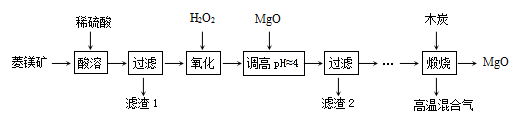
已知:滤渣2中除了过量的MgO外,还含有Fe(OH)3。
(1)酸溶时,MgCO3与稀硫酸反应的离子方程式为___________ 。
(2)滤渣1的化学式为___________ 。
(3)“氧化”流程的目的把Fe2+氧化成Fe3+,再调节pH把Fe3+除去,写出“氧化”流程的离子方程式为___________ 。
(4)高温煅烧过程中,同时存在以下反应: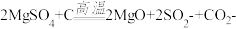 ;
;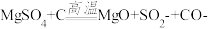 ;
;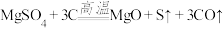 。利用下图装置对煅烧产生的气体进行连续分别吸收或收集(其中S蒸气在A管中沉积)。
。利用下图装置对煅烧产生的气体进行连续分别吸收或收集(其中S蒸气在A管中沉积)。
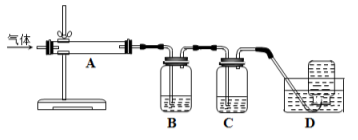
D中收集的气体是___________ (填化学式)。

已知:滤渣2中除了过量的MgO外,还含有Fe(OH)3。
(1)酸溶时,MgCO3与稀硫酸反应的离子方程式为
(2)滤渣1的化学式为
(3)“氧化”流程的目的把Fe2+氧化成Fe3+,再调节pH把Fe3+除去,写出“氧化”流程的离子方程式为
(4)高温煅烧过程中,同时存在以下反应:
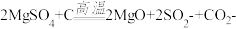 ;
;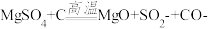 ;
;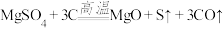 。利用下图装置对煅烧产生的气体进行连续分别吸收或收集(其中S蒸气在A管中沉积)。
。利用下图装置对煅烧产生的气体进行连续分别吸收或收集(其中S蒸气在A管中沉积)。
D中收集的气体是
您最近一年使用:0次



