12-13高三上·陕西咸阳·期末
1 . 有一铁粉和氧化铜的混合物6.96g,进行如下实验:
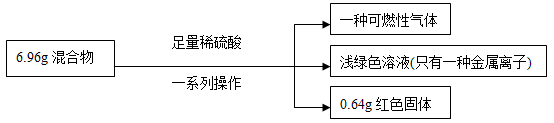
根据实验所得数据,关于混合物相关说法正确的是

根据实验所得数据,关于混合物相关说法正确的是
| A.生成气体质量为0.2g |
| B.原混合物中铁的质量分数无法计算 |
| C.实验中反应的H2SO4质量为10.78g |
| D.原混合物中铜元素的质量不一定为0.64g |
您最近半年使用:0次
名校
解题方法
2 . 现有CuO和Fe2O3组成的混合物a g,向其中加入2 mol·L-1的硫酸溶液50mL,恰好完全反应。若将a g该混合物在足量H2中加热,使其充分反应,冷却后剩余固体质量
| A.1.6 a g | B.(a-1.6) g | C.(a-3.2) g | D.a g |
您最近半年使用:0次
2016-12-09更新
|
1194次组卷
|
6卷引用:陕西省西安市远东第一中学2019届高三上学期期中考试化学试题
陕西省西安市远东第一中学2019届高三上学期期中考试化学试题(已下线)2011-2012学年河北省魏县第一中学高二下学期期中考试化学试卷(已下线)2013届浙江省温州市龙湾中学高三第一次月考化学试卷湖南省衡东县第一中学2017-2018第一学期高一化学期末考试广西南宁市第二中学2017-2018学年高一上学期期末考试化学试题浙江省舟山中学2021-2022学年高三下学期开学考试(返校考)化学试题
名校
3 . 将足量铁投入到200mLH2SO4和CuSO4的混和溶液中,充分反应后,产生H21.12L(标准状况),铁块的质量减轻了1.2g。求原溶液中c(H2SO4)及c(CuSO4)。(假设反应前后溶液的体积不变)
您最近半年使用:0次
14-15高三上·陕西西安·阶段练习
名校
4 . 铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是______________ ;Y与过量浓硝酸反应后溶液中含有的盐的化学式为___________ 。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___ 。
A.Mg2+B.Fe2+C.Al3+D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
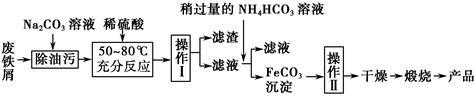
回答下列问题:
①操作Ⅰ的名称是________ ;操作Ⅱ的名称是________ ;操作Ⅱ的方法为_____________________ 。
②请写出生成FeCO3沉淀的离子方程式:____________________________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
A.Mg2+B.Fe2+C.Al3+D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:

回答下列问题:
①操作Ⅰ的名称是
②请写出生成FeCO3沉淀的离子方程式:
您最近半年使用:0次
2016-12-08更新
|
535次组卷
|
5卷引用:2015届陕西省西安一中高三上学期第二次模考试化学试卷
名校
解题方法
5 . 部分被氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共8.0 g,经如下处理:

下列说法正确的是

下列说法正确的是
| A.滤液A中的阳离子为Fe2+、Fe3+、H+ |
| B.该样品中Cu、O元素的质量比为10:l |
| C.V=448 |
| D.溶解样品时消耗H2SO4的物质的量为0.04 mol |
您最近半年使用:0次
2016-11-28更新
|
1100次组卷
|
3卷引用:陕西省西安市长安区第一中学2017-2018学年高一(实验班)上学期期中考试化学试题
6 . 由氧化亚铁、氧化铁、四氧化三铁组成的混合物ag,加入bmol/L的稀硫酸cL时固体恰好完全溶解。若将ag该混合物在足量的一氧化碳中加热充分反应,冷却后固体质量为
| A.16bc克 | B.(a-16bc)克 | C.(a-32bc)克 | D.无法计算 |
您最近半年使用:0次
名校
7 . 根据下列实验现象所得结论正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液未呈血红色 | 稀硝酸不能将Fe氧化为Fe3+ |
| B | 向NaAlO2溶液中滴入NaHCO3溶液 | 产生白色沉淀 | AlO2- 结合H+的能力比CO32-强 |
| C | 已知Cu2O+2H+=Cu2++Cu+H2O 将氢气还原氧化铜后所得红色固体 投入足量稀盐酸 | 溶液呈蓝色 | CuO的还原产物不全部是Cu |
| D | 将0.1mol•L-1 MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 | Cu(OH)2的溶度积比Mg(OH)2的大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2015-12-31更新
|
134次组卷
|
3卷引用:陕西省西安市第八十三中学高三年级2017-2018学年第三阶段考试化学试题
8 . 黄铜矿(主要成分CuFeS2)是提取铜的主要原料
已知:2CuFeS2+4O2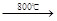 Cu2S+3SO2+2FeO炉渣产物Cu2S在1200℃高温下继续反应: 2Cu2S+3O2 → 2Cu2O+2SO2, 2Cu2O+Cu2S → 6Cu+SO2,假定各步反应都完全,完成下列计算:
Cu2S+3SO2+2FeO炉渣产物Cu2S在1200℃高温下继续反应: 2Cu2S+3O2 → 2Cu2O+2SO2, 2Cu2O+Cu2S → 6Cu+SO2,假定各步反应都完全,完成下列计算:
①由6 mol CuFeS2生成6 mol Cu,求消耗O2的物质的量 mol
②6 mol CuFeS2和14.25 mol O2反应,理论上可得到 mol铜
已知:2CuFeS2+4O2
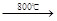 Cu2S+3SO2+2FeO炉渣产物Cu2S在1200℃高温下继续反应: 2Cu2S+3O2 → 2Cu2O+2SO2, 2Cu2O+Cu2S → 6Cu+SO2,假定各步反应都完全,完成下列计算:
Cu2S+3SO2+2FeO炉渣产物Cu2S在1200℃高温下继续反应: 2Cu2S+3O2 → 2Cu2O+2SO2, 2Cu2O+Cu2S → 6Cu+SO2,假定各步反应都完全,完成下列计算:①由6 mol CuFeS2生成6 mol Cu,求消耗O2的物质的量 mol
②6 mol CuFeS2和14.25 mol O2反应,理论上可得到 mol铜
您最近半年使用:0次



