名校
1 . 侯氏制碱法是将氨碱法制取碳酸钠和合成氨联合起来。下列说法正确的是
| A.氨和水分子间能形成氢键,使氨气易溶于水 |
B.工业合成氨是重要的人工固氮途径,该反应 |
| C.相同条件下,碳酸钠比碳酸氢钠溶解度更小 |
D. 溶液呈酸性,是因为 溶液呈酸性,是因为 电离程度大于水解程度 电离程度大于水解程度 |
您最近一年使用:0次
今日更新
|
2次组卷
|
2卷引用:浙江省9+1高中联盟2023-2024学年高二下学期4月期中考试化学试题
2 . 一定温度下,在1L恒容密闭容器中发生反应: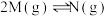 ,测得N的物质的量随时间变化的曲线如图所示。下列说法
,测得N的物质的量随时间变化的曲线如图所示。下列说法不正确 的是
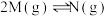 ,测得N的物质的量随时间变化的曲线如图所示。下列说法
,测得N的物质的量随时间变化的曲线如图所示。下列说法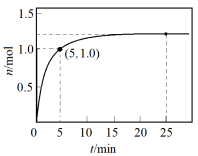
A.0 5 min内,用N表示的平均反应速率为0.2 mol/(L·min) 5 min内,用N表示的平均反应速率为0.2 mol/(L·min) |
| B.5 min时,M的正反应速率小于M的逆反应反应速率 |
| C.5 min时容器内压强大于10min容器内压强 |
| D.25 min时,该反应处于平衡状态 |
您最近一年使用:0次
3 . 下表中"方法导引”与“示例"对应关系不正确的是
| 选项 | 方法导引 | 示例 |
| A | 分类 | 实验室中制取气体装置的连接顺序一般为:发生装置 除杂装置 除杂装置 收集装置 收集装置 尾气处理装置 尾气处理装置 |
| B | 预测 | 钠、钾能与水反应,铷与钠、钾都属于IA族元素,则可预测铷也能与水反应 |
| C | 变量控制 | 探究催化剂对化学反应速率的影响时,需要控制温度、浓度和他影响因素保持不变 |
| D | 认识有机化合物的一般思路 | 先分析有机物的碳骨架和官能团,再认识它的类别、性质和用途 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 通过甲烷干重整(DRM)反应可以实现甲烷的合理转化和二氧化碳的资源化利用。某研究小组用图1方法实现甲烷干重整。
 .
.

 .
.

 .
.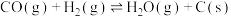

 .
.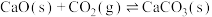

 .
.

①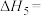
___________ 。
②反应 、
、 、
、 的
的 随
随 的变化如图2所示。反应
的变化如图2所示。反应 、
、 、
、 中属于吸热反应的有
中属于吸热反应的有___________ (填“ ”“
”“ ”或“
”或“ ”)。
”)。 ),关键是开发出具有抗积碳性能(
),关键是开发出具有抗积碳性能( )的催化剂。催化剂A、B对积碳与消碳的影响如图3所示:
)的催化剂。催化剂A、B对积碳与消碳的影响如图3所示:___________ 。
(3)图1中的反应①完成之后,以恒定流速将组成恒定的 、
、 混合气通入反应器中,单位时间流出气体各组分的物质的量随反应时间变化如图4所示。反应过程中始终未检测到
混合气通入反应器中,单位时间流出气体各组分的物质的量随反应时间变化如图4所示。反应过程中始终未检测到 ,在催化剂上有积碳。下列有关图4的说法中不正确的是___________。
,在催化剂上有积碳。下列有关图4的说法中不正确的是___________。
(4)在某温度下,若往装有足量 固体的恒压密闭反应器中充入
固体的恒压密闭反应器中充入
 、
、 混合气体且
混合气体且 ,若只发生反应
,若只发生反应 ,压强恒定为
,压强恒定为 。
。
① 的平衡转化率为50%,该反应的平衡常数
的平衡转化率为50%,该反应的平衡常数 为
为___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
② 的物质的量
的物质的量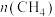 随时间变化如图5所示。在相同温度、压强及
随时间变化如图5所示。在相同温度、压强及 起始物质的量不变情况下,通过调整
起始物质的量不变情况下,通过调整 、
、 比例将
比例将 平衡转化率提高至75%,请在图5中画出
平衡转化率提高至75%,请在图5中画出 的物质的量随时间t变化的曲线。
的物质的量随时间t变化的曲线。___________

 .
.

 .
.

 .
.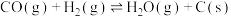

 .
.

 .
.

①
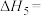
②反应
 、
、 、
、 的
的 随
随 的变化如图2所示。反应
的变化如图2所示。反应 、
、 、
、 中属于吸热反应的有
中属于吸热反应的有 ”“
”“ ”或“
”或“ ”)。
”)。
 ),关键是开发出具有抗积碳性能(
),关键是开发出具有抗积碳性能( )的催化剂。催化剂A、B对积碳与消碳的影响如图3所示:
)的催化剂。催化剂A、B对积碳与消碳的影响如图3所示:
(3)图1中的反应①完成之后,以恒定流速将组成恒定的
 、
、 混合气通入反应器中,单位时间流出气体各组分的物质的量随反应时间变化如图4所示。反应过程中始终未检测到
混合气通入反应器中,单位时间流出气体各组分的物质的量随反应时间变化如图4所示。反应过程中始终未检测到 ,在催化剂上有积碳。下列有关图4的说法中不正确的是___________。
,在催化剂上有积碳。下列有关图4的说法中不正确的是___________。
A. 之前只发生反应 之前只发生反应 |
B. ,可能有副反应 ,可能有副反应 发生,且生成 发生,且生成 的速率大于反应 的速率大于反应 |
C. 之后,CO的气体流率减小,是因为催化剂失活或发生反应 之后,CO的气体流率减小,是因为催化剂失活或发生反应 |
D. 之后,可能是因为积碳,使反应 之后,可能是因为积碳,使反应 不再发生,反应 不再发生,反应 程度变小 程度变小 |
(4)在某温度下,若往装有足量
 固体的恒压密闭反应器中充入
固体的恒压密闭反应器中充入
 、
、 混合气体且
混合气体且 ,若只发生反应
,若只发生反应 ,压强恒定为
,压强恒定为 。
。①
 的平衡转化率为50%,该反应的平衡常数
的平衡转化率为50%,该反应的平衡常数 为
为②
 的物质的量
的物质的量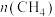 随时间变化如图5所示。在相同温度、压强及
随时间变化如图5所示。在相同温度、压强及 起始物质的量不变情况下,通过调整
起始物质的量不变情况下,通过调整 、
、 比例将
比例将 平衡转化率提高至75%,请在图5中画出
平衡转化率提高至75%,请在图5中画出 的物质的量随时间t变化的曲线。
的物质的量随时间t变化的曲线。
您最近一年使用:0次
5 .  催化加氢制
催化加氢制 ,能助力“碳达峰”,发生的主要反应有:
,能助力“碳达峰”,发生的主要反应有:
反应I:
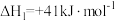
反应Ⅱ:
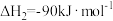
反应Ⅲ:

(1)反应Ⅱ自发进行的条件是___________ (填“高温”“低温”或“任意温度”)。
(2)在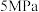 下,
下, 和
和 按物质的量之比
按物质的量之比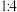 进行投料,只发生反应I和反应Ⅲ,平衡时
进行投料,只发生反应I和反应Ⅲ,平衡时 和
和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。___________ 。
②曲线q在250℃之后随温度升高而增大的原因是___________ 。
③250℃时,反应I的平衡常数
___________ [对于气相反应,用某组分B的平衡压强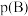 代替物质的量浓度
代替物质的量浓度 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如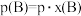 ,p为平衡总压强,
,p为平衡总压强,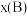 为平衡系统中B的物质的量分数]。
为平衡系统中B的物质的量分数]。
(3)可用 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: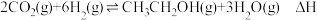 。经实验测定在容积恒定,不同投料比
。经实验测定在容积恒定,不同投料比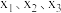 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示 。请结合图像分析,下列相关说法正确的是
。请结合图像分析,下列相关说法正确的是___________ 。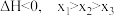
B.投料比为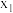 ,随反应进行,气体的压强一定减小
,随反应进行,气体的压强一定减小
C.当混合气体的平均摩尔质量不再变化时,可说明上述反应已达到平衡状态
D.随温度升高,不同投料比时 的平衡转化率趋于相近,其原因可能是升高温度到一定范围,温度对平衡移动的影响占主要因素
的平衡转化率趋于相近,其原因可能是升高温度到一定范围,温度对平衡移动的影响占主要因素
E.达到平衡后,降低温度,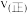 、
、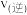 均减小,且
均减小,且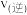 减小的幅度更大
减小的幅度更大
(4)一种以 和
和 为原料,利用
为原料,利用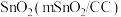 和
和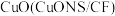 纳米片作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
纳米片作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。___________ 。
 催化加氢制
催化加氢制 ,能助力“碳达峰”,发生的主要反应有:
,能助力“碳达峰”,发生的主要反应有:反应I:

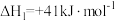
反应Ⅱ:

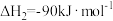
反应Ⅲ:


(1)反应Ⅱ自发进行的条件是
(2)在
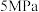 下,
下, 和
和 按物质的量之比
按物质的量之比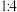 进行投料,只发生反应I和反应Ⅲ,平衡时
进行投料,只发生反应I和反应Ⅲ,平衡时 和
和 在含碳产物中的物质的量分数及
在含碳产物中的物质的量分数及 转化率随温度的变化如图所示。
转化率随温度的变化如图所示。
②曲线q在250℃之后随温度升高而增大的原因是
③250℃时,反应I的平衡常数

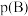 代替物质的量浓度
代替物质的量浓度 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如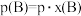 ,p为平衡总压强,
,p为平衡总压强,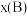 为平衡系统中B的物质的量分数]。
为平衡系统中B的物质的量分数]。(3)可用
 与
与 催化加氢制乙醇,反应原理为:
催化加氢制乙醇,反应原理为: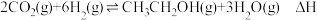 。经实验测定在容积恒定,不同投料比
。经实验测定在容积恒定,不同投料比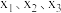 时
时 的平衡转化率与温度的关系如图所示
的平衡转化率与温度的关系如图所示 。请结合图像分析,下列相关说法正确的是
。请结合图像分析,下列相关说法正确的是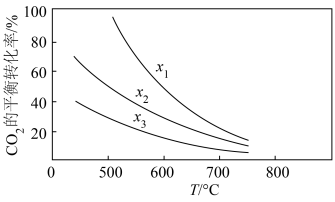
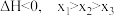
B.投料比为
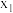 ,随反应进行,气体的压强一定减小
,随反应进行,气体的压强一定减小C.当混合气体的平均摩尔质量不再变化时,可说明上述反应已达到平衡状态
D.随温度升高,不同投料比时
 的平衡转化率趋于相近,其原因可能是升高温度到一定范围,温度对平衡移动的影响占主要因素
的平衡转化率趋于相近,其原因可能是升高温度到一定范围,温度对平衡移动的影响占主要因素E.达到平衡后,降低温度,
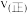 、
、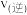 均减小,且
均减小,且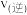 减小的幅度更大
减小的幅度更大(4)一种以
 和
和 为原料,利用
为原料,利用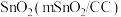 和
和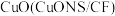 纳米片作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
纳米片作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。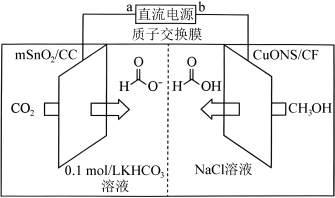
您最近一年使用:0次
名校
6 . 锶( )与钙同主族,某固态化合物Y的组成为
)与钙同主族,某固态化合物Y的组成为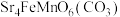 ,以Y为原料可实现如下转化:
,以Y为原料可实现如下转化: 均不能形成配合物。请回答:
均不能形成配合物。请回答:
(1)写出溶液C中的所有阳离子___________ 。
(2)步骤Ⅴ中的反应为 ,说明
,说明 能够较完全转化为
能够较完全转化为 ,的两个原因分别是:①生成
,的两个原因分别是:①生成 降低了体系的能量,促使反应正向进行②
降低了体系的能量,促使反应正向进行②___________ 。
(3)下列说法不正确 的是___________。
(4)固体Y可与 溶液反应,写出该反应的离子方程式
溶液反应,写出该反应的离子方程式___________ 。
(5)设计实验方案检验气体中除 以外的两种主要成分
以外的两种主要成分___________ 。
 )与钙同主族,某固态化合物Y的组成为
)与钙同主族,某固态化合物Y的组成为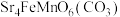 ,以Y为原料可实现如下转化:
,以Y为原料可实现如下转化:
 均不能形成配合物。请回答:
均不能形成配合物。请回答:(1)写出溶液C中的所有阳离子
(2)步骤Ⅴ中的反应为
 ,说明
,说明 能够较完全转化为
能够较完全转化为 ,的两个原因分别是:①生成
,的两个原因分别是:①生成 降低了体系的能量,促使反应正向进行②
降低了体系的能量,促使反应正向进行②(3)下列说法
A.固体B中含有 | B.步骤Ⅱ反应促进了 的水解 的水解 |
C.步骤Ⅲ可推断碱性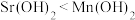 | D.直接加热 无法获得 无法获得 |
(4)固体Y可与
 溶液反应,写出该反应的离子方程式
溶液反应,写出该反应的离子方程式(5)设计实验方案检验气体中除
 以外的两种主要成分
以外的两种主要成分
您最近一年使用:0次
名校
7 . 一定条件下,2,3-二甲基-1,3-丁二烯与溴单质发生液相加成反应(1,2-加成和1,4-加成同时存在),已知体系中两种产物可通过中间产物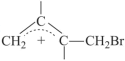 互相转化,反应历程及能量变化如图所示:
互相转化,反应历程及能量变化如图所示:

A.从图示可以看出: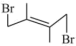 比 比 稳定 稳定 |
B.由 小于 小于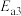 可知,低温更有利于 可知,低温更有利于 的转化 的转化 |
C.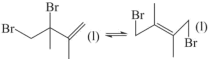 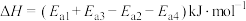 |
| D.由反应历程及能量变化图可知,该加成反应为放热反应 |
您最近一年使用:0次
名校
解题方法
8 . 煤燃烧过程中会产生大气污染物CO、NO,研究氮氧化物的消除和CO2资源再利用是目前研究的热点之一。
(1)用惰性电极(Pt)电解CO2吸收液(假设溶液成分为饱和NaHCO3溶液),阴极区通入CO2可以制得HCOONa,请写出阴极的电解电极方程式_______ 。
(2)已知: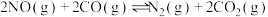 ,CO、NO在铁催化剂表面进行如下两步反应:
,CO、NO在铁催化剂表面进行如下两步反应:
反应I:_______
反应II: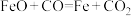
①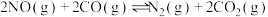 反应自发进行的条件为:
反应自发进行的条件为:_______ 。
②完成反应I的化学方程式:_______ 。
(3)某课题组为研究CO存在下铁对NO的催化还原反应,设计了三组对照实验。分别如下:第1、2组将等量的Fe置于石英管内,通入N2吹扫约10min,然后分别通入一定量NO或NO和CO混合气体后,两端密封开始加热升温,测NO的转化率;第3组与第2组其它条件相同,但没有Fe参与实验,测NO的转化率,得出结果如图。_______ 。
A.其他条件不变时,用空气替代N2,对实验结果有影响
B.当体系中CO和CO2的物质的量浓度相等时,反应达到平衡状态
C.增加铁的质量和表面积,能降低该反应的活化能,提高反应速率,提高NO的平衡转化率
D.当温度小于750K,铁在NO、CO反应系统中,以Fe、NO的气固异相反应为主
②请解释图1中750K后曲线1、2变化趋势不同的原因:_______ 。
③若该反应的正、逆反应速率可表示为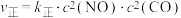 、
、 ,
, 、
、 分别为正、逆反应速率常数,仅与温度有关。一定温度下,在体积为1L的容器中加入2molNO和2.2molCO发生上述反应,测得CO和CO2物质的量浓度随时间的变化如图所示。已知该温度下K=27/20,则a点时
分别为正、逆反应速率常数,仅与温度有关。一定温度下,在体积为1L的容器中加入2molNO和2.2molCO发生上述反应,测得CO和CO2物质的量浓度随时间的变化如图所示。已知该温度下K=27/20,则a点时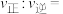
_______ 。(结果保留两位有效数字)
(1)用惰性电极(Pt)电解CO2吸收液(假设溶液成分为饱和NaHCO3溶液),阴极区通入CO2可以制得HCOONa,请写出阴极的电解电极方程式
(2)已知:
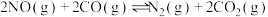 ,CO、NO在铁催化剂表面进行如下两步反应:
,CO、NO在铁催化剂表面进行如下两步反应:反应I:
反应II:
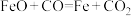
①
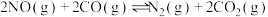 反应自发进行的条件为:
反应自发进行的条件为:②完成反应I的化学方程式:
(3)某课题组为研究CO存在下铁对NO的催化还原反应,设计了三组对照实验。分别如下:第1、2组将等量的Fe置于石英管内,通入N2吹扫约10min,然后分别通入一定量NO或NO和CO混合气体后,两端密封开始加热升温,测NO的转化率;第3组与第2组其它条件相同,但没有Fe参与实验,测NO的转化率,得出结果如图。

A.其他条件不变时,用空气替代N2,对实验结果有影响
B.当体系中CO和CO2的物质的量浓度相等时,反应达到平衡状态
C.增加铁的质量和表面积,能降低该反应的活化能,提高反应速率,提高NO的平衡转化率
D.当温度小于750K,铁在NO、CO反应系统中,以Fe、NO的气固异相反应为主
②请解释图1中750K后曲线1、2变化趋势不同的原因:
③若该反应的正、逆反应速率可表示为
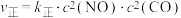 、
、 ,
, 、
、 分别为正、逆反应速率常数,仅与温度有关。一定温度下,在体积为1L的容器中加入2molNO和2.2molCO发生上述反应,测得CO和CO2物质的量浓度随时间的变化如图所示。已知该温度下K=27/20,则a点时
分别为正、逆反应速率常数,仅与温度有关。一定温度下,在体积为1L的容器中加入2molNO和2.2molCO发生上述反应,测得CO和CO2物质的量浓度随时间的变化如图所示。已知该温度下K=27/20,则a点时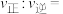
您最近一年使用:0次
名校
解题方法
9 . 一定条件下,CH4与 反应生成CH3OH。已知直接参与化学键变化的原子被替换为更重的同位素时,反应速率会变慢。
反应生成CH3OH。已知直接参与化学键变化的原子被替换为更重的同位素时,反应速率会变慢。 分别与CH4、CD4反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以CH4示例)。下列说法
分别与CH4、CD4反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以CH4示例)。下列说法不正确 的是
 反应生成CH3OH。已知直接参与化学键变化的原子被替换为更重的同位素时,反应速率会变慢。
反应生成CH3OH。已知直接参与化学键变化的原子被替换为更重的同位素时,反应速率会变慢。 分别与CH4、CD4反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以CH4示例)。下列说法
分别与CH4、CD4反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以CH4示例)。下列说法
| A.反应历程中涉及氢原子成键变化的是步骤I |
B. 与CD4反应的过渡态1能量变化应为图中曲线c 与CD4反应的过渡态1能量变化应为图中曲线c |
C.若 与CHD3反应,生成的氘代甲醇有3种 与CHD3反应,生成的氘代甲醇有3种 |
D. 与CH2D2反应,产物的产量 与CH2D2反应,产物的产量 |
您最近一年使用:0次
解题方法
10 . 硫化碱法是工业上制备 的方法之一,反应原理为
的方法之一,反应原理为 下列有关说法不正确的是
下列有关说法不正确的是
 的方法之一,反应原理为
的方法之一,反应原理为 下列有关说法不正确的是
下列有关说法不正确的是A. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
| B.适当升高温度可以加快此反应的反应速率 |
C. 是还原剂, 是还原剂, 是氧化剂 是氧化剂 |
D.生成 转移电子的数目为8 转移电子的数目为8 |
您最近一年使用:0次



