名校
1 . 恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。[已知:2SO2(g)+O2(g) 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
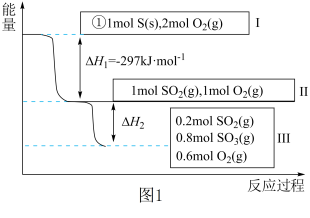
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:___________ 。
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|___________ (填“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是___________ ;图中表示平衡混合物中SO3的含量最高的一段时间是___________ 。

 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
| A.升高温度 | B.充入He | C.再充入1mol SO2(g)和1mol O2(g) | D.使用催化剂 |
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是

您最近一年使用:0次
名校
解题方法
2 . 在此之前,我国科学家已成功利用二氧化碳完成了淀粉的人工全合成工作,合成淀粉的重要反应包括二氧化碳制备甲醇的反应:
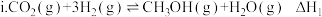 (主反应)
(主反应)
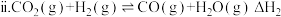 (副反应)
(副反应)
298K、 时氢气的燃烧热为
时氢气的燃烧热为 ;甲醇的燃烧热为
;甲醇的燃烧热为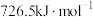 ;
;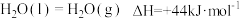
(1)由此可求得反应i的焓变
_______  。
。
(2)反应i在_______ (选填字母: A.“高温”;B.“低温”;C.“任意温度”)下可以自发进行。
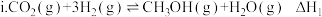 (主反应)
(主反应)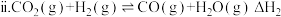 (副反应)
(副反应)298K、
 时氢气的燃烧热为
时氢气的燃烧热为 ;甲醇的燃烧热为
;甲醇的燃烧热为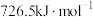 ;
;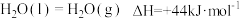
(1)由此可求得反应i的焓变

 。
。(2)反应i在
您最近一年使用:0次
名校
3 . 写出下列反应的热化学方程式。
(1)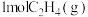 与适量
与适量 反应,生成
反应,生成 和
和 ,放出
,放出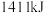 的热量
的热量___________ 。
(2) 完全燃烧生成氮气和气态水时,放出
完全燃烧生成氮气和气态水时,放出 热量
热量___________ 。
(3)1g碳与适量水蒸气反应生成CO和 ,吸收
,吸收 热量
热量___________ 。
(4)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,请写出表示硫的燃烧热的热化学方程式:___________ 。
(5)如图是298 K、101 kPa时,CO2和NH3合成尿素[CO(NH2)2]的能量变化图,写出该反应的热化学方程式:___________ 。

(1)
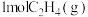 与适量
与适量 反应,生成
反应,生成 和
和 ,放出
,放出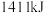 的热量
的热量(2)
 完全燃烧生成氮气和气态水时,放出
完全燃烧生成氮气和气态水时,放出 热量
热量(3)1g碳与适量水蒸气反应生成CO和
 ,吸收
,吸收 热量
热量(4)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,请写出表示硫的燃烧热的热化学方程式:
(5)如图是298 K、101 kPa时,CO2和NH3合成尿素[CO(NH2)2]的能量变化图,写出该反应的热化学方程式:

您最近一年使用:0次
4 . 按要求填空:
(1) 是一种无色气体,在空气中能发生爆炸性自燃生成固态
是一种无色气体,在空气中能发生爆炸性自燃生成固态 和液态
和液态 。已知室温下
。已知室温下 自燃放出热量
自燃放出热量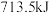 ,写出室温下
,写出室温下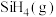 自燃的热化学方程式
自燃的热化学方程式_______ 。
(2)在 时,
时, 在
在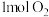 中完全燃烧生成
中完全燃烧生成 液态水,放出
液态水,放出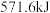 的热量,表示
的热量,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。
(3)在25℃、 下,一定质量的无水乙醇完全燃烧时放出热量
下,一定质量的无水乙醇完全燃烧时放出热量 ,燃烧生成的
,燃烧生成的 用过量澄清石灰水吸收可得
用过量澄清石灰水吸收可得 沉淀,则在此条件下,
沉淀,则在此条件下, 乙醇完全燃烧的
乙醇完全燃烧的
_______  。
。
(4) 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知25℃、
在空气中加热反应可制得铁系氧化物材料。已知25℃、 时:
时:
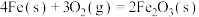
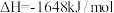

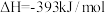
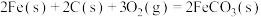
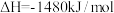
则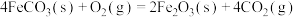

_______ 。
(1)
 是一种无色气体,在空气中能发生爆炸性自燃生成固态
是一种无色气体,在空气中能发生爆炸性自燃生成固态 和液态
和液态 。已知室温下
。已知室温下 自燃放出热量
自燃放出热量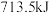 ,写出室温下
,写出室温下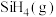 自燃的热化学方程式
自燃的热化学方程式(2)在
 时,
时, 在
在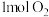 中完全燃烧生成
中完全燃烧生成 液态水,放出
液态水,放出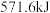 的热量,表示
的热量,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(3)在25℃、
 下,一定质量的无水乙醇完全燃烧时放出热量
下,一定质量的无水乙醇完全燃烧时放出热量 ,燃烧生成的
,燃烧生成的 用过量澄清石灰水吸收可得
用过量澄清石灰水吸收可得 沉淀,则在此条件下,
沉淀,则在此条件下, 乙醇完全燃烧的
乙醇完全燃烧的
 。
。(4)
 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知25℃、
在空气中加热反应可制得铁系氧化物材料。已知25℃、 时:
时: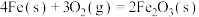
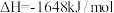

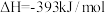
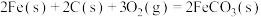
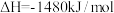
则
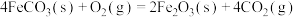

您最近一年使用:0次
名校
5 . 写出下列反应的热化学方程式
(1)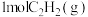 在
在 中完全燃烧生成
中完全燃烧生成 和液态水,放出
和液态水,放出 的热量
的热量___________ .
(2) 在
在 中完全燃烧生成
中完全燃烧生成 和液态水,放出
和液态水,放出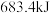 的热量
的热量___________ .
(3)在 时,足量
时,足量 在
在 中完全燃烧生成
中完全燃烧生成 液态水,放出
液态水,放出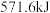 的热量,
的热量, 的燃烧热
的燃烧热
___________ ,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ .
(1)
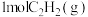 在
在 中完全燃烧生成
中完全燃烧生成 和液态水,放出
和液态水,放出 的热量
的热量(2)
 在
在 中完全燃烧生成
中完全燃烧生成 和液态水,放出
和液态水,放出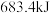 的热量
的热量(3)在
 时,足量
时,足量 在
在 中完全燃烧生成
中完全燃烧生成 液态水,放出
液态水,放出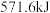 的热量,
的热量, 的燃烧热
的燃烧热
 燃烧热的热化学方程式为
燃烧热的热化学方程式为
您最近一年使用:0次
解题方法
6 . 已知下列反应的反应热数值正确,回答下列问题:
①
②
③
④
⑤
(1)上述热化学方程式中,不正确的有___________ 。(填序号,下同)
(2)上述反应中,表示燃烧热的热化学方程式是_________________________________ ;
上述反应中,表示中和热的热化学方程式是______________________ 。
已知热化学方程式: ;
;

(3)则金刚石转化为石墨的热化学方程式为___________ ,由热化学方程式可知更稳定的碳的同素异形体是___________ 。
(4)已知 ,用
,用 配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式
配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式_______________________ 。
(5)已知:

 、
、 和
和 键的键能分别为
键的键能分别为 、
、 和
和 ,则a的值为
,则a的值为________ 。
①

②

③

④

⑤

(1)上述热化学方程式中,不正确的有
(2)上述反应中,表示燃烧热的热化学方程式是
上述反应中,表示中和热的热化学方程式是
已知热化学方程式:
 ;
;
(3)则金刚石转化为石墨的热化学方程式为
(4)已知
 ,用
,用 配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式
配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式(5)已知:


 、
、 和
和 键的键能分别为
键的键能分别为 、
、 和
和 ,则a的值为
,则a的值为
您最近一年使用:0次
7 . 2023年7月28日,第31届世界大学生运动会在四川省成都市盛大开幕。已知:
回答下列问题:
(1)火炬“蓉火"采用了生物质丙烷为燃料。
①写出表示丙烷气体燃烧热的热化学方程式:_______ 。
②生物质丙烷由秸秆、稻壳、玉米芯等废弃物合成而来,与传统来自天然气加工和石油提炼的丙烷相比,其优点是_______ 。
(2)火炬“蓉火”通过优化燃料喷注和空气掺混等方式,减少了燃料的使用量,其原因是_______ 。
(3)我国科学家将甲烷无氧偶联制备乙烷和氢气,根据以上数据,计算该反应2CH4(g)=C2H6(g)+H2(g)的△H=_______ 。
| 物质 | 甲烷CH4 | 乙烷C2H6 | 丙烷C3H8 | H2 |
| 燃烧热△H/(kJ/mol) | -890.3 | -1559.8 | -2219.9 | -285.8 |
(1)火炬“蓉火"采用了生物质丙烷为燃料。
①写出表示丙烷气体燃烧热的热化学方程式:
②生物质丙烷由秸秆、稻壳、玉米芯等废弃物合成而来,与传统来自天然气加工和石油提炼的丙烷相比,其优点是
(2)火炬“蓉火”通过优化燃料喷注和空气掺混等方式,减少了燃料的使用量,其原因是
(3)我国科学家将甲烷无氧偶联制备乙烷和氢气,根据以上数据,计算该反应2CH4(g)=C2H6(g)+H2(g)的△H=
您最近一年使用:0次
名校
8 . 生产生活中的化学反应都伴随能量的变化,请用学到的有关知识回答下列问题:
(1)制作有降温、保鲜和镇痛的冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热盒饭”可利用下面___________ (填字母序号)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水 C.钠和水
(3)CH3OH是优质液体燃料,在25℃、101 kPa下,充分燃烧1 g CH3OH并恢复到原状态,会释放22.7 kJ的热量。请写出表示CH3OH燃烧热的热化学反应方程式:___________ 。
(1)制作有降温、保鲜和镇痛的冷敷袋可以利用
(2)“即热盒饭”可利用下面
A.生石灰和水 B.浓硫酸和水 C.钠和水
(3)CH3OH是优质液体燃料,在25℃、101 kPa下,充分燃烧1 g CH3OH并恢复到原状态,会释放22.7 kJ的热量。请写出表示CH3OH燃烧热的热化学反应方程式:
您最近一年使用:0次
9 . 完成下列问题。
(1)下列说法正确的是_______ 。
①浓H2SO4稀释是放热反应
②放热反应不需要加热就能反应,吸热反应不加热就不能反应
③吸热反应中,反应物化学键断裂吸收的总能量高于生成物形成化学键放出的总能量
④C(石墨,s)= C(金刚石,s) ΔH>0,说明石墨比金刚石稳定
⑤热化学方程式前面的化学计量数既表示分子数也表示物质的量
(2)写出下列反应的热化学方程式。
①16CH4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出890.3kJ热量:___________ 。
②若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量:___________ 。
(3)已知:①N2(g)+2O2(g)=2NO2(g) △H1=+66.4 kJ/mol
②N2H4(1)+O2(g)=N2(g)+2H2O(g) △H2=−534kJ/mol
请写出N2H4(1)与NO2反应生成N2和水蒸气的的热化学方程式___________ 。
(1)下列说法正确的是
①浓H2SO4稀释是放热反应
②放热反应不需要加热就能反应,吸热反应不加热就不能反应
③吸热反应中,反应物化学键断裂吸收的总能量高于生成物形成化学键放出的总能量
④C(石墨,s)= C(金刚石,s) ΔH>0,说明石墨比金刚石稳定
⑤热化学方程式前面的化学计量数既表示分子数也表示物质的量
(2)写出下列反应的热化学方程式。
①16CH4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出890.3kJ热量:
②若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量:
(3)已知:①N2(g)+2O2(g)=2NO2(g) △H1=+66.4 kJ/mol
②N2H4(1)+O2(g)=N2(g)+2H2O(g) △H2=−534kJ/mol
请写出N2H4(1)与NO2反应生成N2和水蒸气的的热化学方程式
您最近一年使用:0次
名校
10 . I.写出对应的反应热和热化学方程式
(1)足量H2在1molO2中完全燃烧生成2mol液态水,放出571.6k的热量,则H2的燃烧热ΔH=___________ 。
(2)已知:8g的CH4与足量的O2反应,生成CO2和液态水,放出445.15kJ的热量写出表示甲烷燃烧的热化学方程式:___________ 。
II.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为
(3)下列各组试剂混合发生反应的离子方程式为 的是
的是___________ (填序号)。
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(4)若稀硫酸与氢氧化钠固体反应生成1molH2O(l),则反应放出的热量___________ (填“>”“<”或“=”)57.3kJ,原因是___________ 。
III.如图所示,某反应在不同条件下的反应历程分别为a、b。

(5)据图可判断出反应物的总键能___________ (填“>”“<”或“=”)生成物的总键能,则该反应的反应热ΔH___________ 0。
(1)足量H2在1molO2中完全燃烧生成2mol液态水,放出571.6k的热量,则H2的燃烧热ΔH=
(2)已知:8g的CH4与足量的O2反应,生成CO2和液态水,放出445.15kJ的热量写出表示甲烷燃烧的热化学方程式:
II.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为

(3)下列各组试剂混合发生反应的离子方程式为
 的是
的是A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(4)若稀硫酸与氢氧化钠固体反应生成1molH2O(l),则反应放出的热量
III.如图所示,某反应在不同条件下的反应历程分别为a、b。

(5)据图可判断出反应物的总键能
您最近一年使用:0次
2023-11-16更新
|
131次组卷
|
2卷引用:山西省临汾市2023-2024学年高二上学期11月期中考试化学试题



