名校
1 . 氨的催化氧化反应是硝酸工业中的重要反应,某条件下 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:
Ⅰ.
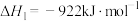
Ⅱ.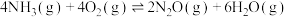
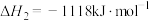
Ⅲ.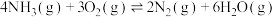

已知:298K时,相关物质的焓的数据如图。
___________  。
。
(2)将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。
②随着温度的升高, 的选择性下降的原因可能为
的选择性下降的原因可能为___________ 。
(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
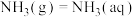

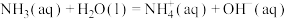

其中p为 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度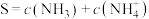 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为___________ 。
(4)由 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。
已知: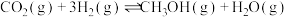 的
的 -49.5kJ/mol
-49.5kJ/mol
反应②:

反应③: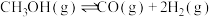
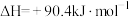
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。___________  。
。
Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入
 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在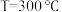 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在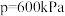 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。
ii. 点
点 的分压为
的分压为___________  ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
___________  (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
iii.图中 点的
点的 高于
高于 点的原因是
点的原因是___________ 。
 与
与 作用时可发生如下3个反应:
作用时可发生如下3个反应:Ⅰ.

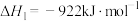
Ⅱ.
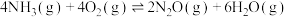
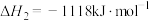
Ⅲ.
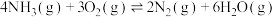

已知:298K时,相关物质的焓的数据如图。


 。
。(2)将一定比例的
 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性与温度的关系如图所示。
的选择性与温度的关系如图所示。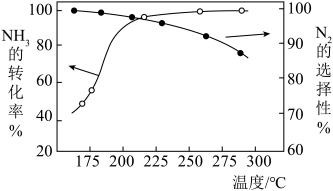
 适宜的温度为 210℃左右。
适宜的温度为 210℃左右。②随着温度的升高,
 的选择性下降的原因可能为
的选择性下降的原因可能为(3)在一定温度下,氨气溶于水的过程及其平衡常数为:
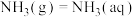

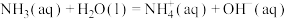

其中p为
 的平衡压强,
的平衡压强, 为
为 在水溶液中的平衡浓度。设氨气在水中的溶解度
在水溶液中的平衡浓度。设氨气在水中的溶解度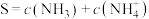 ,则用p、
,则用p、 和
和 表示S的代数式为
表示S的代数式为(4)由
 与
与 制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由
制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由 人工合成淀粉(节选途径见图)中的重要反应之一。
人工合成淀粉(节选途径见图)中的重要反应之一。已知:
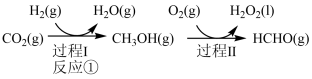
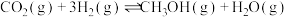 的
的 -49.5kJ/mol
-49.5kJ/mol反应②:


反应③:
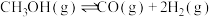
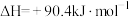
Ⅰ.反应①在有、无催化剂条件下的反应历程如下图所示,其中吸附在催化剂表面上的物种用*标注,TS为过渡态。
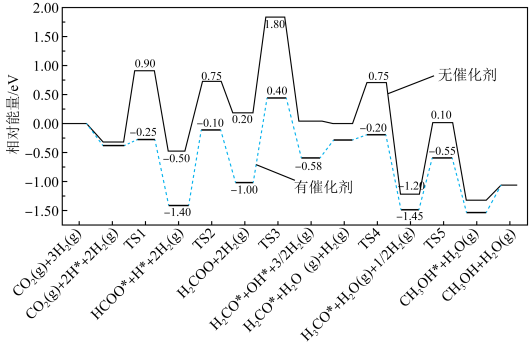
 。
。Ⅱ.某研究小组采用上述催化剂,向密闭容器中通入

 和
和
 ,只发生反应①和反应②,在不同条件下达到平衡,在
,只发生反应①和反应②,在不同条件下达到平衡,在 下甲醇的物质的量分数
下甲醇的物质的量分数 随压强
随压强 的变化、在
的变化、在 下
下 随温度
随温度 的变化,如下图所示。
的变化,如下图所示。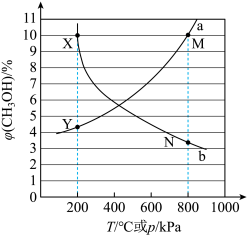
 点对应的温度和压强分别为200℃、600
点对应的温度和压强分别为200℃、600 。
。ii.
 点
点 的分压为
的分压为 ,此时容器中
,此时容器中 为
为 ,
, 为
为 ,反应①的压强平衡常数
,反应①的压强平衡常数
 (压强平衡常数
(压强平衡常数 是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。
是以分压代替浓度表示的平衡常数,分压=总压×物质的量分数)。iii.图中
 点的
点的 高于
高于 点的原因是
点的原因是
您最近一年使用:0次
名校
解题方法
2 .  是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:
是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:
(1)已知:①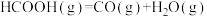
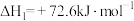
②
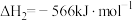
③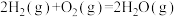
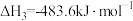
则 的
的
_______  。
。
(2)恒温恒容条件下,向密闭容器中充入1
 和2
和2
 合成
合成 ,下列叙述正确的是_______(填字母)。
,下列叙述正确的是_______(填字母)。
(3)一定温度下,保持总压强为2.0 ,向密闭容器中充入1
,向密闭容器中充入1
 和1.6
和1.6
 ,发生反应:
,发生反应: 、
、 。反应达到平衡时
。反应达到平衡时 的转化率为50%,
的转化率为50%, 的选择性为80%(已知:甲酸的选择性
的选择性为80%(已知:甲酸的选择性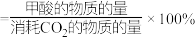 。该温度下,
。该温度下, 的平衡常数
的平衡常数
_______  。
。
(4)常温下,向 溶液中滴加
溶液中滴加 溶液。溶液的
溶液。溶液的 与
与 的关系如图所示。
的关系如图所示。
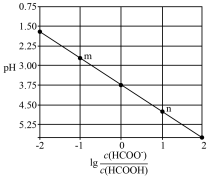
则
_______ ,n点溶液中离子浓度由大到小的排序为_______ 。
(5)常温下,已知 一元酸HCOOH(甲酸)溶液中
一元酸HCOOH(甲酸)溶液中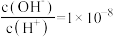 。
。
①
 的
的
_______ 。
②取10mL0.1mol/L的HCOOH溶液稀释100倍,有关说法正确的是_______ (填序号)
A.所有离子的浓度在稀释过程中都会减少
B.稀释后溶液的
C.稀释后甲酸的电离度会增大
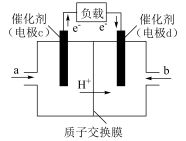
(6)C2H5OH可作为燃料使用,用C2H5OH和O2组合形成的质子交换膜燃料电池如图。则d电极是_______ (填“正极”或“负极”),c电极的电极反应式为_______ 。
 是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:
是最简单的有机羧酸,常作抗菌剂和化工原料。回答下列问题:(1)已知:①
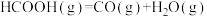
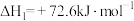
②

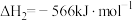
③
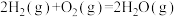
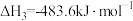
则
 的
的
 。
。(2)恒温恒容条件下,向密闭容器中充入1

 和2
和2
 合成
合成 ,下列叙述正确的是_______(填字母)。
,下列叙述正确的是_______(填字母)。| A.气体压强不随时间变化时达到平衡状态 |
B.平衡时 的最大体积分数为50% 的最大体积分数为50% |
C.平衡后及时移走 ,平衡常数增大 ,平衡常数增大 |
D.平衡后再充入 , , 的平衡转化率增大 的平衡转化率增大 |
(3)一定温度下,保持总压强为2.0
 ,向密闭容器中充入1
,向密闭容器中充入1
 和1.6
和1.6
 ,发生反应:
,发生反应: 、
、 。反应达到平衡时
。反应达到平衡时 的转化率为50%,
的转化率为50%, 的选择性为80%(已知:甲酸的选择性
的选择性为80%(已知:甲酸的选择性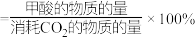 。该温度下,
。该温度下, 的平衡常数
的平衡常数
 。
。(4)常温下,向
 溶液中滴加
溶液中滴加 溶液。溶液的
溶液。溶液的 与
与 的关系如图所示。
的关系如图所示。
则

(5)常温下,已知
 一元酸HCOOH(甲酸)溶液中
一元酸HCOOH(甲酸)溶液中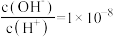 。
。①

 的
的
②取10mL0.1mol/L的HCOOH溶液稀释100倍,有关说法正确的是
A.所有离子的浓度在稀释过程中都会减少
B.稀释后溶液的

C.稀释后甲酸的电离度会增大
(6)C2H5OH可作为燃料使用,用C2H5OH和O2组合形成的质子交换膜燃料电池如图。则d电极是

您最近一年使用:0次
解题方法
3 . 聚丙烯是生产N95口罩和医用无纺布口罩防护服材料,而丙烯是制造聚丙烯的单体。工业上,生成丙烯的方法有多种。
Ⅰ.以异丙醇为原料制备丙烯。已知:
①
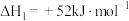 ;
;
②
 ;
;
③
 。
。
(1) 为
为___________  。
。
(2)反应③在___________ (填“较高”“较低”或“任意”)温度下能自发进行。
Ⅱ.近日,中国石油大学(华东)代鹏程副教授课题组开发富含硼氧活性位点的热稳定层柱状框架类材料助力丙烷氧化脱氢。有关反应如下:
反应1: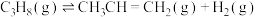

反应2: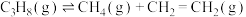
 。
。
(3)向密闭反应器中充入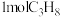 ,发生上述反应1,测得平衡时的丙烯的体积分数与温度、压强的关系如图1所示。
,发生上述反应1,测得平衡时的丙烯的体积分数与温度、压强的关系如图1所示。
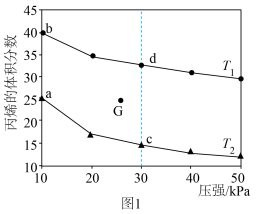
①其他条件相同,增大压强,丙烯体积分数减小的原因是___________ 。
②已知G点为某条件下的平衡状态,若将G点对应反应容器降温同时缩小容器体积使体系压强增大,重新达到平衡状态可能是图中a、b、c、d中的___________ 点。
③下列物理量中,图中c点大于d点的是___________ (填字母)。
A.正反应速率 B.对应温度的平衡常数 C.逆反应速率 D.平均摩尔质量
(4)一定温度下,若向密闭反应器中充入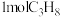 ,发生上述两个反应,达到平衡时,丙烯的体积分数为
,发生上述两个反应,达到平衡时,丙烯的体积分数为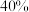 ,丙烯、乙烯体积之比为
,丙烯、乙烯体积之比为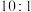 ,丙烷的平衡转化率为
,丙烷的平衡转化率为___________ (用百分数表示,结果保留3位有效数字)。
(5)一定温度下,总压保持为 时,向反应器中充入
时,向反应器中充入 和
和 ,发生上述两个反应。测得丙烷平衡转化率与投料比
,发生上述两个反应。测得丙烷平衡转化率与投料比 的关系如图2所示。
的关系如图2所示。
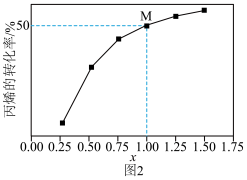
①向反应器充入 的目的是
的目的是___________ 。
②该温度下, 点丙烯的选择性为
点丙烯的选择性为 ,此时反应1的平衡常数
,此时反应1的平衡常数 为
为___________ 。
提示:(i)用分压计算的平衡常数为 ,分压
,分压 总压
总压 物质的量分数;(ii)丙烯的选择性
物质的量分数;(ii)丙烯的选择性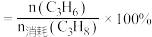 。
。
Ⅰ.以异丙醇为原料制备丙烯。已知:
①

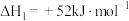 ;
;②

 ;
;③

 。
。(1)
 为
为 。
。(2)反应③在
Ⅱ.近日,中国石油大学(华东)代鹏程副教授课题组开发富含硼氧活性位点的热稳定层柱状框架类材料助力丙烷氧化脱氢。有关反应如下:
反应1:
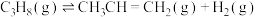

反应2:
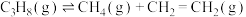
 。
。(3)向密闭反应器中充入
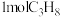 ,发生上述反应1,测得平衡时的丙烯的体积分数与温度、压强的关系如图1所示。
,发生上述反应1,测得平衡时的丙烯的体积分数与温度、压强的关系如图1所示。
①其他条件相同,增大压强,丙烯体积分数减小的原因是
②已知G点为某条件下的平衡状态,若将G点对应反应容器降温同时缩小容器体积使体系压强增大,重新达到平衡状态可能是图中a、b、c、d中的
③下列物理量中,图中c点大于d点的是
A.正反应速率 B.对应温度的平衡常数 C.逆反应速率 D.平均摩尔质量
(4)一定温度下,若向密闭反应器中充入
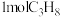 ,发生上述两个反应,达到平衡时,丙烯的体积分数为
,发生上述两个反应,达到平衡时,丙烯的体积分数为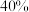 ,丙烯、乙烯体积之比为
,丙烯、乙烯体积之比为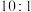 ,丙烷的平衡转化率为
,丙烷的平衡转化率为(5)一定温度下,总压保持为
 时,向反应器中充入
时,向反应器中充入 和
和 ,发生上述两个反应。测得丙烷平衡转化率与投料比
,发生上述两个反应。测得丙烷平衡转化率与投料比 的关系如图2所示。
的关系如图2所示。
①向反应器充入
 的目的是
的目的是②该温度下,
 点丙烯的选择性为
点丙烯的选择性为 ,此时反应1的平衡常数
,此时反应1的平衡常数 为
为提示:(i)用分压计算的平衡常数为
 ,分压
,分压 总压
总压 物质的量分数;(ii)丙烯的选择性
物质的量分数;(ii)丙烯的选择性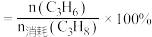 。
。
您最近一年使用:0次
4 . 研发二氧化碳的碳捕集和碳利用技术是科学研究热点问题。
(1)常温常压下,一些常见物质的燃烧热如表所示:
已知:
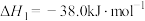
则

___________  ,该反应在
,该反应在___________ (填“高温”“低温”或“任意温度”)下能自发进行。
(2) 催化加氢制取甲醇,反应如下:
催化加氢制取甲醇,反应如下:
主反应:

副反应:
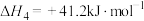
在一定条件下,向某1L恒容密闭容器中充入1mol 和a mol
和a mol 发生反应,起始总压强为21.2MPa.实验测得
发生反应,起始总压强为21.2MPa.实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度变化如图甲所示:
的选择性随温度变化如图甲所示:

已知: 的选择性
的选择性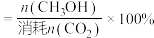 。图甲中表示平衡时
。图甲中表示平衡时 的选择性的曲线为
的选择性的曲线为___________ (填“X”或“Y”),温度高于280℃时,曲线Y随温度升高而升高的原因是___________ 。240℃时,反应20min容器内达到平衡状态,副反应的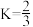 ,则初始充入
,则初始充入 的物质的量
的物质的量
___________ mol,平衡时容器内的总压强为___________ MPa。
(1)常温常压下,一些常见物质的燃烧热如表所示:
| 名称 | 氢气 | 甲烷 | 一氧化碳 | 甲醇 |
 /( /( ) ) | -285.8 | -890.3 | -283.0 | -726.5 |

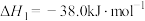
则


 ,该反应在
,该反应在(2)
 催化加氢制取甲醇,反应如下:
催化加氢制取甲醇,反应如下:主反应:


副反应:

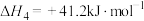
在一定条件下,向某1L恒容密闭容器中充入1mol
 和a mol
和a mol 发生反应,起始总压强为21.2MPa.实验测得
发生反应,起始总压强为21.2MPa.实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度变化如图甲所示:
的选择性随温度变化如图甲所示:
已知:
 的选择性
的选择性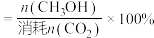 。图甲中表示平衡时
。图甲中表示平衡时 的选择性的曲线为
的选择性的曲线为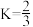 ,则初始充入
,则初始充入 的物质的量
的物质的量
您最近一年使用:0次
5 . 天然气开采过程中产生大量的含硫废水(硫元素的主要存在形式为  需要回收处理并加以利用,有关反应如下:
需要回收处理并加以利用,有关反应如下:
i.2H2S(g)+3O2(g) 2SO2(g)+2H2O(g)
2SO2(g)+2H2O(g) 
ii.4H2S(g)+2SO2(g) 3S2(g)+4H2O(g)
3S2(g)+4H2O(g) 
iii.2H2(g)+O2(g) 2H2O(g)
2H2O(g) 
回答下列问题:
(1)H2S热分解反应2H2S(g) S2(g)+2H2(g)的
S2(g)+2H2(g)的 =
=___________ (用含 、
、 、
、 的式子表示),若起始加1molH2S气体在刚性容器中发生该分解反应,下列说法能说明该反应已达平衡的是
的式子表示),若起始加1molH2S气体在刚性容器中发生该分解反应,下列说法能说明该反应已达平衡的是___________ (填序号)。
A.H₂与S₂的物质的量之比保持2:1不变
B.容器中混合气体平均摩尔质量保持不变
C.反应速率 保持不变
保持不变
D.单位时间内每断开4molH-S键,就生成2molH-H键
(2)总压恒定为 100kPa,向密闭容器中充入 发生反应i和反应ii,反应过程中
发生反应i和反应ii,反应过程中 等含硫物质的分布分数δ随时间变化如图所示。
等含硫物质的分布分数δ随时间变化如图所示。

①表示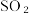 分布分数的曲线为
分布分数的曲线为___________ (填“甲”“乙”或“丙”)。
②t1时测得 转化率为α,此时体系中
转化率为α,此时体系中 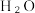 的物质的量为
的物质的量为___________ mol (用含α的式子表示)。
(3)也可采用Na2SO3氧化法对H2S进行处理,过程中发生反应的方程式(均未配平)为:
i.
ii.
iii.S(s)+ (aq)→
(aq)→ (aq)
(aq)
实验测得在 时,Na2SO3的投加量对平衡体系中部分微粒浓度的影响如图所示。
时,Na2SO3的投加量对平衡体系中部分微粒浓度的影响如图所示。

①T℃时,反应iii的平衡常数 K=___________ 。
②结合三个反应分析,当 Na2SO3投加量高于 5g/L时,单位体积内S的质量减小的原因为:___________ 。
 需要回收处理并加以利用,有关反应如下:
需要回收处理并加以利用,有关反应如下:i.2H2S(g)+3O2(g)
 2SO2(g)+2H2O(g)
2SO2(g)+2H2O(g) 
ii.4H2S(g)+2SO2(g)
 3S2(g)+4H2O(g)
3S2(g)+4H2O(g) 
iii.2H2(g)+O2(g)
 2H2O(g)
2H2O(g) 
回答下列问题:
(1)H2S热分解反应2H2S(g)
 S2(g)+2H2(g)的
S2(g)+2H2(g)的 =
= 、
、 、
、 的式子表示),若起始加1molH2S气体在刚性容器中发生该分解反应,下列说法能说明该反应已达平衡的是
的式子表示),若起始加1molH2S气体在刚性容器中发生该分解反应,下列说法能说明该反应已达平衡的是A.H₂与S₂的物质的量之比保持2:1不变
B.容器中混合气体平均摩尔质量保持不变
C.反应速率
 保持不变
保持不变 D.单位时间内每断开4molH-S键,就生成2molH-H键
(2)总压恒定为 100kPa,向密闭容器中充入
 发生反应i和反应ii,反应过程中
发生反应i和反应ii,反应过程中 等含硫物质的分布分数δ随时间变化如图所示。
等含硫物质的分布分数δ随时间变化如图所示。
①表示
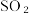 分布分数的曲线为
分布分数的曲线为②t1时测得
 转化率为α,此时体系中
转化率为α,此时体系中 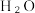 的物质的量为
的物质的量为(3)也可采用Na2SO3氧化法对H2S进行处理,过程中发生反应的方程式(均未配平)为:
i.

ii.

iii.S(s)+
 (aq)→
(aq)→ (aq)
(aq)实验测得在
 时,Na2SO3的投加量对平衡体系中部分微粒浓度的影响如图所示。
时,Na2SO3的投加量对平衡体系中部分微粒浓度的影响如图所示。
①T℃时,反应iii的平衡常数 K=
②结合三个反应分析,当 Na2SO3投加量高于 5g/L时,单位体积内S的质量减小的原因为:
您最近一年使用:0次
名校
解题方法
6 . 碘及碘的化合物在生产、生活中有广泛应用。在KI溶液中滴加少量 溶液发生有关反应如下:
溶液发生有关反应如下:
①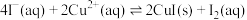
 ;
;
②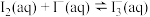 (棕黄色)
(棕黄色)  。
。
回答下列问题:
(1)在碘水中加入 ,萃取、分液得到紫红色液体和水层(M)。
,萃取、分液得到紫红色液体和水层(M)。
①由此可知, 的溶解度:四氯化碳>水,从结构角度分析其原因:
的溶解度:四氯化碳>水,从结构角度分析其原因:___________ ;
②检验M中是否有 的试剂是
的试剂是___________ 。
(2)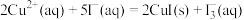

___________ 。
(3)一定温度下,在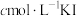 溶液中加入适量的
溶液中加入适量的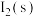 ,只发生反应
,只发生反应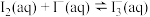
 。测得
。测得 与温度(T)关系如图所示。
与温度(T)关系如图所示。
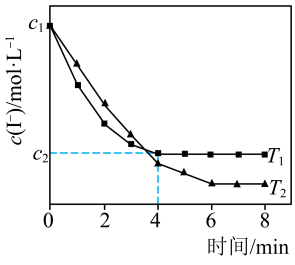
①
___________ (填“>”“<”或“=”)0。
② 温度下,0~4min时间段内
温度下,0~4min时间段内 平均速率
平均速率 为
为___________  。
。
(4)某温度下,起始在反应器中加入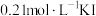 溶液和
溶液和 固体(忽略溶液体积变化),发生上述①②反应。测得
固体(忽略溶液体积变化),发生上述①②反应。测得 、
、 、
、 的平衡浓度与起始
的平衡浓度与起始 关系如图所示。
关系如图所示。
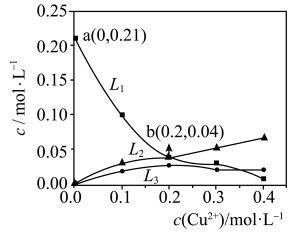
①起始 时,
时, 的平衡转化率为
的平衡转化率为___________ 。
②该温度下,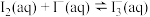 的平衡常数K=
的平衡常数K=___________ 。
(5) 的氧化性比
的氧化性比 的强,但是KI和
的强,但是KI和 发生复分解反应,不发生氧化还原反应,其原因是
发生复分解反应,不发生氧化还原反应,其原因是___________ 。
 溶液发生有关反应如下:
溶液发生有关反应如下:①
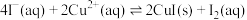
 ;
;②
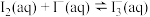 (棕黄色)
(棕黄色)  。
。回答下列问题:
(1)在碘水中加入
 ,萃取、分液得到紫红色液体和水层(M)。
,萃取、分液得到紫红色液体和水层(M)。①由此可知,
 的溶解度:四氯化碳>水,从结构角度分析其原因:
的溶解度:四氯化碳>水,从结构角度分析其原因:②检验M中是否有
 的试剂是
的试剂是(2)
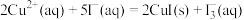

(3)一定温度下,在
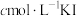 溶液中加入适量的
溶液中加入适量的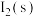 ,只发生反应
,只发生反应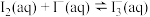
 。测得
。测得 与温度(T)关系如图所示。
与温度(T)关系如图所示。
①

②
 温度下,0~4min时间段内
温度下,0~4min时间段内 平均速率
平均速率 为
为 。
。(4)某温度下,起始在反应器中加入
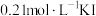 溶液和
溶液和 固体(忽略溶液体积变化),发生上述①②反应。测得
固体(忽略溶液体积变化),发生上述①②反应。测得 、
、 、
、 的平衡浓度与起始
的平衡浓度与起始 关系如图所示。
关系如图所示。
①起始
 时,
时, 的平衡转化率为
的平衡转化率为②该温度下,
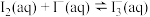 的平衡常数K=
的平衡常数K=(5)
 的氧化性比
的氧化性比 的强,但是KI和
的强,但是KI和 发生复分解反应,不发生氧化还原反应,其原因是
发生复分解反应,不发生氧化还原反应,其原因是
您最近一年使用:0次
解题方法
7 . 苯酚是重要的有机化工原料之一,工业上主要用于酚醛树脂、双酚、己内酰胺、水杨酸等的制备。回答下列问题:
(1)一定条件下,在CuCl2-FeCl3作催化剂的条件下,氧气直接氧化苯制备苯酚:2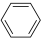 (g)
(g)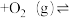 2
2 (g)△H<0,可分以下两步进行(其中b>0)
(g)△H<0,可分以下两步进行(其中b>0)
恒容密闭容器I:2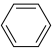 (g)
(g)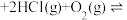 2
2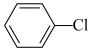 (g)
(g)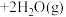 △H1=akJ·mol-1;
△H1=akJ·mol-1;
恒容密闭容器II: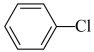 (g)
(g)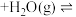
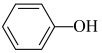 (g)
(g) △H2=bkJ·mol-1。
△H2=bkJ·mol-1。
①a___________ 0(填“大于”“小于”或“等于”,下同)。
②向容器I中加入10mol苯(g)、10molHCl(g)和一定量的O2(g),发生上述I中反应。苯的平衡转化率按不同投料比x[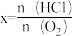 ]随温度的变化曲线如图所示。
]随温度的变化曲线如图所示。
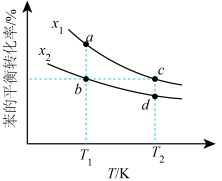
以下物理量大小关系有:图中所示投料比x1___________ x2;平衡常数Kb___________ Kc。T2温度下,加入物料后,x=2,测得初始压强为P0kPa,c点对应的HCl的平衡转化率为50%,则d点对应的平衡常数Kp=___________ 。(Kp是用气体平衡分压代替平衡浓度计算的平衡常数,气体平衡分压为平衡总压与其体积分数的积)
(2)改用乙酸铁催化苯直接羟基化制苯酚:在常压下,当反应时间为2h、乙酸用量为3.2mol时,改变反应温度,反应结果如表所示(转化率及收率均以苯酚的摩尔收率计)。
60℃时,苯酚选择性为___________ %(保留一位小数),温度高于50℃时,苯的转化率增大,而苯酚的选择性___________ (填“升高”“降低”或“不变”),乙酸铁催化苯直接羟基化合成苯酚的实验中反应温度的范围最好为___________ 。
(1)一定条件下,在CuCl2-FeCl3作催化剂的条件下,氧气直接氧化苯制备苯酚:2
 (g)
(g)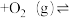 2
2 (g)△H<0,可分以下两步进行(其中b>0)
(g)△H<0,可分以下两步进行(其中b>0)恒容密闭容器I:2
 (g)
(g)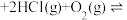 2
2 (g)
(g)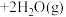 △H1=akJ·mol-1;
△H1=akJ·mol-1;恒容密闭容器II:
 (g)
(g)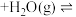
 (g)
(g) △H2=bkJ·mol-1。
△H2=bkJ·mol-1。①a
②向容器I中加入10mol苯(g)、10molHCl(g)和一定量的O2(g),发生上述I中反应。苯的平衡转化率按不同投料比x[
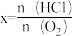 ]随温度的变化曲线如图所示。
]随温度的变化曲线如图所示。
以下物理量大小关系有:图中所示投料比x1
(2)改用乙酸铁催化苯直接羟基化制苯酚:在常压下,当反应时间为2h、乙酸用量为3.2mol时,改变反应温度,反应结果如表所示(转化率及收率均以苯酚的摩尔收率计)。
| 温度/℃ | 苯转化率/% | 苯酚收率/% | 苯酚选择性/% |
| 40 | 9.5 | 9.5 | 100 |
| 44.5 | 15.9 | 15.8 | 99.4 |
| 50 | 62.0 | 60.1 | 96.9 |
| 55.5 | 65.2 | 60.8 | 93.3 |
| 60 | 67.4 | 58 |
您最近一年使用:0次
解题方法
8 . 已知:CO2氧化C2H6制C2H4的主反应热化学方程式为:C2H6(g)+CO2(g)=C2H4(g)+CO(g)+H2O(g) △H=+177kJ/mol。该反应的历程分为如下两步:
反应①:C2H6(g)=C2H4(g)+H2(g)(快反应) △H1
反应②:H2(g)+CO2(g)=CO(g)+H2O(g)(慢反应) △H2=+42kJ/mol
下列说法不正确的是
反应①:C2H6(g)=C2H4(g)+H2(g)(快反应) △H1
反应②:H2(g)+CO2(g)=CO(g)+H2O(g)(慢反应) △H2=+42kJ/mol
下列说法不正确的是
| A.反应①在高温条件下可以自发进行 |
B.相比于提高 ,提高c(C2H6)对主反应速率影响更大 ,提高c(C2H6)对主反应速率影响更大 |
C.将 液化分离,有利提高C2H6的转化率 液化分离,有利提高C2H6的转化率 |
D.反应①的活化能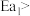 反应②的活化能 反应②的活化能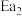 |
您最近一年使用:0次
9 . 硫酸是基础化学工业的重要产品,下列为接触法制硫酸的反应:
①4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g) ΔH=-3412kJ·mol-1
②2SO2(g)+O2(g)⇌2SO3(g) ΔH=-196.6kJ·mol-1
③SO3(g)+H2O(l)=H2SO4(l) ΔH=-130.3kJ·mol-1
下列说法正确的是
①4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g) ΔH=-3412kJ·mol-1
②2SO2(g)+O2(g)⇌2SO3(g) ΔH=-196.6kJ·mol-1
③SO3(g)+H2O(l)=H2SO4(l) ΔH=-130.3kJ·mol-1
下列说法正确的是
| A.反应②中使用高效催化剂释放出的热量更大 |
| B.反应①中1molFeS2(s)参与反应放出的热量为3412kJ |
| C.64gSO2与1molO2在密闭容器中发生反应释放出98.3kJ热量 |
D.FeS2生成H2SO4的热化学方程式可表示为2FeS2(s)+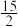 O2(g)+4H2O(l)=Fe2O3(s)+4H2SO4(l) ΔH=-2620.4kJ·mol-1 O2(g)+4H2O(l)=Fe2O3(s)+4H2SO4(l) ΔH=-2620.4kJ·mol-1 |
您最近一年使用:0次
10 . 二氧化碳的捕集和资源化利用是缓解温室效应的重要战略方向。回答下列问题:
(1)我国在二氧化碳催化加氢合成甲醇上取得了突破性进展,有关反应如下:
反应ⅰ

反应ⅱ

 和
和 合成甲醇的热化学方程式为
合成甲醇的热化学方程式为_______ 。
(2)在催化剂M的作用下, 的微观反应历程和相对能量(
的微观反应历程和相对能量( )如图所示,其中吸附在催化剂表面上的物种用“*”标注。已知:●表示C,•表示O,○表示H。
)如图所示,其中吸附在催化剂表面上的物种用“*”标注。已知:●表示C,•表示O,○表示H。
历程Ⅰ:
反应甲:
历程Ⅱ:
反应乙:_______
历程Ⅲ:
反应丙:
①历程Ⅱ中的反应乙可表示为_______ 。
②决定 的总反应速率的是历程
的总反应速率的是历程_______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
(3)将 和
和 按物质的量之比
按物质的量之比 充入一恒容密闭容器中,同时发生了反应ⅰ和反应ⅱ,测得
充入一恒容密闭容器中,同时发生了反应ⅰ和反应ⅱ,测得 的平衡转化率随温度、压强变化的情况如图所示。
的平衡转化率随温度、压强变化的情况如图所示。

①压强 、
、 、
、 由小到大的顺序为
由小到大的顺序为_______ 。
②B点、A点的化学反应速率大小:
_______ 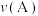 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
③温度高于543K时, 的平衡转化率随温度的升高而增大的原因是
的平衡转化率随温度的升高而增大的原因是_______ 。
④图中M点对应的温度下,已知 的选择性(生成的
的选择性(生成的 与转化的
与转化的 的百分比)为40%,该温度下反应ⅱ的平衡常数为
的百分比)为40%,该温度下反应ⅱ的平衡常数为_______ (结果保留3位小数)。
(4)催化 加氢合成乙酸在减少碳排放的同时还可以生产重要的化工原料。已知电离度
加氢合成乙酸在减少碳排放的同时还可以生产重要的化工原料。已知电离度 ,
,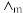 为一定浓度下电解质的摩尔电导率,
为一定浓度下电解质的摩尔电导率,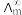 为无限稀释时溶液的摩尔电导率,
为无限稀释时溶液的摩尔电导率, (
( )。某小组实验测得
)。某小组实验测得 时,
时, 乙酸的
乙酸的 。
。
①该条件下测定的乙酸的电离平衡常数 为
为_______ (列出计算式,不需化简)。
②在298K时,几种离子的摩尔电导率如表所示。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现 的再生,从导电性角度选择,最适宜的电解质为出
的再生,从导电性角度选择,最适宜的电解质为出_______ (填化学式)。
(1)我国在二氧化碳催化加氢合成甲醇上取得了突破性进展,有关反应如下:
反应ⅰ


反应ⅱ


 和
和 合成甲醇的热化学方程式为
合成甲醇的热化学方程式为(2)在催化剂M的作用下,
 的微观反应历程和相对能量(
的微观反应历程和相对能量( )如图所示,其中吸附在催化剂表面上的物种用“*”标注。已知:●表示C,•表示O,○表示H。
)如图所示,其中吸附在催化剂表面上的物种用“*”标注。已知:●表示C,•表示O,○表示H。历程Ⅰ:

反应甲:

历程Ⅱ:

反应乙:_______
历程Ⅲ:

反应丙:

①历程Ⅱ中的反应乙可表示为
②决定
 的总反应速率的是历程
的总反应速率的是历程(3)将
 和
和 按物质的量之比
按物质的量之比 充入一恒容密闭容器中,同时发生了反应ⅰ和反应ⅱ,测得
充入一恒容密闭容器中,同时发生了反应ⅰ和反应ⅱ,测得 的平衡转化率随温度、压强变化的情况如图所示。
的平衡转化率随温度、压强变化的情况如图所示。
①压强
 、
、 、
、 由小到大的顺序为
由小到大的顺序为②B点、A点的化学反应速率大小:

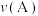 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。③温度高于543K时,
 的平衡转化率随温度的升高而增大的原因是
的平衡转化率随温度的升高而增大的原因是④图中M点对应的温度下,已知
 的选择性(生成的
的选择性(生成的 与转化的
与转化的 的百分比)为40%,该温度下反应ⅱ的平衡常数为
的百分比)为40%,该温度下反应ⅱ的平衡常数为(4)催化
 加氢合成乙酸在减少碳排放的同时还可以生产重要的化工原料。已知电离度
加氢合成乙酸在减少碳排放的同时还可以生产重要的化工原料。已知电离度 ,
,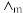 为一定浓度下电解质的摩尔电导率,
为一定浓度下电解质的摩尔电导率,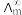 为无限稀释时溶液的摩尔电导率,
为无限稀释时溶液的摩尔电导率, (
( )。某小组实验测得
)。某小组实验测得 时,
时, 乙酸的
乙酸的 。
。①该条件下测定的乙酸的电离平衡常数
 为
为②在298K时,几种离子的摩尔电导率如表所示。已知:摩尔电导率越大,溶液的导电性越好。空间站通过电解水实现
 的再生,从导电性角度选择,最适宜的电解质为出
的再生,从导电性角度选择,最适宜的电解质为出| 离子种类 |  |  |  |  |  |  |
摩尔电导率 | 50.18 | 71.44 | 76.34 | 73.40 | 73.52 | 50.11 |
您最近一年使用:0次



