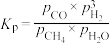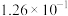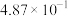1 . 羰基硫(COS)是一种粮食熏蒸剂,能防止某些害虫和真菌的危害,工业上用于合成除草剂、杀草丹、燕麦敌、杀虫剂巴丹等。其结构与 类似。工业上一般通过
类似。工业上一般通过 或者CO与
或者CO与 反应制取COS,发生的相关反应如下:
反应制取COS,发生的相关反应如下:
i.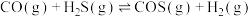
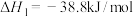
ii.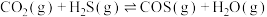
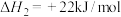
iii.

(1)
_______ 。
(2)COS的中心原子的杂化方式为_______ 。
(3)在一定温度下,将4molCO和 通入一固定容积的密闭容器中发生上述反应i。
通入一固定容积的密闭容器中发生上述反应i。
①能证明上述反应达到平衡的标志是_______ (填字母)。
A.CO和 的转化率相等 B.
的转化率相等 B. 的体积分数不再变化
的体积分数不再变化
C.混合气体的密度不再变化 D.CO、 、COS、
、COS、 浓度之比为1:1:1:1
浓度之比为1:1:1:1
②上述反应达到平衡后,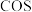 所占的体积分数为12.5%,则该反应的平衡常数为
所占的体积分数为12.5%,则该反应的平衡常数为_______ (保留两位有效数字)。若此时再向体系中加入0.5molCO和 ,平衡将
,平衡将_______ (填“向正反应方向”“向逆反应方向”或“不”)移动;理由是_______ 。
(4)将4molCO和 通入一固定容积的密闭容器中发生上述反应i,反应5分钟,CO的转化率随温度的变化关系如图所示。a点
通入一固定容积的密闭容器中发生上述反应i,反应5分钟,CO的转化率随温度的变化关系如图所示。a点_______ (填“是”或“不是”)平衡状态,判断的理由是_______ 。 、1molCO和
、1molCO和 通入一固定容积的密闭容器中发生上述反应i、ii和iii,CO、
通入一固定容积的密闭容器中发生上述反应i、ii和iii,CO、 和
和 平衡时的转化率如图所示,
平衡时的转化率如图所示, 转化率先减小后增大的原因是
转化率先减小后增大的原因是_______ 。
 类似。工业上一般通过
类似。工业上一般通过 或者CO与
或者CO与 反应制取COS,发生的相关反应如下:
反应制取COS,发生的相关反应如下:i.
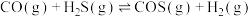
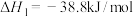
ii.
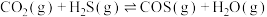
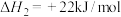
iii.


(1)

(2)COS的中心原子的杂化方式为
(3)在一定温度下,将4molCO和
 通入一固定容积的密闭容器中发生上述反应i。
通入一固定容积的密闭容器中发生上述反应i。①能证明上述反应达到平衡的标志是
A.CO和
 的转化率相等 B.
的转化率相等 B. 的体积分数不再变化
的体积分数不再变化C.混合气体的密度不再变化 D.CO、
 、COS、
、COS、 浓度之比为1:1:1:1
浓度之比为1:1:1:1②上述反应达到平衡后,
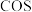 所占的体积分数为12.5%,则该反应的平衡常数为
所占的体积分数为12.5%,则该反应的平衡常数为 ,平衡将
,平衡将(4)将4molCO和
 通入一固定容积的密闭容器中发生上述反应i,反应5分钟,CO的转化率随温度的变化关系如图所示。a点
通入一固定容积的密闭容器中发生上述反应i,反应5分钟,CO的转化率随温度的变化关系如图所示。a点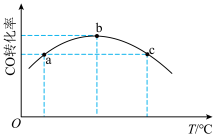
 、1molCO和
、1molCO和 通入一固定容积的密闭容器中发生上述反应i、ii和iii,CO、
通入一固定容积的密闭容器中发生上述反应i、ii和iii,CO、 和
和 平衡时的转化率如图所示,
平衡时的转化率如图所示, 转化率先减小后增大的原因是
转化率先减小后增大的原因是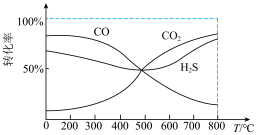
您最近一年使用:0次
名校
解题方法
2 . 深入研究碳、氮元素的物质转化有着重要的实际意义,汽车尾气净化装置中CO和NO发生如下反应:
i.
 ,
,
ii.
 ,
,
iii.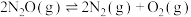
 ,
,
回答下列问题:
(1)上述反应的 的线性关系如图所示(
的线性关系如图所示( )。
)。
_______ (填“>”或“<”)0,反应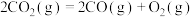 的
的
_______ (用 、
、 表示)。
表示)。 ,初始总压强为
,初始总压强为 ,仅发生以上反应ⅰ、ⅱ,且反应ⅰ的
,仅发生以上反应ⅰ、ⅱ,且反应ⅰ的 ,
, ,
, ,
, 分别为正、逆反应速率常数。充分反应达平衡时总压强为
分别为正、逆反应速率常数。充分反应达平衡时总压强为 ,
, 的物质的量为1.25mol,则
的物质的量为1.25mol,则
_______ 。
(3)CO和NO发生上述三个反应,在不同条件下达到平衡时,在 K时NO的转化率与
K时NO的转化率与 的变化曲线及
的变化曲线及 时NO的转化率与T的变化曲线如图所示。
时NO的转化率与T的变化曲线如图所示。 时NO的转化率与T的变化曲线为
时NO的转化率与T的变化曲线为_______ 曲线(填“Ⅰ”或“Ⅱ”),A点后NO的平衡转化率增大的原因是_______ 。
(4)CO、NO均能够与血红蛋白(Hb)中 形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。已知:CO进入血液后有如下平衡:
形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。已知:CO进入血液后有如下平衡: 。
。
①从化学平衡角度简述CO的中毒原理:_______ 。
②已知反应
 实验表明,人体内HbCO与
实验表明,人体内HbCO与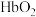 的浓度之比为1∶50已足以使人智力受损,则抽烟时吸入肺部的空气中CO与
的浓度之比为1∶50已足以使人智力受损,则抽烟时吸入肺部的空气中CO与 的体积比大于
的体积比大于_______ 即达到智力受损的程度。
i.

 ,
,
ii.

 ,
,
iii.
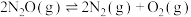
 ,
,
回答下列问题:
(1)上述反应的
 的线性关系如图所示(
的线性关系如图所示( )。
)。
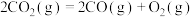 的
的
 、
、 表示)。
表示)。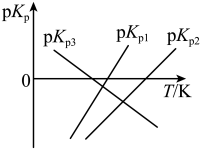
 ,初始总压强为
,初始总压强为 ,仅发生以上反应ⅰ、ⅱ,且反应ⅰ的
,仅发生以上反应ⅰ、ⅱ,且反应ⅰ的 ,
, ,
, ,
, 分别为正、逆反应速率常数。充分反应达平衡时总压强为
分别为正、逆反应速率常数。充分反应达平衡时总压强为 ,
, 的物质的量为1.25mol,则
的物质的量为1.25mol,则
(3)CO和NO发生上述三个反应,在不同条件下达到平衡时,在
 K时NO的转化率与
K时NO的转化率与 的变化曲线及
的变化曲线及 时NO的转化率与T的变化曲线如图所示。
时NO的转化率与T的变化曲线如图所示。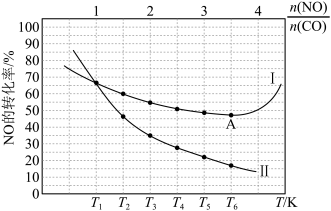
 时NO的转化率与T的变化曲线为
时NO的转化率与T的变化曲线为(4)CO、NO均能够与血红蛋白(Hb)中
 形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。已知:CO进入血液后有如下平衡:
形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。已知:CO进入血液后有如下平衡: 。
。①从化学平衡角度简述CO的中毒原理:
②已知反应

 实验表明,人体内HbCO与
实验表明,人体内HbCO与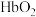 的浓度之比为1∶50已足以使人智力受损,则抽烟时吸入肺部的空气中CO与
的浓度之比为1∶50已足以使人智力受损,则抽烟时吸入肺部的空气中CO与 的体积比大于
的体积比大于
您最近一年使用:0次
名校
解题方法
3 . 我国提出力争2060年前实现碳中和,以 为原料催化加氢制备甲醇具有较好的发展前景。已知:
为原料催化加氢制备甲醇具有较好的发展前景。已知:
I.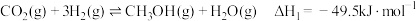
Ⅱ.
Ⅲ.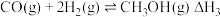
回答下列问题:
(1)反成I在_________ (填“高温”“低温”或“任何温度”)条件下能够自发进行,反应Ⅲ的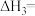
_________  。
。
(2)将 和
和 按
按 通入密闭容器中发生反应Ⅰ和反应Ⅱ,测得不同温度下
通入密闭容器中发生反应Ⅰ和反应Ⅱ,测得不同温度下 的平衡转化率以及
的平衡转化率以及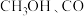 选择性的变化如图所示(选择性为目标产物的物质的量在转化的
选择性的变化如图所示(选择性为目标产物的物质的量在转化的 的总物质的量中的比率)。
的总物质的量中的比率)。 的选择性曲线为
的选择性曲线为_________ (填“a”或“b”)。
②不同压强下, 的平衡转化率如图所示,则
的平衡转化率如图所示,则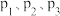 由大到小的顺序
由大到小的顺序_________ 。
③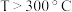 时,
时,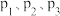 三条曲线接近重合的原因是
三条曲线接近重合的原因是_______________ 。
④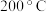 时,在某催化剂作用下
时,在某催化剂作用下 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为
的选择性为 ;保持投料比、反应时间和温度不变,一定能提高
;保持投料比、反应时间和温度不变,一定能提高 选择性的措施有
选择性的措施有_________ (写出一种即可)。
(3)已知:对于反应,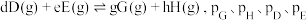 为各组分的平衡分压,
为各组分的平衡分压,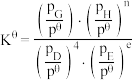 ,其中
,其中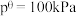 ,分压=总压×该组分物质的量分数。
,分压=总压×该组分物质的量分数。
①则图为反应_________ (填“Ⅱ”或“Ⅲ”)的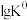 随
随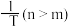 的变化关系。
的变化关系。
②在图中n点对应温度下、原料组成为 ,初始总压为
,初始总压为 的恒容密闭容器中进行反应,体系达到平衡时
的恒容密闭容器中进行反应,体系达到平衡时 的分压为
的分压为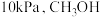 的分压为
的分压为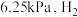 的平衡转化率为
的平衡转化率为_________ 。
 为原料催化加氢制备甲醇具有较好的发展前景。已知:
为原料催化加氢制备甲醇具有较好的发展前景。已知:I.
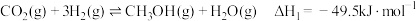
Ⅱ.

Ⅲ.
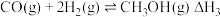
回答下列问题:
(1)反成I在
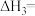
 。
。(2)将
 和
和 按
按 通入密闭容器中发生反应Ⅰ和反应Ⅱ,测得不同温度下
通入密闭容器中发生反应Ⅰ和反应Ⅱ,测得不同温度下 的平衡转化率以及
的平衡转化率以及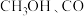 选择性的变化如图所示(选择性为目标产物的物质的量在转化的
选择性的变化如图所示(选择性为目标产物的物质的量在转化的 的总物质的量中的比率)。
的总物质的量中的比率)。
 的选择性曲线为
的选择性曲线为②不同压强下,
 的平衡转化率如图所示,则
的平衡转化率如图所示,则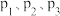 由大到小的顺序
由大到小的顺序③
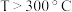 时,
时,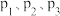 三条曲线接近重合的原因是
三条曲线接近重合的原因是④
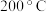 时,在某催化剂作用下
时,在某催化剂作用下 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为
的选择性为 ;保持投料比、反应时间和温度不变,一定能提高
;保持投料比、反应时间和温度不变,一定能提高 选择性的措施有
选择性的措施有(3)已知:对于反应,
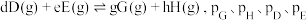 为各组分的平衡分压,
为各组分的平衡分压,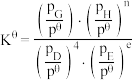 ,其中
,其中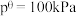 ,分压=总压×该组分物质的量分数。
,分压=总压×该组分物质的量分数。①则图为反应
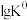 随
随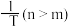 的变化关系。
的变化关系。②在图中n点对应温度下、原料组成为
 ,初始总压为
,初始总压为 的恒容密闭容器中进行反应,体系达到平衡时
的恒容密闭容器中进行反应,体系达到平衡时 的分压为
的分压为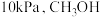 的分压为
的分压为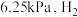 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
4 . 在一定的温度和压强下,将按一定比例混合的CO2和H2通过装有催化剂的反应器可得到甲烷.
已知: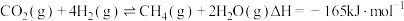
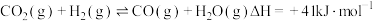
催化剂的选择是CO2甲烷化技术的核心.在两种不同催化剂作用下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示.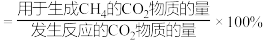
下列有关说法错误的是
已知:
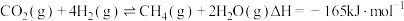
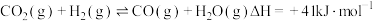
催化剂的选择是CO2甲烷化技术的核心.在两种不同催化剂作用下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如图所示.
下列有关说法错误的是
A.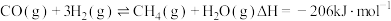 |
| B.延长W点的反应时间,能提高CO2的转化率 |
| C.在260~320℃间,以Ni-CeO2为催化剂,升高温度CH4的产率不变 |
| D.选择合适的催化剂、合适的温度有利于提高CH4的选择性 |
您最近一年使用:0次
名校
5 . 研究硫及其化合物的性质具有重要意义。
Ⅰ.已知 可以催化二氧化硫在水溶液中发生的歧化反应:
可以催化二氧化硫在水溶液中发生的歧化反应:

 ,催化原理分为两步,
,催化原理分为两步,
第一步反应为吸热的慢反应:
第二步反应为放热的快反应: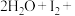 ______
______ ______+______
______+______
(1)请补充第二步反应:______ 。
(2)能正确表示 催化
催化 歧化反应原理的能量变化示意图为______(填标号)。
歧化反应原理的能量变化示意图为______(填标号)。
Ⅱ.工业制硫酸,在接触室发生反应: ,在1L的恒容密闭容器中充入2mol
,在1L的恒容密闭容器中充入2mol 和1mol
和1mol ,在不同温度下测得
,在不同温度下测得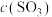 与时间的关系如图A:
与时间的关系如图A:
______ 0(填“>”“<”或“=”)。
(4)能证明反应已经达到平衡状态的是______ (填序号)。
①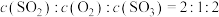
②单位时间内生成n mol 的同时消耗n mol
的同时消耗n mol
③反应速率
④温度和体积一定时,容器内压强不再变化
⑤温度和体积一定时,混合气体的密度不再变化
(5)反应开始到10min时 的平均反应速率
的平均反应速率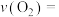
______ mol/(L·min); 时该反应的平衡常数
时该反应的平衡常数
______ L/mol。
(6)一定条件下在恒温恒容的密闭容器中按一定比例充入 和
和 ,平衡时
,平衡时 的体积分数随
的体积分数随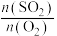 的变化如图B,则A、B、C三状态中,
的变化如图B,则A、B、C三状态中, 的转化率最小的是
的转化率最小的是______ 点,当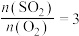 时,达到平衡状态
时,达到平衡状态 的体积分数可能是D、E、F三点中的
的体积分数可能是D、E、F三点中的______ 点。
Ⅰ.已知
 可以催化二氧化硫在水溶液中发生的歧化反应:
可以催化二氧化硫在水溶液中发生的歧化反应:
 ,催化原理分为两步,
,催化原理分为两步,第一步反应为吸热的慢反应:

第二步反应为放热的快反应:
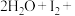 ______
______ ______+______
______+______
(1)请补充第二步反应:
(2)能正确表示
 催化
催化 歧化反应原理的能量变化示意图为______(填标号)。
歧化反应原理的能量变化示意图为______(填标号)。A.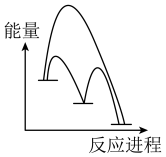 | B.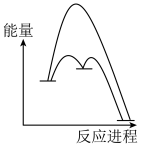 |
C.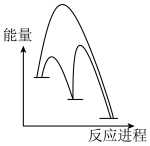 | D.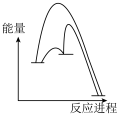 |
Ⅱ.工业制硫酸,在接触室发生反应:
 ,在1L的恒容密闭容器中充入2mol
,在1L的恒容密闭容器中充入2mol 和1mol
和1mol ,在不同温度下测得
,在不同温度下测得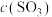 与时间的关系如图A:
与时间的关系如图A: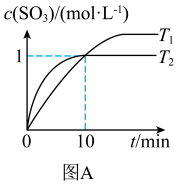

(4)能证明反应已经达到平衡状态的是
①
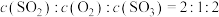
②单位时间内生成n mol
 的同时消耗n mol
的同时消耗n mol
③反应速率

④温度和体积一定时,容器内压强不再变化
⑤温度和体积一定时,混合气体的密度不再变化
(5)反应开始到10min时
 的平均反应速率
的平均反应速率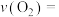
 时该反应的平衡常数
时该反应的平衡常数
(6)一定条件下在恒温恒容的密闭容器中按一定比例充入
 和
和 ,平衡时
,平衡时 的体积分数随
的体积分数随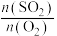 的变化如图B,则A、B、C三状态中,
的变化如图B,则A、B、C三状态中, 的转化率最小的是
的转化率最小的是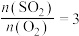 时,达到平衡状态
时,达到平衡状态 的体积分数可能是D、E、F三点中的
的体积分数可能是D、E、F三点中的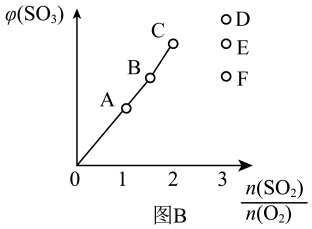
您最近一年使用:0次
名校
解题方法
6 . 燃油汽车尾气中含有NO、 、CO等有毒气体造成大气污染,可在汽车尾气排放装置中加催化转化装置,将有毒气体转化为无毒气体。反应原理如下:
、CO等有毒气体造成大气污染,可在汽车尾气排放装置中加催化转化装置,将有毒气体转化为无毒气体。反应原理如下:
反应①:

反应②: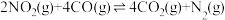
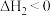
回答下列问题:
(1)已知:1 mol物质中化学键断裂时所需能量如下表。
CO燃烧热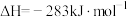 ,则反应①的
,则反应①的
___________  。
。
(2)恒温恒压密闭容器中充入一定量NO(g)和CO(g)(不考虑反应②),下列条件不能判断反应①达到平衡状态的是___________(填标号)。
(3)瑞典化学家阿伦尼乌斯根据实验结果,提出了温度与反应速率常数关系的经验公式: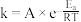 [k为反应速率常数,A为比例常数,e为自然对数的底数,R为摩尔气体常数,T为开尔文温度,
[k为反应速率常数,A为比例常数,e为自然对数的底数,R为摩尔气体常数,T为开尔文温度, 为活化能(
为活化能( )]。
)]。
①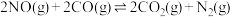 反应达到平衡后,升高温度,正反应速率常数增大的倍数
反应达到平衡后,升高温度,正反应速率常数增大的倍数___________ (填“大于”“小于”或“等于”)逆反应速率常数增大的倍数。
②由此判断下列说法正确的是___________ (填标号, 、
、 为正、逆反应速率常数)。
为正、逆反应速率常数)。
A.其他条件不变,升高温度, 增大,
增大, 变小
变小
B.其他条件不变,使用催化剂, 、
、 同倍数增大
同倍数增大
C.其他条件不变,增大反应物浓度 增大,
增大, 不变
不变
D.其他条件不变,减小压强, 、
、 都变小
都变小
(4)探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,测量相同时间内逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示。曲线上a点的脱氮率___________ (填“ ”“
”“ ”或“
”或“ ”)对应温度下的平衡脱氮率。催化剂
”)对应温度下的平衡脱氮率。催化剂 条件下,450℃后,脱氮率随温度升高而下降的原因可能是
条件下,450℃后,脱氮率随温度升高而下降的原因可能是___________ 。 催化还原NO,也可以消除氮氧化物的污染。在适当催化剂的作用下,用
催化还原NO,也可以消除氮氧化物的污染。在适当催化剂的作用下,用 脱氮过程中存在主反应和副反应:
脱氮过程中存在主反应和副反应:
主反应: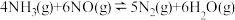

副反应: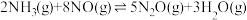

在TK下,向恒容密闭容器中充入2 mol 和3 mol NO,发生上述反应;若初始压强为20MPa,反应达到平衡时,压强仍为20 MPa且
和3 mol NO,发生上述反应;若初始压强为20MPa,反应达到平衡时,压强仍为20 MPa且 的分压为4MPa。
的分压为4MPa。
①该温度下主反应的压强平衡常数
___________ (保留1位小数)。
②若反应10min达到上述平衡状态,则用 表示的平均速率
表示的平均速率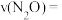
___________ 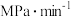 。
。
 、CO等有毒气体造成大气污染,可在汽车尾气排放装置中加催化转化装置,将有毒气体转化为无毒气体。反应原理如下:
、CO等有毒气体造成大气污染,可在汽车尾气排放装置中加催化转化装置,将有毒气体转化为无毒气体。反应原理如下:反应①:


反应②:
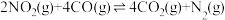
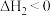
回答下列问题:
(1)已知:1 mol物质中化学键断裂时所需能量如下表。
| 物质 |  |  |  |
| 能量/kJ | 945 | 498 | 631 |
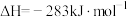 ,则反应①的
,则反应①的
 。
。(2)恒温恒压密闭容器中充入一定量NO(g)和CO(g)(不考虑反应②),下列条件不能判断反应①达到平衡状态的是___________(填标号)。
| A.混合气体的颜色保持不变 |
| B.混合气体的平均相对分子质量保持不变 |
C. 的体积分数不变 的体积分数不变 |
D.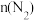 和 和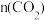 的比值一定 的比值一定 |
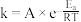 [k为反应速率常数,A为比例常数,e为自然对数的底数,R为摩尔气体常数,T为开尔文温度,
[k为反应速率常数,A为比例常数,e为自然对数的底数,R为摩尔气体常数,T为开尔文温度, 为活化能(
为活化能( )]。
)]。①
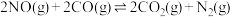 反应达到平衡后,升高温度,正反应速率常数增大的倍数
反应达到平衡后,升高温度,正反应速率常数增大的倍数②由此判断下列说法正确的是
 、
、 为正、逆反应速率常数)。
为正、逆反应速率常数)。A.其他条件不变,升高温度,
 增大,
增大, 变小
变小B.其他条件不变,使用催化剂,
 、
、 同倍数增大
同倍数增大C.其他条件不变,增大反应物浓度
 增大,
增大, 不变
不变D.其他条件不变,减小压强,
 、
、 都变小
都变小(4)探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,测量相同时间内逸出气体中NO含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示。曲线上a点的脱氮率
 ”“
”“ ”或“
”或“ ”)对应温度下的平衡脱氮率。催化剂
”)对应温度下的平衡脱氮率。催化剂 条件下,450℃后,脱氮率随温度升高而下降的原因可能是
条件下,450℃后,脱氮率随温度升高而下降的原因可能是
 催化还原NO,也可以消除氮氧化物的污染。在适当催化剂的作用下,用
催化还原NO,也可以消除氮氧化物的污染。在适当催化剂的作用下,用 脱氮过程中存在主反应和副反应:
脱氮过程中存在主反应和副反应:主反应:
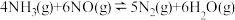

副反应:
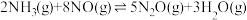

在TK下,向恒容密闭容器中充入2 mol
 和3 mol NO,发生上述反应;若初始压强为20MPa,反应达到平衡时,压强仍为20 MPa且
和3 mol NO,发生上述反应;若初始压强为20MPa,反应达到平衡时,压强仍为20 MPa且 的分压为4MPa。
的分压为4MPa。①该温度下主反应的压强平衡常数

②若反应10min达到上述平衡状态,则用
 表示的平均速率
表示的平均速率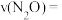
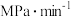 。
。
您最近一年使用:0次
名校
7 . 我国提出2060年前实现碳中和,为有效降低大气 中的含量,以
中的含量,以 为原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。
为原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。 在固体催化剂表面加氢合成甲烷过程中发生如下反应:
在固体催化剂表面加氢合成甲烷过程中发生如下反应:
Ⅰ.主反应:

Ⅱ.副反应:

(1)已知:Ⅲ.
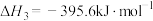
Ⅳ.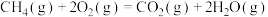

___________ 。
(2) 加氢合成甲烷时,通常控制温度为500℃左右,其可能的原因为___________。
加氢合成甲烷时,通常控制温度为500℃左右,其可能的原因为___________。
(3)500℃时,向1L恒容密闭容器中充入4mol 和12mol
和12mol ,初始压强为p,20min时主、副反应都达到平衡状态,测得
,初始压强为p,20min时主、副反应都达到平衡状态,测得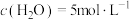 ,体系压强为
,体系压强为 ,则0~20min内
,则0~20min内
___________  ,平衡时
,平衡时 选择性=
选择性=___________ ( 选择性
选择性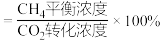 ,计算保留三位有效数字,下同),副反应的
,计算保留三位有效数字,下同),副反应的
___________ 。
(4)以 催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为
催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为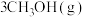
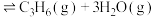 。该反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式
。该反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式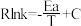 ,(Ea为活化能,k为速率常数,R和C为常数)。当改变外界条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是
,(Ea为活化能,k为速率常数,R和C为常数)。当改变外界条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是___________ 。 配体:四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为
配体:四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为 ,则M元素为
,则M元素为___________ (填元素符号):在该化合物中,M离子的价电子排布式为___________ 。
 中的含量,以
中的含量,以 为原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。
为原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。 在固体催化剂表面加氢合成甲烷过程中发生如下反应:
在固体催化剂表面加氢合成甲烷过程中发生如下反应:Ⅰ.主反应:


Ⅱ.副反应:


(1)已知:Ⅲ.

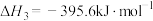
Ⅳ.
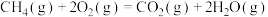

(2)
 加氢合成甲烷时,通常控制温度为500℃左右,其可能的原因为___________。
加氢合成甲烷时,通常控制温度为500℃左右,其可能的原因为___________。| A.反应速率快 | B.平衡转化率高 |
| C.催化剂活性高 | D.主反应催化剂选择性好 |
(3)500℃时,向1L恒容密闭容器中充入4mol
 和12mol
和12mol ,初始压强为p,20min时主、副反应都达到平衡状态,测得
,初始压强为p,20min时主、副反应都达到平衡状态,测得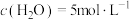 ,体系压强为
,体系压强为 ,则0~20min内
,则0~20min内
 ,平衡时
,平衡时 选择性=
选择性= 选择性
选择性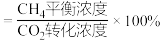 ,计算保留三位有效数字,下同),副反应的
,计算保留三位有效数字,下同),副反应的
(4)以
 催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为
催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为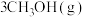
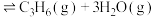 。该反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式
。该反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式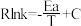 ,(Ea为活化能,k为速率常数,R和C为常数)。当改变外界条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是
,(Ea为活化能,k为速率常数,R和C为常数)。当改变外界条件时,实验数据如图中的曲线b所示,则实验可能改变的外界条件是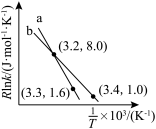
 配体:四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为
配体:四面体中心为硼原子,顶点均为氢原子。若其摩尔质量为 ,则M元素为
,则M元素为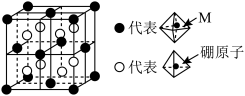
您最近一年使用:0次
名校
解题方法
8 . 丙烷的价格低廉且产量大,而丙烯及其衍生物具有较高的经济附加值,因此丙烷脱氢制丙烯具有重要的价值。回答下列问题:
(1)已知下列反应的热化学方程式:
直接脱氢
反应①:

反应②: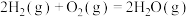

计算 氧化丙烷脱氢反应③:
氧化丙烷脱氢反应③: 的
的
___________  。
。
(2)已知下列键能数据,结合反应①数据,计算 的键能是
的键能是___________  。
。
(3)一定温度下,向密闭容器中充入1mol ,发生反应①。
,发生反应①。
①若该反应在恒压环境中进行,常通过向体系中通入稀有气体Ar的方式来提高 的平衡转化率,原因是
的平衡转化率,原因是___________ 。
②若该反应在恒容环境中进行,用压强传感器测出容器内体系压强随时间的变化关系如图a所示,计算该温度下反应①的平衡常数
___________ kPa( 为用平衡时各气体分压代替气体的浓度表示的平衡常数,分压=总压×物质的量分数)。若保持相同反应时间,在不同温度下,丙烯产率如图b所示,丙烯产率在425℃之前随温度升高而增大的原因可能是
为用平衡时各气体分压代替气体的浓度表示的平衡常数,分压=总压×物质的量分数)。若保持相同反应时间,在不同温度下,丙烯产率如图b所示,丙烯产率在425℃之前随温度升高而增大的原因可能是___________ 、___________ ,随着温度继续升高,丙烷可能分解为其他产物。
 作催化剂,对反应③的机理展开研究。以
作催化剂,对反应③的机理展开研究。以 和
和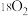 为原料,初期产物中没有检测到
为原料,初期产物中没有检测到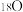 ;以含有
;以含有 的
的 (D为
(D为 )和
)和 为原料,反应过程中没有检测到
为原料,反应过程中没有检测到 。下列推断合理的是
。下列推断合理的是___________ (填标号)。
A. 先吸附氧气,吸附的氧气直接与吸附的丙烷反应
先吸附氧气,吸附的氧气直接与吸附的丙烷反应
B. 直接氧化吸附的丙烷,吸附的氧气补充
直接氧化吸附的丙烷,吸附的氧气补充 中反应掉的氧
中反应掉的氧
C. 催化丙烷脱氢过程中,碳氢键的断裂是可逆的
催化丙烷脱氢过程中,碳氢键的断裂是可逆的
(5)基于电化学原理,我国科学家利用固体氧化物电解池实现高选择性 电化学脱氢制
电化学脱氢制 的工艺,装置如图c,则
的工艺,装置如图c,则 生成
生成 的电极反应式为
的电极反应式为___________ 。
(1)已知下列反应的热化学方程式:
直接脱氢
反应①:


反应②:
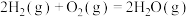

计算
 氧化丙烷脱氢反应③:
氧化丙烷脱氢反应③: 的
的
 。
。(2)已知下列键能数据,结合反应①数据,计算
 的键能是
的键能是 。
。| 化学键 |  |  |  |
键能/( ) ) | 347.7 | 413.4 | 436.0 |
(3)一定温度下,向密闭容器中充入1mol
 ,发生反应①。
,发生反应①。①若该反应在恒压环境中进行,常通过向体系中通入稀有气体Ar的方式来提高
 的平衡转化率,原因是
的平衡转化率,原因是②若该反应在恒容环境中进行,用压强传感器测出容器内体系压强随时间的变化关系如图a所示,计算该温度下反应①的平衡常数

 为用平衡时各气体分压代替气体的浓度表示的平衡常数,分压=总压×物质的量分数)。若保持相同反应时间,在不同温度下,丙烯产率如图b所示,丙烯产率在425℃之前随温度升高而增大的原因可能是
为用平衡时各气体分压代替气体的浓度表示的平衡常数,分压=总压×物质的量分数)。若保持相同反应时间,在不同温度下,丙烯产率如图b所示,丙烯产率在425℃之前随温度升高而增大的原因可能是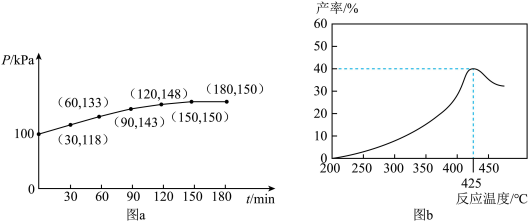
 作催化剂,对反应③的机理展开研究。以
作催化剂,对反应③的机理展开研究。以 和
和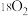 为原料,初期产物中没有检测到
为原料,初期产物中没有检测到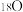 ;以含有
;以含有 的
的 (D为
(D为 )和
)和 为原料,反应过程中没有检测到
为原料,反应过程中没有检测到 。下列推断合理的是
。下列推断合理的是A.
 先吸附氧气,吸附的氧气直接与吸附的丙烷反应
先吸附氧气,吸附的氧气直接与吸附的丙烷反应B.
 直接氧化吸附的丙烷,吸附的氧气补充
直接氧化吸附的丙烷,吸附的氧气补充 中反应掉的氧
中反应掉的氧C.
 催化丙烷脱氢过程中,碳氢键的断裂是可逆的
催化丙烷脱氢过程中,碳氢键的断裂是可逆的(5)基于电化学原理,我国科学家利用固体氧化物电解池实现高选择性
 电化学脱氢制
电化学脱氢制 的工艺,装置如图c,则
的工艺,装置如图c,则 生成
生成 的电极反应式为
的电极反应式为 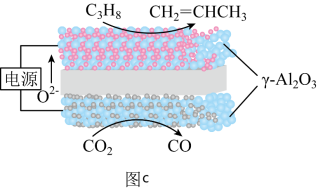
您最近一年使用:0次
9 . 低碳烯烃是重要的化工原料,广泛用于生产塑料、溶剂、药物、化妆品等。低碳烯烃主要是指乙烯、丙烯、丁烯。回答下列问题:
Ⅰ.我国科学家研究出新型催化剂 /ZMS—5,能使
/ZMS—5,能使 加氢生成乙烯,反应过程如图所示:
加氢生成乙烯,反应过程如图所示:
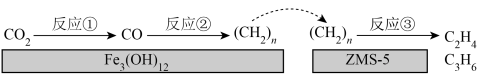
(1) 催化
催化 加氢的反应由反应①和反应②两步完成,反应①的活化能
加氢的反应由反应①和反应②两步完成,反应①的活化能 >反应②的活化能
>反应②的活化能 ,则
,则 催化
催化 加氢反应的决速步骤是
加氢反应的决速步骤是___________ (填“反应①”或“反应②”)。反应③为解聚、烯烃异构化反应,烯烃异构化是指改变烯烃结构而相对分子质量不变的反应过程,化工生产中的下列烯烃能发生异构化反应的是___________ (填字母)。
A.乙烯 B.2-甲基丙烯 C.2,3-二甲基-1-丁烯
Ⅱ.丙烯作为化工原料,其用量仅次于乙烯,应用丙烷脱氢制丙烯成为丙烯的重要来源,涉及的主要反应如下:
ⅰ.

ⅱ.

(2)

___________  。
。
(3)按起始投料比 将气体匀速通入到恒压(100kPa)密闭容器中,发生反应ⅰ和反应ⅱ。在相同时间不同温度(T)下,测得反应过程中
将气体匀速通入到恒压(100kPa)密闭容器中,发生反应ⅰ和反应ⅱ。在相同时间不同温度(T)下,测得反应过程中 、
、 的转化率变化曲线如图所示:
的转化率变化曲线如图所示:

M表示___________ (填“ ”或“
”或“ ”)的转化率随温度变化的曲线;C点后,随着温度升高,主要进行的反应是
”)的转化率随温度变化的曲线;C点后,随着温度升高,主要进行的反应是___________ (填“ⅰ”或“ⅱ”),该反应在温度为 K时的压强平衡常数
K时的压强平衡常数
___________ kPa(保留一位小数)。
Ⅲ.中国科学院大连化学物理研究所利用金属氧化物和分子筛的复合催化剂(OXZEO)实现了合成气(CO、)转化为低碳烯烃,反应过程如图所示:
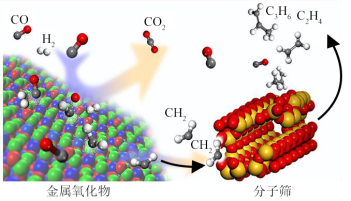
(4)该图显示,CO吸附到金属氧化物表面,碳氧键被“剪断”变成O原子和C原子, 与C原子反应形成烃类中间体,该烃类中间体的电子式为
与C原子反应形成烃类中间体,该烃类中间体的电子式为_____________ 。该中间体通过碳原子的链式增长,生成各种烯烃。该反应机理中,碳原子的链式增长的位置为___________ (填字母)。
A.金属氧化物表面 B.金属氧化物与分子筛之间的气体氛围中
C.分子筛表面 D.分子筛的孔道中
Ⅰ.我国科学家研究出新型催化剂
 /ZMS—5,能使
/ZMS—5,能使 加氢生成乙烯,反应过程如图所示:
加氢生成乙烯,反应过程如图所示:
(1)
 催化
催化 加氢的反应由反应①和反应②两步完成,反应①的活化能
加氢的反应由反应①和反应②两步完成,反应①的活化能 >反应②的活化能
>反应②的活化能 ,则
,则 催化
催化 加氢反应的决速步骤是
加氢反应的决速步骤是A.乙烯 B.2-甲基丙烯 C.2,3-二甲基-1-丁烯
Ⅱ.丙烯作为化工原料,其用量仅次于乙烯,应用丙烷脱氢制丙烯成为丙烯的重要来源,涉及的主要反应如下:
ⅰ.


ⅱ.


(2)


 。
。(3)按起始投料比
 将气体匀速通入到恒压(100kPa)密闭容器中,发生反应ⅰ和反应ⅱ。在相同时间不同温度(T)下,测得反应过程中
将气体匀速通入到恒压(100kPa)密闭容器中,发生反应ⅰ和反应ⅱ。在相同时间不同温度(T)下,测得反应过程中 、
、 的转化率变化曲线如图所示:
的转化率变化曲线如图所示:
M表示
 ”或“
”或“ ”)的转化率随温度变化的曲线;C点后,随着温度升高,主要进行的反应是
”)的转化率随温度变化的曲线;C点后,随着温度升高,主要进行的反应是 K时的压强平衡常数
K时的压强平衡常数
Ⅲ.中国科学院大连化学物理研究所利用金属氧化物和分子筛的复合催化剂(OXZEO)实现了合成气(CO、)转化为低碳烯烃,反应过程如图所示:

(4)该图显示,CO吸附到金属氧化物表面,碳氧键被“剪断”变成O原子和C原子,
 与C原子反应形成烃类中间体,该烃类中间体的电子式为
与C原子反应形成烃类中间体,该烃类中间体的电子式为A.金属氧化物表面 B.金属氧化物与分子筛之间的气体氛围中
C.分子筛表面 D.分子筛的孔道中
您最近一年使用:0次
解题方法
10 . 合成气(CO、 )可用于合成低碳烯烃和甲醇等化工产品。回答下列问题:
)可用于合成低碳烯烃和甲醇等化工产品。回答下列问题:
(1)用天然气制备合成气的原理如下:

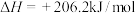
该反应的压强平衡常数(Kp)随温度的变化如下表:
温度/℃ | 700 | 750 | 800 | 850 | 900 |
|
|
| 1.00 | 5.23 |
|
根据热力学状态函数自由能(∆G)的数学表达式: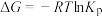 (R为大于0的常数,T为热力学温度),可以推知当温度超过
(R为大于0的常数,T为热力学温度),可以推知当温度超过
(2)用转炉熔渣(未冷却)制备合成气时,涉及反应如下:
Ⅰ.

Ⅱ.

Ⅲ.

反应温度与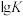 的关系如图所示。
的关系如图所示。
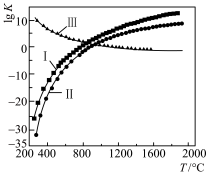
①
②反应: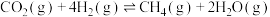 的
的
 、
、 表示)。
表示)。
③用转炉熔渣制取合成气的优点是
(3)在三个密闭容器中,按起始物质的量之比
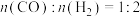 ,将CO和
,将CO和 充入容器中,在不同的温度和压强下,发生反应:
充入容器中,在不同的温度和压强下,发生反应: 。CO的转化率
。CO的转化率 与温度的关系如图所示:
与温度的关系如图所示: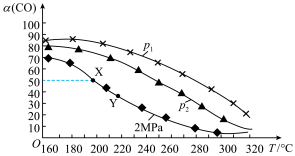
①
 (填“>”“<”或“=”);反应速率
(填“>”“<”或“=”);反应速率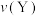
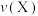 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②X点处,该反应的平衡常数为 (用平衡分压表示,分压等于总压乘以物质的量分数)。
(用平衡分压表示,分压等于总压乘以物质的量分数)。
③提高CO的转化率除改变温度和压强外还可采取的措施是
您最近一年使用:0次