1 . 为了探究碳酸钠、碳酸氢钠与盐酸反应是吸热反应还是放热反应。某化学兴趣小组同学进行了下列实验(每项实验各做三次平行实验,取平均值)。
(1)NaHCO3固体溶于水是_______ (填“吸热”“放热”)过程;NaHCO3溶液与盐酸反应是_______ (填“吸热”“放热”)反应。
(2)Na2CO3固体溶于水是_______ (填“吸热”“放热”)过程;Na2CO3溶液与盐酸反应是_______ (填“吸热”“放热”)反应。
(3)设计a、b组实验的目的是_______ 。
(4)判断CO (aq)+H+(aq)=HCO
(aq)+H+(aq)=HCO (aq) ∆H
(aq) ∆H_______ 0。
| 序号 | 试剂(35mL) | 固态物质及质量 | 混合前温度/℃ | 混合后温度/℃ |
| a | 水 | 2.5g NaHCO3 | 20.0 | 18.5 |
| b | 水 | 3.2g Na2CO3 | 20.0 | 24.3 |
| c | 盐酸 | 2.5g NaHCO3 | 20.0 | 16.2 |
| d | 盐酸 | 3.2g Na2CO3 | 20.0 | 25.1 |
(2)Na2CO3固体溶于水是
(3)设计a、b组实验的目的是
(4)判断CO
 (aq)+H+(aq)=HCO
(aq)+H+(aq)=HCO (aq) ∆H
(aq) ∆H
您最近一年使用:0次
名校
解题方法
2 . I.已知下列热化学方程式:
①P4(s,白磷)+5O2(g)=P4O10(s);△H1=-2983.2kJ/mol
②P(s,红磷)+ O2(g)=
O2(g)= P4O10(s);△H1=-738.5kJ/mol
P4O10(s);△H1=-738.5kJ/mol
③CO(g)=C(s)+ O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1
④C(s)+O2(g)=CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
(1)白磷的稳定性比红磷___________ (填“高”或“低”)
(2)表示CO燃烧热的热化学方程式为___________
II.一定条件下,在2L密闭容器中发生反应:3A(g)+B(s) 2C(g)。开始时加入4molA、6molB、2molC,在5min末测得C的物质的量是3mol。
2C(g)。开始时加入4molA、6molB、2molC,在5min末测得C的物质的量是3mol。
(1)用A的浓度变化表示反应的平均速率:___________ 。
(2)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①降低温度,化学反应速率___________ ;
②充入1molB,化学反应速率___________ ;
③将容器的体积变为1L,化学反应速率___________
①P4(s,白磷)+5O2(g)=P4O10(s);△H1=-2983.2kJ/mol
②P(s,红磷)+
 O2(g)=
O2(g)= P4O10(s);△H1=-738.5kJ/mol
P4O10(s);△H1=-738.5kJ/mol③CO(g)=C(s)+
 O2(g);△H=+110.5kJ•mol-1
O2(g);△H=+110.5kJ•mol-1④C(s)+O2(g)=CO2(g);△H=-393.5kJ•mol-1
回答下列问题:
(1)白磷的稳定性比红磷
(2)表示CO燃烧热的热化学方程式为
II.一定条件下,在2L密闭容器中发生反应:3A(g)+B(s)
 2C(g)。开始时加入4molA、6molB、2molC,在5min末测得C的物质的量是3mol。
2C(g)。开始时加入4molA、6molB、2molC,在5min末测得C的物质的量是3mol。(1)用A的浓度变化表示反应的平均速率:
(2)若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”):
①降低温度,化学反应速率
②充入1molB,化学反应速率
③将容器的体积变为1L,化学反应速率
您最近一年使用:0次
解题方法
3 . 不同价态含硫化合物的转化在工业上有重要的应用。回答下列问题:
(1)利用NO2将SO2转化为SO3的反应过程如下:
Ⅰ.SO2(g)+NO2(g)=SO3(g)+NO(g) ΔH=QkJ·mol-1
Ⅱ.2NO(g)+O2(g)=2NO2(g) ΔH= -114.1kJ·mol-1
反应2SO2(g)+O2(g)=2SO3(g) ΔH= -197.7kJ·mol-1。
则Q=_______ ;NO2的作用是_______ 。
(2)某化学小组对反应2SO2(g)+O2(g)⇌2SO3(g)进行研究。在一个容积为2L的恒温恒容密闭容器中,以不同投料方式研究上述反应,得到数据如下表:
①表中a=_______ ,甲组实验在该条件下的平衡常数K=_______ 。
②在相同条件下,若将甲组实验按2molSO2、1molO2、1molSO3进行投料,则反应开始时v正_______ v逆(填“>”“=”或“<”),平衡时SO3的百分含量与原甲组实验相比_______ (填“变大”“变小”或“不变”)。
③表中b=_______ ,若将乙组实验的容器改为绝热容器,则b值_______ (填“变大”“变小”或“不变”)。
(1)利用NO2将SO2转化为SO3的反应过程如下:
Ⅰ.SO2(g)+NO2(g)=SO3(g)+NO(g) ΔH=QkJ·mol-1
Ⅱ.2NO(g)+O2(g)=2NO2(g) ΔH= -114.1kJ·mol-1
反应2SO2(g)+O2(g)=2SO3(g) ΔH= -197.7kJ·mol-1。
则Q=
(2)某化学小组对反应2SO2(g)+O2(g)⇌2SO3(g)进行研究。在一个容积为2L的恒温恒容密闭容器中,以不同投料方式研究上述反应,得到数据如下表:
| 实验分组 | 甲组 | 乙组 |
| 反应物 | 2molSO2、1molO2 | 2molSO3 |
| 反应热量 | 放热158.16kJ | |
| 反应物的平衡转化率 | a | b |
①表中a=
②在相同条件下,若将甲组实验按2molSO2、1molO2、1molSO3进行投料,则反应开始时v正
③表中b=
您最近一年使用:0次
名校
4 . 反应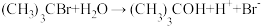
 分两步进行,反应如下:
分两步进行,反应如下:
第一步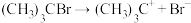 (慢反应)
(慢反应) 
第二步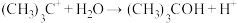 (快反应)
(快反应)
该反应的能量与反应历程图象正确的是
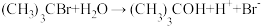
 分两步进行,反应如下:
分两步进行,反应如下:第一步
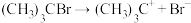 (慢反应)
(慢反应) 
第二步
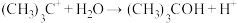 (快反应)
(快反应)该反应的能量与反应历程图象正确的是
A.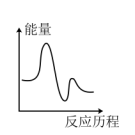 | B.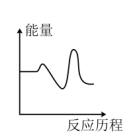 |
C.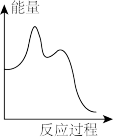 | D.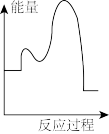 |
您最近一年使用:0次
2021-05-20更新
|
796次组卷
|
11卷引用:云南省保山市腾冲市第八中学2020-2021学年高一下学期期末考试化学试题
云南省保山市腾冲市第八中学2020-2021学年高一下学期期末考试化学试题湖南省永州市省重点中学2021届高三5月联考化学试题河北省沧州市2021届高考第二次模拟考试化学试题辽宁省朝阳市2021届高三第四次模拟考试化学试题山西省2020-2021学年高二下学期5月考试化学试题河南省南阳地区2020-2021学年高二下学期阶段检测考试化学试题湖南省重点中学2020-2021学年高二下学期5月份联合考试化学试题(已下线)1.3 化学反应热的计算-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第一章 化学反应与能量 单元综合检测-2021-2022学年高二化学课后培优练(人教版选修4)湖南省长沙市长郡梅溪湖中学2022-2023学年高二上学期第三次月考化学试题广东省深圳外国语学校2022-2023学年高二上学期期末考试化学试题
名校
解题方法
5 . 氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。回答下列问题:
(1)汽车尾气中常含有碳烟、CO、NO等有害物质,尾气中含有碳烟的主要原因为______ 。
(2)已知在298 K和101 kPa条件下,有如下反应:反应①:C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol
反应②:N2(g)+O2(g)=2NO(g) ΔH2=+180.5kJ·mol
若反应 CO2(g)+
CO2(g)+ N2(g)⇌
N2(g)⇌ C(s)+NO(g)的活化能为a kJ·mol
C(s)+NO(g)的活化能为a kJ·mol ,则反应C(s)+2NO(g)⇌CO2(g)+N2(g)的活化能为
,则反应C(s)+2NO(g)⇌CO2(g)+N2(g)的活化能为____ kJ·mol
(3)在常压下,已知反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g) ΔH(298 K)= -113.0 kJ·mol ,ΔS(298 K)= -145.3×10-3kJ/(mol·K) ,据此可判断该反应在常温下
,ΔS(298 K)= -145.3×10-3kJ/(mol·K) ,据此可判断该反应在常温下___ (填“能”或“不能”)自发进行。
(4)向容积为2L的真空密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)⇌ N2 (g)+CO2(g),NO和N2的物质的量变化如下表所示,在T1℃、T2℃分别到达平衡时容器的总压强分别为p1 kPa、p2 kPa。
①0~10min内,以NO表示的该反应速率v(NO)=_____ kPa·min-1。
②第15 min后,温度调整到T2,数据变化如上表所示,则p1____ p2(填“>”、“<”或“=”)。
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,再次达平衡时NO的体积百分含量为________ 。
(1)汽车尾气中常含有碳烟、CO、NO等有害物质,尾气中含有碳烟的主要原因为
(2)已知在298 K和101 kPa条件下,有如下反应:反应①:C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol

反应②:N2(g)+O2(g)=2NO(g) ΔH2=+180.5kJ·mol

若反应
 CO2(g)+
CO2(g)+ N2(g)⇌
N2(g)⇌ C(s)+NO(g)的活化能为a kJ·mol
C(s)+NO(g)的活化能为a kJ·mol ,则反应C(s)+2NO(g)⇌CO2(g)+N2(g)的活化能为
,则反应C(s)+2NO(g)⇌CO2(g)+N2(g)的活化能为
(3)在常压下,已知反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g) ΔH(298 K)= -113.0 kJ·mol
 ,ΔS(298 K)= -145.3×10-3kJ/(mol·K) ,据此可判断该反应在常温下
,ΔS(298 K)= -145.3×10-3kJ/(mol·K) ,据此可判断该反应在常温下(4)向容积为2L的真空密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)⇌ N2 (g)+CO2(g),NO和N2的物质的量变化如下表所示,在T1℃、T2℃分别到达平衡时容器的总压强分别为p1 kPa、p2 kPa。
| 物质的量/mol | T1℃ | T2℃ | |||||
| 0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min | |
| NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
| N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
①0~10min内,以NO表示的该反应速率v(NO)=
②第15 min后,温度调整到T2,数据变化如上表所示,则p1
③若30min时,保持T2不变,向该容器中再加入该四种反应混合物各2 mol,再次达平衡时NO的体积百分含量为
您最近一年使用:0次
名校
6 . (1)在高温、高压、催化剂作用下,1mol石墨转化为金刚石,吸收1.9 kJ的热量。该反应的ΔH ___________ 0 (填“>”或“<”),对于石墨和金刚石,___________ 更稳定。
(2)用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应反应热的测定实验。回答下列问题:
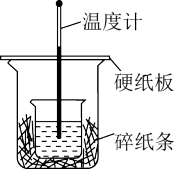
①从实验装置上看,图中尚缺少的一种玻璃用品是___________ 。
②大烧杯上如不盖硬纸板,测得的反应热数值___________ (填“偏大、偏小、无影响”)。
③用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的反应热的数值会___________ (填“偏大”、“偏小”、“无影响”)。
(3)在25℃、101 kPa下,1g CH3OH(l)完全燃烧生成CO2和液态水时放热22.68 kJ。写出表示CH3OH燃烧热的热化学方程式___________ 。
(4)已知几种化学键的键能如表所示:
则反应Cl2(g)+ 3F2(g) 2ClF3(g) 的ΔH =
2ClF3(g) 的ΔH =___________ kJ/mol
(5)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) =2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:___________ 。
(2)用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应反应热的测定实验。回答下列问题:

①从实验装置上看,图中尚缺少的一种玻璃用品是
②大烧杯上如不盖硬纸板,测得的反应热数值
③用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的反应热的数值会
(3)在25℃、101 kPa下,1g CH3OH(l)完全燃烧生成CO2和液态水时放热22.68 kJ。写出表示CH3OH燃烧热的热化学方程式
(4)已知几种化学键的键能如表所示:
| 化学键 | Cl—Cl | F—F | Cl—F |
| 键能/ (kJ/mol) | 242 | 159 | 172 |
则反应Cl2(g)+ 3F2(g)
 2ClF3(g) 的ΔH =
2ClF3(g) 的ΔH =(5)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) =2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:
您最近一年使用:0次
解题方法
7 . 联氨( )是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料。回答下列问题:
)是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料。回答下列问题:
(1)工业上利用 和
和 合成
合成 ,用
,用 进一步制备联氨
进一步制备联氨 。
。
①已知断开(或形成) 键、
键、 键分别需要吸收(或放出)
键分别需要吸收(或放出)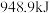 ,
, 的热量,合成
的热量,合成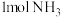 可放出
可放出 的热量,则形成
的热量,则形成 放出的热量为
放出的热量为___________  (保留一位小数)。
(保留一位小数)。
②工业上一种制备联氨的方法为 。该反应涉及物质中属于离子化合物的是
。该反应涉及物质中属于离子化合物的是___________ (填写化学式)。制备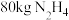 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为___________  。
。
(2)发射航天器时常以 为燃料,
为燃料, 为推进剂。
为推进剂。
已知
ⅰ. 的摩尔燃烧焓为
的摩尔燃烧焓为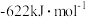 。
。
ⅱ. 与
与 反应的物质和能量变化示意图如下:
反应的物质和能量变化示意图如下:
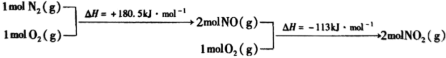
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
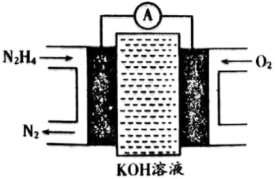
(3)一种联氨燃料电池的工作原理如图所示。放电一段时间,电解质溶液中 的物质的量浓度
的物质的量浓度___________ (填“增大”“减小”或“不变”),负极反应式为___________ 。
 )是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料。回答下列问题:
)是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料。回答下列问题:(1)工业上利用
 和
和 合成
合成 ,用
,用 进一步制备联氨
进一步制备联氨 。
。①已知断开(或形成)
 键、
键、 键分别需要吸收(或放出)
键分别需要吸收(或放出)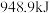 ,
, 的热量,合成
的热量,合成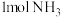 可放出
可放出 的热量,则形成
的热量,则形成 放出的热量为
放出的热量为 (保留一位小数)。
(保留一位小数)。②工业上一种制备联氨的方法为
 。该反应涉及物质中属于离子化合物的是
。该反应涉及物质中属于离子化合物的是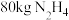 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为 。
。(2)发射航天器时常以
 为燃料,
为燃料, 为推进剂。
为推进剂。已知
ⅰ.
 的摩尔燃烧焓为
的摩尔燃烧焓为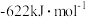 。
。ⅱ.
 与
与 反应的物质和能量变化示意图如下:
反应的物质和能量变化示意图如下: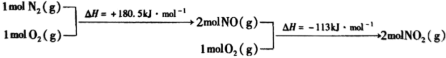
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(3)一种联氨燃料电池的工作原理如图所示。放电一段时间,电解质溶液中
 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
8 . 目前,汽车尾气系统中均安装了催化转化器,大大减少了CO和NOx汽车尾气的排放。
(1)在催化剂作用下CO还原NO、NO2。
标准摩尔生成焓是指由稳态单质生成1mol该化合物的焓变,25℃下几种物质的标准生成焓如下:
ⅰ.CO(g)+NO2(g) CO2(g)+NO(g) ΔH1
CO2(g)+NO(g) ΔH1
ⅱ.2CO(g)+2NO(g) 2CO2(g)+N2(g) ΔH2=-623KJ• mol-1
2CO2(g)+N2(g) ΔH2=-623KJ• mol-1
ΔH1=___________ ;写出用 CO还原NO2生成两种无污染的气态物质总反应的热化学方程式:___________
人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(2)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为:___________ 。
(3)一种以 CO为燃料,以空气为氧化剂,以熔融态 K2CO3为电解质的燃料电池,工作原理如下图所示:
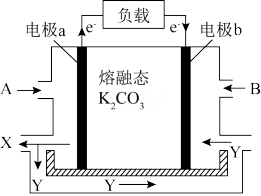
①电极a为___________ (填“ 正极”或“ 负极” ),Y物质为___________ ;
②正极上的电极反应式为___________ 。
(1)在催化剂作用下CO还原NO、NO2。
标准摩尔生成焓是指由稳态单质生成1mol该化合物的焓变,25℃下几种物质的标准生成焓如下:
| NO2 | CO | CO2 | NO | |
| 标准生成焓/kJ•mol-1 | 33.1 | -110.5 | -183.6 | 90.3 |
 CO2(g)+NO(g) ΔH1
CO2(g)+NO(g) ΔH1ⅱ.2CO(g)+2NO(g)
 2CO2(g)+N2(g) ΔH2=-623KJ• mol-1
2CO2(g)+N2(g) ΔH2=-623KJ• mol-1ΔH1=
人们应用原电池原理制作了多种电池,以满足不同的需要。请根据题中提供的信息,填写空格。
(2)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为:
(3)一种以 CO为燃料,以空气为氧化剂,以熔融态 K2CO3为电解质的燃料电池,工作原理如下图所示:

①电极a为
②正极上的电极反应式为
您最近一年使用:0次
名校
解题方法
9 . 已知:CH3OH(g)+ O2(g)=CO2(g)+2H2O(g)△H=akJ·mol﹣1、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=bkJ·mol﹣1,则下列叙述正确的是
O2(g)=CO2(g)+2H2O(g)△H=akJ·mol﹣1、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=bkJ·mol﹣1,则下列叙述正确的是
 O2(g)=CO2(g)+2H2O(g)△H=akJ·mol﹣1、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=bkJ·mol﹣1,则下列叙述正确的是
O2(g)=CO2(g)+2H2O(g)△H=akJ·mol﹣1、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=bkJ·mol﹣1,则下列叙述正确的是| A.C﹣H键键长小于H﹣H键 |
| B.CH4(g)+2O2=CO2(g)+2H2O(g)△H=bkJ·mol﹣1表示甲烷燃烧热的热化学方程式 |
| C.2CH3OH(g)=2CH4(g)+O2(g)△H=2(a﹣b)kJ·mol﹣1 |
D.当CH3OH(g)和CH4(g)物质的量之比为1:2时,其完全燃烧生成CO2和H2O(g)时,放出的热量为ckJ,则该混合物中CH3OH(g)的物质的量为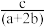 mol mol |
您最近一年使用:0次
10 . 物质的摩尔燃烧焓是指在一定温度和压强条件下,1mol物质完全氧化为同温下的指定产物时的焓变,其中物质中所含的N元素氧化为N2(g)、H元素氧化为H2O(l)、C元素氧化为CO2(g)。
已知:①几种物质的摩尔燃烧焓:
②298k,101kPa时,部分化学键键能:
③H2O(l)=H2O(g) △H=+44.0kJ/mol
回答下列问题:
(1)计算反应2CO(g)+O2(g)=2CO2(g)的焓变△H1=___________ kJ·mol-1,由此可求CO的化学键C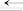 O键能a=
O键能a=___________ kJ·mol-1。
(2)已知相同条件下,石墨比金刚石稳定,则1mol金刚石的燃烧放热___________ 393.5kJ(填“>”、“<”、“=”)。
(3)写出常温下氢气燃烧的热化学方程式___________ ,则反应CO(g)+H2O(g)=CO2(g)+H2(g)的焓变△H2=___________ kJ·mol-1。
已知:①几种物质的摩尔燃烧焓:
| 物质 | 石墨(s) | H2(g) | CO(g) |
| △H/(kJ·mol—1) | -393.5 | -285.8 | -283.0 |
②298k,101kPa时,部分化学键键能:
| 化学键 | C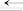 O O | O=O | C=O | C-O |
| E/(kJ·mol-1) | a | 498 | 745 | 351 |
③H2O(l)=H2O(g) △H=+44.0kJ/mol
回答下列问题:
(1)计算反应2CO(g)+O2(g)=2CO2(g)的焓变△H1=
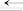 O键能a=
O键能a=(2)已知相同条件下,石墨比金刚石稳定,则1mol金刚石的燃烧放热
(3)写出常温下氢气燃烧的热化学方程式
您最近一年使用:0次



