1 . 现有反应:
A.CaCO3 CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑
CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑
C.C+CO2 2CO D.2KOH+H2SO4=K2SO4+2H2O
2CO D.2KOH+H2SO4=K2SO4+2H2O
(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合如图的是_______ (填反应序号)。
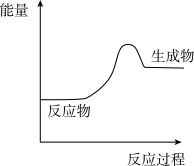
(2)在常温下,上述四个反应中可用于设计原电池的是_______ (填反应序号),根据该原电池回答下列问题:
①负极发生_______ (填“氧化”或“还原”)反应;正极的电极反应式为_______ 。
②当导线中有1 mol电子通过时,理论上发生的变化是_______ (填序号)。
a.溶液增重32.5 g b.溶液增重31.5 g c.析出1g H2 d.析出11.2LH2
(3)对于反应B,将足量且等量的形状相同的锌块分别加入到等浓度等体积的两份稀硫酸X、Y中,同时向X中加入少量饱和CuSO4溶液,发生反应生成氢气的体积(V)与时间(t)的关系如图所示。
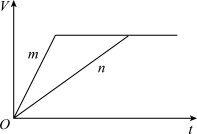
反应速率变快的原因是_______(填序号)。
A.CaCO3
 CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑
CaO+CO2↑ B.Zn+H2SO4=ZnSO4+H2↑C.C+CO2
 2CO D.2KOH+H2SO4=K2SO4+2H2O
2CO D.2KOH+H2SO4=K2SO4+2H2O(1)上述四个反应中属于氧化还原反应且反应过程中能量变化符合如图的是

(2)在常温下,上述四个反应中可用于设计原电池的是
①负极发生
②当导线中有1 mol电子通过时,理论上发生的变化是
a.溶液增重32.5 g b.溶液增重31.5 g c.析出1g H2 d.析出11.2LH2
(3)对于反应B,将足量且等量的形状相同的锌块分别加入到等浓度等体积的两份稀硫酸X、Y中,同时向X中加入少量饱和CuSO4溶液,发生反应生成氢气的体积(V)与时间(t)的关系如图所示。

反应速率变快的原因是_______(填序号)。
| A.CuSO4作催化剂 |
B.加入硫酸铜溶液增大了c( ) ) |
| C.Zn首先与Cu2+反应,生成的Cu与Zn、稀硫酸构成原电池 |
| D.加入硫酸铜溶液增大了溶液体积 |
您最近一年使用:0次
2 . 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
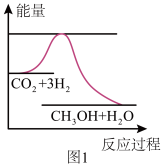
(1)该反应是___________ (填“吸热”或“放热”)反应。
(2)温度升高,CO2的转化率___________ (填“增大”、“不变”或“减小”)。
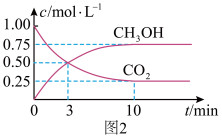
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率v(H2)为___________ mol·L-1·min-1,CO2和H2的转化率比是___________
(4)下列措施中能使(3)题中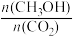 增大的有
增大的有___________ 。(填字母)
A.升高温度
B.加入催化剂
C.将H2O(g)从体系中分离
D.充入He(g),使体系总压强增大
E.再充入1molCO2和3molH2
 CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。
(1)该反应是
(2)温度升高,CO2的转化率
(3)为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。从反应开始到平衡,用H2浓度变化表示的平均反应速率v(H2)为

(4)下列措施中能使(3)题中
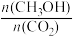 增大的有
增大的有A.升高温度
B.加入催化剂
C.将H2O(g)从体系中分离
D.充入He(g),使体系总压强增大
E.再充入1molCO2和3molH2
您最近一年使用:0次
名校
解题方法
3 . 已知2SO2+O2 2SO3为放热反应,对该反应的下列说法中正确的是
2SO3为放热反应,对该反应的下列说法中正确的是
 2SO3为放热反应,对该反应的下列说法中正确的是
2SO3为放热反应,对该反应的下列说法中正确的是| A.O2的能量一定高于SO2的能量 |
| B.SO2和O2的总能量一定高于SO3的总能量 |
| C.SO2的能量一定高于SO3的能量 |
| D.因该反应为放热反应,故不必加热就可发生 |
您最近一年使用:0次
2022-12-21更新
|
255次组卷
|
2卷引用:广西贺州市钟山县钟山中学2020-2021学年高一下学期第二次月考理科化学试题
12-13高一·新疆乌鲁木齐·期中
名校
解题方法
4 . 下列反应既属于氧化还原反应,又属于吸热反应的是
| A.铝片与稀盐酸的反应 | B.Ba(OH)2·8H2O与NH4Cl的反应 |
| C.灼热的碳与CO2的反应 | D.甲烷在氧气中的燃烧 |
您最近一年使用:0次
2022-12-21更新
|
563次组卷
|
17卷引用:【浙江新东方】【2021.4.27】【宁波】【高二上】【高中化学】【00135】
(已下线)【浙江新东方】【2021.4.27】【宁波】【高二上】【高中化学】【00135】广西贺州市钟山县钟山中学2020-2021学年高一下学期第一次月考理科化学试题(已下线)2012-2013学年新疆乌鲁木齐一中高一(特长班)下期中考试化学卷(已下线)2013届新疆乌鲁木齐市一中高一下学期特长班期中考试化学试卷吉林省松原市前郭尔罗斯蒙古族自治县蒙古族中学2019-2020学年高一下学期网课检测化学试题湖南省郴州市永兴县童星学校2022-2023学年高二上学期9月月考化学试题广东省汕尾华大实验学校2022-2023学年高二上学期12月月考化学试题福建省福州第三中学2022-2023学年高一下学期期中考试化学试题福建省福州重点中学2022-2023学年高一下学期期中考试化学试题广东省揭阳市普宁市勤建学校2022-2023学年高二上学期期中考试化学试题作业(一) 化学反应的反应热第一章 化学反应的热效应 第一节 反应热 第1课时 反应热 焓变浙江省绍兴市稽山中学2022-2023学年高一下学期期中检测化学试题黑龙江省佳木斯市三校联考2023-2024学年高三上学期第三次调研考试化学试题广东省茂名市化州市第一中学2023-2024学年高二上学期期中测评化学试题 广东实验中学越秀学校2023-2024学年高二上学期期中考试化学试题浙江省杭州第十一中学2023-2024学年高二上学期期末考试化学试题
解题方法
5 . 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。
(1)①工业合成氨反应:N2+3H2 2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量
2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量_______ (填“大于”、“小于”或“等于”)920kJ。
②已知拆开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为_______ 。
(2)某实验小组同学进行如图1所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度_______ (填“升高”或“降低”)。反应过程_______ (填“①”或“②”)的能量变化可用图2表示。
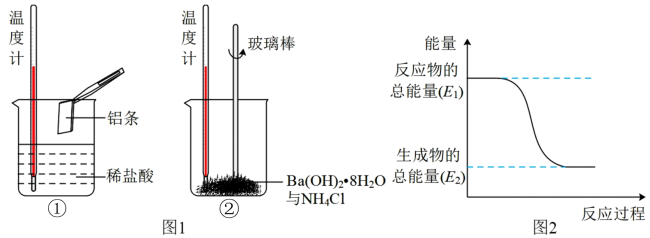
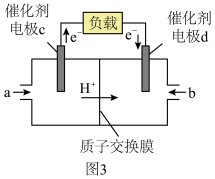
(3)用CH3OH和O2组合形成的质子交换膜燃料电池的结构如图3所示,则d电极是_______ (填“正极”或“负极”),d电极的电极反应式为_______ 。
(1)①工业合成氨反应:N2+3H2
 2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量
2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN2完全反应生成NH3可放出92kJ热量。如果将10molN2和足量H2混合,使其充分反应,放出的热量②已知拆开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为
(2)某实验小组同学进行如图1所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度

(3)用CH3OH和O2组合形成的质子交换膜燃料电池的结构如图3所示,则d电极是

您最近一年使用:0次
名校
解题方法
6 . 我国科学家研究化合物M(s)催化CO2氢化机理。由化合物M(s)生成化合物N(s)过程的机理和相对能量曲线如图所示(已知1eV=1.6×10−19J)。TS1、TS2均为过渡态。下列说法错误的是
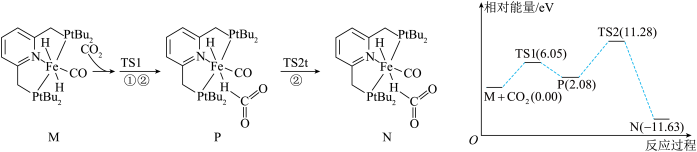

| A.过渡态TS1比TS2更稳定 |
| B.过程P→TS2为化合物M生成化合物N的决速步骤 |
| C.化合物M催化CO2氢化反应过程中一定有Fe−O键的断裂 |
| D.该过程的热化学方程式为:M(s)+CO2(g)=N(s) ΔH=−11.63 kJ·mol −1 |
您最近一年使用:0次
2022-12-21更新
|
369次组卷
|
5卷引用:湖北省宜昌英杰学校2021-2022学年高三上学期9月月考化学试题
解题方法
7 . 利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:CO2+H2O CO+H2+O2
CO+H2+O2
已知:
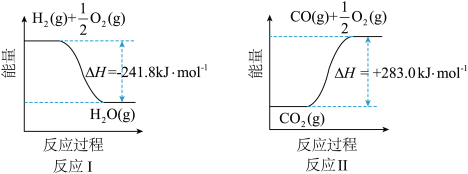
(1)反应Ⅱ是___________ 反应(填“吸热”或“放热”),其原因是___________ 。
(2)反应A的热化学方程式是___________ 。反应A的平衡常数表达式为___________ 。
反应A:CO2+H2O
 CO+H2+O2
CO+H2+O2已知:

(1)反应Ⅱ是
(2)反应A的热化学方程式是
您最近一年使用:0次
8 . 已知化学反应A2(g)+B2(g) 2AB(l)的能量变化如图所示,判断下列叙述中正确的是
2AB(l)的能量变化如图所示,判断下列叙述中正确的是
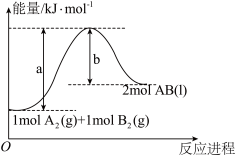
 2AB(l)的能量变化如图所示,判断下列叙述中正确的是
2AB(l)的能量变化如图所示,判断下列叙述中正确的是
| A.每生成2mol气态AB放出bkJ热量 |
| B.向密闭容器中充入1molA2和1molB2充分反应,吸收的热量为(a-b)kJ |
| C.向密闭容器中充入一定量的A2和B2,、生成2molAB(g)吸收的热量小于(a-b)kJ |
| D.AB(l)分解为A2(g)和B2(g)的反应为放热反应 |
您最近一年使用:0次
2022-12-20更新
|
245次组卷
|
3卷引用:四川省成都东部新区养马中学2020-2021学年高一下学期期中考试化学试题
9 . 如图是CH4与Zr形成过渡金属化合物的过程。下列说法不正确的是
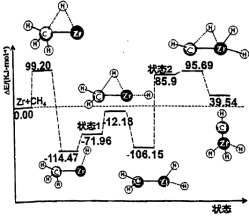

| A.1molCH2-Zr…H2 转化成CH-Zr…H3需要吸收145.69kJ能量 |
B.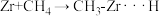 活化能为 活化能为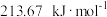 |
C.在中间产物中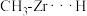 状态最稳定 状态最稳定 |
D.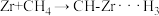 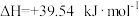 |
您最近一年使用:0次
10 . 铋基催化剂对CO2电化学还原制取HCOOH具有高效选择性。其反应历程与能量变化如图:
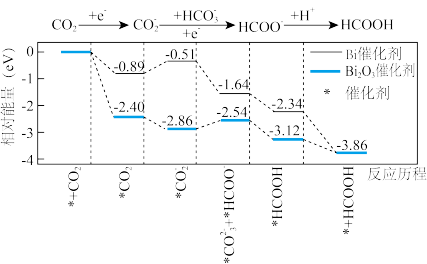
下列说法错误的是

下列说法错误的是
| A.使用Bi2O3催化剂更有利于CO2的吸附 |
| B.使用不同铋基催化剂,最大能垒(活化能)不相等 |
| C.CO2电化学还原制取HCOOH的反应△H<0 |
D.*CO 生成*HCOO-的反应为:*CO 生成*HCOO-的反应为:*CO +HCO +HCO =*CO =*CO +*HCOO- +*HCOO- |
您最近一年使用:0次



