名校
解题方法
1 . 化学反应中的能量变化,通常表现为热量的变化,研究化学反应中的热量变化具有重要的意义。
(1)下列变化属于吸热反应的是_______ (填序号)。
①液态水气化②胆矾加热变成白色粉末③浓硫酸稀释④氢气还原氧化铜⑤盐酸和碳酸氢钠反应⑥氢氧化钾和稀硫酸反应⑦灼热的木炭与CO2的反应⑧Ba(OH)2•8H2O晶体与NH4Cl晶体的反应⑨甲烷在空气中燃烧的反应
(2)已知:C(s)+O2(g)=CO(g) ΔH1 C(g)+O2(g)=CO2(g) ΔH2
则ΔH1_______ ΔH2(填“>”、“<”或“=”)。
(3)已知:2SO2(g)+O2(g)⇌2SO3(g) ΔH=-196.6kJ·mol-1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量_______(填字母)。
(4)在25℃、101kPa下,23g乙醇CH3CH2OH(l)完全燃烧生成CO2和液态水时放热638.4kJ。则表示乙醇燃烧的热化学方程式为_______ 。
(5)50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。

①图中缺少的一种玻璃仪器是_______ 。
②若用相同浓度和体积的醋酸代替盐酸进行上述实验,测得的中和反应ΔH将_______ (填“偏大”、“偏小”或“无影响”)。
(1)下列变化属于吸热反应的是
①液态水气化②胆矾加热变成白色粉末③浓硫酸稀释④氢气还原氧化铜⑤盐酸和碳酸氢钠反应⑥氢氧化钾和稀硫酸反应⑦灼热的木炭与CO2的反应⑧Ba(OH)2•8H2O晶体与NH4Cl晶体的反应⑨甲烷在空气中燃烧的反应
(2)已知:C(s)+O2(g)=CO(g) ΔH1 C(g)+O2(g)=CO2(g) ΔH2
则ΔH1
(3)已知:2SO2(g)+O2(g)⇌2SO3(g) ΔH=-196.6kJ·mol-1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量_______(填字母)。
| A.等于196.6kJ | B.98.3kJ~196.6kJ | C.等于98.3kJ | D.小于98.3kJ |
(5)50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。

①图中缺少的一种玻璃仪器是
②若用相同浓度和体积的醋酸代替盐酸进行上述实验,测得的中和反应ΔH将
您最近半年使用:0次
2 . 下列说法正确的是
A.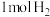 完全燃烧生成 完全燃烧生成 放出的热量叫 放出的热量叫 的燃烧热 的燃烧热 |
B.25℃、 时,已知碳的燃烧热为 时,已知碳的燃烧热为 ,则碳的热值也为 ,则碳的热值也为 |
C.已知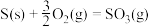  ,则硫生成SO3的反应热为 ,则硫生成SO3的反应热为 |
D.25℃、 时, 时,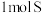 和 和 的燃烧热相等 的燃烧热相等 |
您最近半年使用:0次
解题方法
3 . 下列关于中和反应反应热和燃烧热的描述中,正确的是
| A.25℃,101kPa时,H2SO4和Ca(OH)2反应生成1mol水放出的热量与HCl和NaOH反应生成1mol水放出的热量一定相等 |
| B.中和反应反应热的测定过程中,若隔热层隔热效果不好,会导致所测数值的绝对值偏小 |
| C.根据热化学方程式N2H4(l)+3O2(g)=2NO2(g)+2H2O(l) △H=-622kJ•mol-1,可求得N2H4(l)的燃烧热 |
| D.1gH2完全燃烧生成液态水时放出的热量即为H2的燃烧热 |
您最近半年使用:0次
2022-12-17更新
|
256次组卷
|
2卷引用:广东部分名校2022-2023学年高二上学期12月联考化学试题
名校
4 . 北京奥运会“祥云”奥运火炬所用环保型燃料为丙烷( ),悉尼奥运会所用火炬燃料为65%丁烷(
),悉尼奥运会所用火炬燃料为65%丁烷( )和
)和 丙烷。
丙烷。
已知: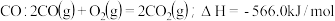 。
。
丙烷: 。
。
正丁烷: 。
。
异丁烷: 。
。
下列有关说法正确的是
 ),悉尼奥运会所用火炬燃料为65%丁烷(
),悉尼奥运会所用火炬燃料为65%丁烷( )和
)和 丙烷。
丙烷。已知:
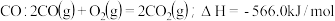 。
。丙烷:
 。
。正丁烷:
 。
。异丁烷:
 。
。下列有关说法正确的是
A.常温下,正丁烷的燃烧热为 |
| B.相同质量的丙烷和正丁烷分别完全燃烧,前者需要的氧气少产生的热量也多 |
C.常温下, 的燃烧热为 的燃烧热为 |
| D.人类利用的能源都是通过化学反应获得的 |
您最近半年使用:0次
5 . 已知碳酸钙分解的热化学方程式为:
 ,欲使1t
,欲使1t 完全分解,需要提供多少热
完全分解,需要提供多少热_______ ?若通过煤炭燃烧来提供热,则至少需要燃烧____ 千克煤炭?(已知煤炭的热值为 )
)

 ,欲使1t
,欲使1t 完全分解,需要提供多少热
完全分解,需要提供多少热 )
)
您最近半年使用:0次
6 . 乙炔( )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
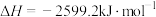 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热__________ ?

 )气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
)气体在氧气中完全燃烧放出大量热,形成高温火焰(氧炔焰),可以用于焊接或切割钢板。已知乙炔在氧气中完全燃烧的热化学方程式是:
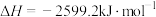 。则1kg乙炔在氧气中完全燃烧放出多少热
。则1kg乙炔在氧气中完全燃烧放出多少热
您最近半年使用:0次
7 . 已知:CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H1=-akJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H2=-bkJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(1) △H3=-ckJ·mol-1
则下列叙述正确的是
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H2=-bkJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(1) △H3=-ckJ·mol-1
则下列叙述正确的是
| A.由上述热化学方程式可知△H2<△H3 |
| B.甲烷的燃烧热为bkJ·mol-l |
| C. 2CH3OH(g)=2CH4(g)+O2(g) △H=2(b-a)kJ/mol-1 |
| D.当甲醇和甲烷物质的量之比为1:2时,其完全燃烧生成CO2和H2O(l)时,放出的热量为QkJ,则该混合物中甲醇的物质的量为Q/(a+2b)mol |
您最近半年使用:0次
2022-11-22更新
|
202次组卷
|
2卷引用:四川省成都外国语学校2022-2023学年高二上学期期中考试化学试题
名校
解题方法
8 . 化学反应与能量
(1)已知



设有氢气和丙烷的混合气体5mol,完全燃烧时放出热量为3847kJ,则混合气体中氢气与丙烷的体积比是_______ 。
(2)甲醇( )广泛用作燃料电池的燃料,可由天然气来合成,已知:
)广泛用作燃料电池的燃料,可由天然气来合成,已知:
①

②
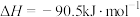
③
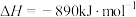
则甲醇的燃烧热为_______ 。
(3)向足量的 溶液中加入100mL
溶液中加入100mL 的
的 溶液,放出的热量是5.12kJ。向足量的
溶液,放出的热量是5.12kJ。向足量的 溶液中加入100mL
溶液中加入100mL 的
的 溶液,放出的热量为2.2kJ。则
溶液,放出的热量为2.2kJ。则 溶液与
溶液与 溶液反应的热化学方程式为
溶液反应的热化学方程式为


_______ 。
(4)已知:
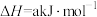

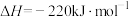
 、
、 和
和 键的键能分别为436、496和
键的键能分别为436、496和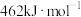 ,则a为
,则a为_______ 。
(1)已知




设有氢气和丙烷的混合气体5mol,完全燃烧时放出热量为3847kJ,则混合气体中氢气与丙烷的体积比是
(2)甲醇(
 )广泛用作燃料电池的燃料,可由天然气来合成,已知:
)广泛用作燃料电池的燃料,可由天然气来合成,已知:①


②

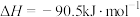
③

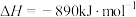
则甲醇的燃烧热为
(3)向足量的
 溶液中加入100mL
溶液中加入100mL 的
的 溶液,放出的热量是5.12kJ。向足量的
溶液,放出的热量是5.12kJ。向足量的 溶液中加入100mL
溶液中加入100mL 的
的 溶液,放出的热量为2.2kJ。则
溶液,放出的热量为2.2kJ。则 溶液与
溶液与 溶液反应的热化学方程式为
溶液反应的热化学方程式为

(4)已知:

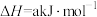

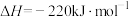
 、
、 和
和 键的键能分别为436、496和
键的键能分别为436、496和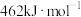 ,则a为
,则a为
您最近半年使用:0次
9 . 完成下列问题
(1)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液测定计算中和反应的反应热。
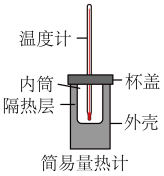
回答下列问题:
①从实验装置上看,图中缺少的一种玻璃用品是_______ 。
②如改用0.0275molNaOH固体与该盐酸进行实验,则实验中测得的“中和热”数值将_______ (填“偏大”、“偏小”或“无影响”)。
(2)反应mA(g)+nB(g) pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
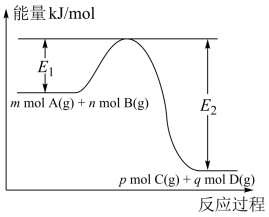
①该反应ΔH=_______ (用含E1、E2式子表示);
②在反应体系中加入催化剂,E1_______ (填“增大”、“减小”、“不变”),ΔH_______ (填“增大”、“减小”、“不变”)。
(3)依据事实,写出下列反应的热化学方程式:
①4g硫粉在O2中完全燃烧生成SO2气体,放出37kJ热量,写出表示硫燃烧热的热化学方程式为:_______ 。
②25℃101kPa时,氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化为液态水,放出2.444kJ的热量。请写出氢气和氧气反应生成1mol液态水时的热化方程式为:_______ 。
(4)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:①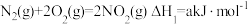
②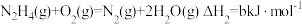
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:_______ 。
(1)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液测定计算中和反应的反应热。

回答下列问题:
①从实验装置上看,图中缺少的一种玻璃用品是
②如改用0.0275molNaOH固体与该盐酸进行实验,则实验中测得的“中和热”数值将
(2)反应mA(g)+nB(g)
 pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
pC(g)+qD(g)过程中的能量变化如图,回答下列问题。
①该反应ΔH=
②在反应体系中加入催化剂,E1
(3)依据事实,写出下列反应的热化学方程式:
①4g硫粉在O2中完全燃烧生成SO2气体,放出37kJ热量,写出表示硫燃烧热的热化学方程式为:
②25℃101kPa时,氢气和氧气反应生成1mol水蒸气放热241.8kJ,若1g水蒸气转化为液态水,放出2.444kJ的热量。请写出氢气和氧气反应生成1mol液态水时的热化方程式为:
(4)发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。
已知:①
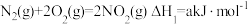
②
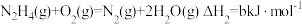
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:
您最近半年使用:0次