①
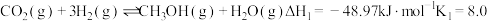
②

③
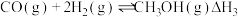
(1)反应③活化能
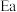 (正)
(正)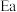 (逆)(填“>”、“<”或“=”),该反应在
(逆)(填“>”、“<”或“=”),该反应在(2)当只发生以上反应时,单位时间内反应物投料与
 转化率、
转化率、 产率之间关系如下表:
产率之间关系如下表: |  |  |  | 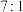 |
 转化率% 转化率% | 11.6 | 13.7 | 15.9 | 18.7 |
 产率% 产率% | 3.0 | 4.1 | 5.3 | 6.9 |
A.2∶1 B.3∶1 C.5∶1 D.7∶1
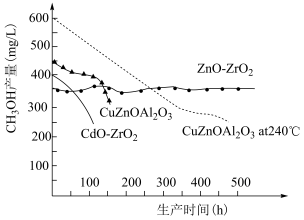
(3)工业生产对催化剂进行选择的时候,除了要考虑催化剂的效率以外,催化剂的稳定性也是很重要的参考条件,一般工业生产所用催化剂更换间隔为半年到一年,请根据下图信息,选出最适合的催化剂___________。
A. | B.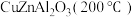 | C.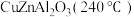 | D. |
(4)在恒温密闭容器中,往容器中注入一定量
 和
和 发生以上反应,若反应达到平衡时
发生以上反应,若反应达到平衡时 和
和 浓度相等,则平衡时的
浓度相等,则平衡时的 的浓度=
的浓度= 。
。(5)通过设计燃料电池(图1),可以将甲醇中蕴藏的能量释放出来,酸性电解质溶液中,甲醇在电极上反应,产生碳氧化物
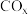 。
。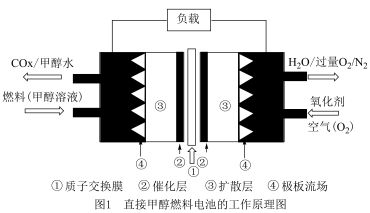
请写出燃料电池负极反应方程式
2 . 煤的洁净技术(包括固硫技术和脱硫技术两类)可有效降低燃煤废气中SO2的含量,已成为我国解决环境问题的主导技术之一。
I.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。石灰石是常用的固硫剂,固硫过程中涉及的部分反应如下:
①CaCO3(s)⇌CaO(s)+CO2(g) ∆H1= +178.30kJ/mol
②CaO(s)+SO2(g)+0.5O2(g)⇌CaSO4(s) ∆H2= -501.92 kJ/mol
③CO(g) + 0.5O2(g)⇌CO2(g) ∆H3
④CaSO4(s) + CO(g)⇌CaO(s) + SO2(g) + CO2(g) ∆H4= +218.92kJ/mol
(1)温度升高,反应①的化学平衡常数
(2)∆H3=
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:
II.电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去,其装置示意图如图所示。
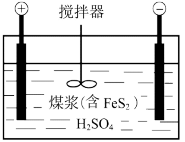
(4)将煤打成煤浆加入电解槽的目的是
(5)阳极的电极反应式为
(6)用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式为(补全并配平):FeS2+·OH =Fe3++SO + H2O +_______
+ H2O +_______
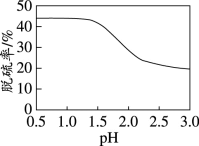
(7)利用上述装置对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;
(1)汽车尾气中的CO、NO、NO2等有毒气体会危害人体健康,可在汽车尾部加催化转化器,将有毒气体转化为无毒气体。
已知:①2NO(g)+O2(g)=2NO2(g) ΔH1=-112.4 kJ·mol-1
②NO2(g)+CO(g)=NO(g)+CO2(g) ΔH2=-234 kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH3=+179.2 kJ·mol-1
请写出CO和NO2生成无污染气体的热化学方程式
(2)若将CO和NO按不同比例投入一密闭容器中发生反应:2CO(g)+2NO(g)
 N2(g)+2CO2(g) ΔH=-759.8 kJ·mol-1,反应达到平衡时,N2的体积分数随n(CO)/n(NO)的变化曲线如图1。
N2(g)+2CO2(g) ΔH=-759.8 kJ·mol-1,反应达到平衡时,N2的体积分数随n(CO)/n(NO)的变化曲线如图1。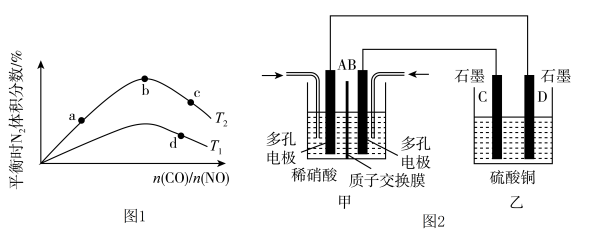
①b点时,平衡体系中C、N原子个数之比接近
②a、b、c三点CO的转化率从大到小的顺序为
③a、c、d三点的平衡常数从大到小的顺序为
④若n(CO)/n(NO)=0.8,反应达平衡时,N2的体积分数为25%,则CO的转化率为
(3)若将NO2与O2通入甲中设计成如图2所示装置,D电极上有红色物质析出,则A电极的电极反应式为
(4)已知:25 ℃时,H2C2O4的电离常数Ka1=5.9×10-2,Ka2=6.4×10-5,25 ℃时,0.1 mol·L-1NaHC2O4溶液中各离子浓度由大到小的顺序为
查阅资料可得有关的化学键键能数据如下:
| 化学键 | N≡N | H-O | N-H | O=O |
| E/ (kJ·mol-1) | 946 | 463 | 391 | 496 |
由此计算上述反应的反应热△H=
(2)已知:N2(g)+O2(g)=2NO(g) K1
N2(g)+3H2(g)=2NH3(g) K2
2H2(g)+O2(g)=2H2O(g) K3
注:K1、K2、K3分别为上述三个反应的平衡常数
回答下列问题:
①氨催化氧化反应(生成气态水)的平衡常数K为
②一定条件下,将4molNH3和5.2molO2混合于容积为4L的恒容密闭容器中发生催化氧化反应,经过10s后达到平衡,测得NO的浓度为0.4mol/L则0到10s内,用NH3表示该反应的平均反应速率为
③若上述反应第一次达到平衡时,保持其他条件不变的情况下,只是将容器的体积扩大一倍,假定在25s后达到新的平衡。请在下图中用曲线表示15~30s这个阶段体系中NH3的浓度随时间变化的趋势。
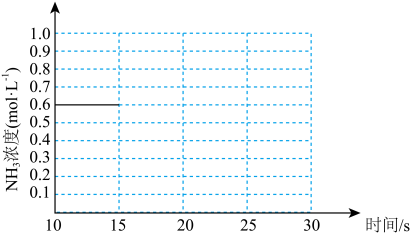
(3)下列有关该反应的说法正确的是
A.恒温恒容,再充入4molNH3和5.2molO2,再次达到平衡时,NH3的转化率增大
B.恒温恒容,当容器内的密度保持不变时,反应达到了平衡
C.当混合气体的平均摩尔质量不变时,反应达到了平衡
D.当2v正(NO)=3v逆(H2O)时,反应达到了平衡
(4)工业上常用氨水吸收SO2,可生成(NH4)2SO3,请判断常温下(NH4)2SO3溶液的酸碱性并通过计算说明判断依据:
 的超干重整,获得富
的超干重整,获得富 产物。装置示意图及反应原理如下。
产物。装置示意图及反应原理如下。
 ,先通
,先通 和
和 混合气,分离水蒸气;再通惰性气体,获得富
混合气,分离水蒸气;再通惰性气体,获得富 产物。各催化剂表面发生的反应为:
产物。各催化剂表面发生的反应为:①
 表面:
表面: (反应①)、
(反应①)、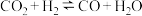 (反应②)
(反应②)②
 表面:
表面: (反应③)、
(反应③)、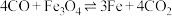 (反应④)
(反应④)③
 表面:
表面: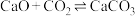 (反应⑤)
(反应⑤)请回答:
(1)已知反应①的
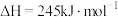 且
且 的燃烧热为
的燃烧热为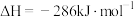 ,则
,则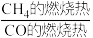
(2)
 催化下,研究单独使用
催化下,研究单独使用 对反应②的影响:
对反应②的影响: 。
。①该反应的反应速率与浓度关系可表示为:
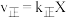 、
、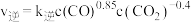 ,其中
,其中 、
、 为速率常数。则
为速率常数。则
②某温度下该反应的平衡常数
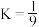 ,将等物质的量的
,将等物质的量的 和
和 通入含
通入含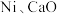 的反应器中,平衡后
的反应器中,平衡后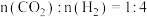 ,则
,则 的转化率为
的转化率为 (结果保留一位小数)。
(结果保留一位小数)。(3)下列说法正确的是_______。
A.获得等量 ,该技术的能耗小于单独用反应①的能耗 ,该技术的能耗小于单独用反应①的能耗 |
B.原料气中 与 与 的物质的量之比必须控制为 的物质的量之比必须控制为 |
C.该技术利用 暂存了 暂存了 ,利用 ,利用 暂存了还原性 暂存了还原性 |
D.须严格控制温度,防止 吸收水蒸气变成 吸收水蒸气变成 |
 平衡产率,原因是
平衡产率,原因是(1)2NO(g)+O2(g)=2NO2(g) △H=akJ/mol的反应历程与能量变化关系如图所示。
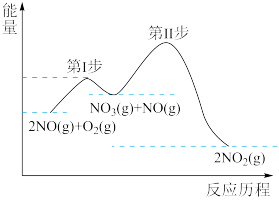
①a
②已知:第Ⅱ步反应为:NO3(g)+NO(g)=2NO2(g) △H=bkJ/mol
第I步反应的热化学方程式为
(2)汽车尾气中常含有NO。NH3在加热和催化剂存在的条件下能消除NO的污染。
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=—905kJ/mol
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=—1268kJ/mol
NH3与NO反应的热化学方程式为
(3)工业上NO的重要来源是NH3,NH3也可作为燃料设计成碱性燃料电池,在碱性条件下,燃料电池产物主要为N2。燃料电池负极的电极反应式为
II.含乙酸钠和对氯酚
 的废水可通过如下装置处理,其原理如图所示:
的废水可通过如下装置处理,其原理如图所示: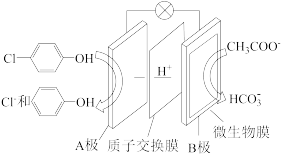
(1)写出HCO3-的电子式
(2)电池的正极是
(3)B极发生的电极反应方程式为
 为原料制备甲烷、甲醇等能源物质具有较好的发展前景。回答下列问题:
为原料制备甲烷、甲醇等能源物质具有较好的发展前景。回答下列问题:(1)
 在固体催化表面加氢合成甲烷过程中发生以下两个反应:
在固体催化表面加氢合成甲烷过程中发生以下两个反应:主反应:
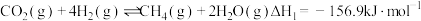
副反应:
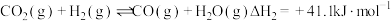
①已知
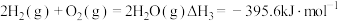 ,则
,则 燃烧的热化学方程式
燃烧的热化学方程式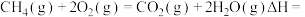
 。
。②对于主反应,在一定条件下存在:
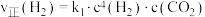 或
或 ,相应的速率与温度关系如图所示。
,相应的速率与温度关系如图所示。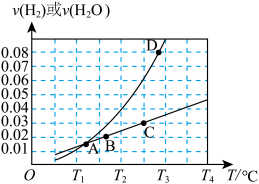
则主反应的平衡常数

 的代数式表示);图中
的代数式表示);图中 四个点中,能表示反应已达到平衡状态的是
四个点中,能表示反应已达到平衡状态的是(2)某研究小组采用双合金团簇催化甲烷干法重整法(DRM)取得了良好的效果。通过大量的研究
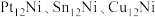 三种双金属合金团簇可用于催化
三种双金属合金团簇可用于催化 反应,在催化剂表面涉及多个基元反应,分别为过程1:甲烷逐步脱氢,过程2:
反应,在催化剂表面涉及多个基元反应,分别为过程1:甲烷逐步脱氢,过程2: 的活化(包括直接活化和氢诱导活化),过程3:
的活化(包括直接活化和氢诱导活化),过程3: 和
和 的氧化,过程4:扩散吸附反应。其反应机理如图所示。
的氧化,过程4:扩散吸附反应。其反应机理如图所示。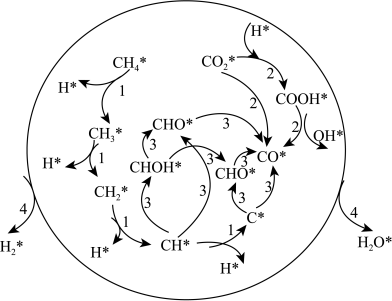
则过程3的最终产物为
(3)光催化
 制甲醇技术也是研究热点。铜基纳米光催化材料还原
制甲醇技术也是研究热点。铜基纳米光催化材料还原 的机理为:光照时,低能价带失去电子并产生空穴(
的机理为:光照时,低能价带失去电子并产生空穴( ,具有强氧化性)。
,具有强氧化性)。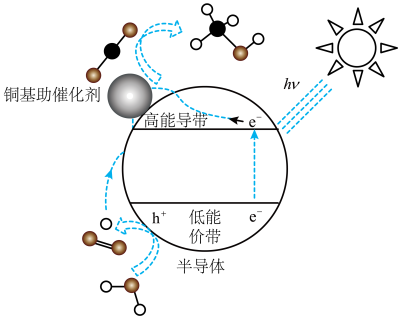
光催化原理与电解原理类似,写出高能导带的电极反应式:
 的还原再生。
的还原再生。
(1)已知:①
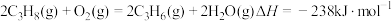
②

则丙烷脱氢制丙烯反应
 的
的 为
为
(2)一定温度下,恒容密闭容器中充入
 ,发生
,发生 反应。
反应。①下列可判断反应达到平衡的是
A.该反应的焓变保持不变 B.气体平均摩尔质量保持不变
C.气体密度保持不变 D.
 分解速率与
分解速率与 消耗速率相等
消耗速率相等②若初始压强为
 ,反应过程中
,反应过程中 的气体体积分数与反应时间的关系如图1所示。此温度下该反应的平衡常数
的气体体积分数与反应时间的关系如图1所示。此温度下该反应的平衡常数
 (用含字母p的代数式表示,
(用含字母p的代数式表示, 是用反应体系中气体物质的平衡分压表示的平衡常数,平衡分压=平衡总压×物质的量分数)。
是用反应体系中气体物质的平衡分压表示的平衡常数,平衡分压=平衡总压×物质的量分数)。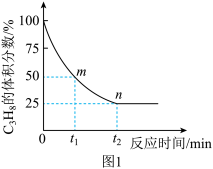
③已知上述反应中,
 ,
, ,其中
,其中 为速率常数,只与温度有关,则图1中m点处
为速率常数,只与温度有关,则图1中m点处
④在压强分别为
 下,丙烷和丙烯的平衡体积分数随温度变化关系如图2所示。图中表示
下,丙烷和丙烯的平衡体积分数随温度变化关系如图2所示。图中表示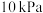 时丙烯的曲线是
时丙烯的曲线是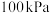 时丙烷的曲线是
时丙烷的曲线是
(3)科学家探索出在无机膜反应器中进行丙烷脱氢制丙烯的技术。在膜反应器中,利用特定功能膜将生成的氢气从反应区一侧有选择性地及时移走。与丙烷直接脱氢法相比,该方法的优点是
(4)利用
 的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。该工艺可采用
的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。该工艺可采用 为催化剂,反应机理如图,其总反应方程式为
为催化剂,反应机理如图,其总反应方程式为
该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是
(1)以下是相同条件下,等体积等浓度的H2O2溶液分解的对比实验时,放出 O2的体积随时间的变化关系示意图(线a为使用FeCl3作催化剂,线b为不使用催化剂),其中正确的图像是______(填字母)。
A. | B.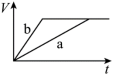 |
C.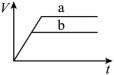 | D.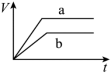 |
Ⅱ.已知下列热化学为程式:
①Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) △H1=﹣25 kJ·mol-1
②Fe2O3(s)+CO(g) = 2FeO(s)+CO2(g) △H2=﹣3 kJ·mol-1
(2)写出Fe被CO2氧化成FeO(s) 和 CO的热化学方程式
一定温度下,向某密闭容器中加入足量铁并充入一定量的CO2气体,发生第(2)题的反应。反应过程中CO2气体和CO气体的浓度变化与时间的关系如图所示。
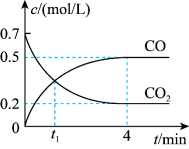
(4)0~4min内, CO的平均反应速率v(CO)=
(5)仅改变下列条件,化学反应速率减小的是
A.减少铁的质量 B.降低温度 C.保持压强不变,充入He使容器的体积增大
Ⅲ.某化学兴趣小组利用反应Cu + 2FeCl3 = CuCl2 + 2FeCl2,设计了如图所示的原电池装置。
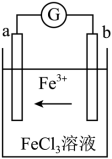
(7)写出b电极上的电极反应式
 和
和 置于预先抽真空的恒容密闭容器中加热到
置于预先抽真空的恒容密闭容器中加热到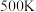 ,体系达平衡后总强为
,体系达平衡后总强为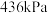 。体系中存在如下反应:
。体系中存在如下反应:①
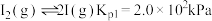
②
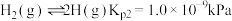
③
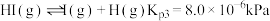
④
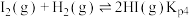
部分物质的键能如下表
| 共价键 | H-H | I-I | H-I |
键能 | 436 | 151 | 299 |
(1)反应④的焓变

 。
。(2)反应开始时
 的分压
的分压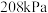 ,平衡后
,平衡后 的分压
的分压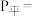
 。
。(3)一定条件下,
 可将溶液中的
可将溶液中的 氧化为
氧化为 。下图体现的是体系吸光度在不同
。下图体现的是体系吸光度在不同 值下随时间的变化关系[吸光度越高表明该体系中
值下随时间的变化关系[吸光度越高表明该体系中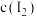 越大]
越大]
①不同
 条件下反应进行
条件下反应进行 时,用曲线序号表示
时,用曲线序号表示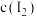 从大到小的顺序是
从大到小的顺序是②
 时,体系的吸光度很快达到最大值,之后快速下降。吸光度快速下降的可能原因是
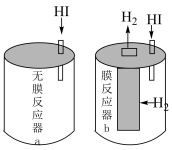
时,体系的吸光度很快达到最大值,之后快速下降。吸光度快速下降的可能原因是(4)某研究小组为提高HI分解率,在恒容密闭容器a基础上设计了一种膜反应器b,
 在反应器内发生分解反应,
在反应器内发生分解反应, 能以恒定速率透过膜并迅速脱离体系。反应开始时两容器中均通入
能以恒定速率透过膜并迅速脱离体系。反应开始时两容器中均通入 气体,保持压强为
气体,保持压强为 ,膜反应器中
,膜反应器中 的逸出速率为
的逸出速率为 。
。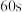 时反应器a中剩余
时反应器a中剩余 的物质的量为
的物质的量为 ,反应器b中
,反应器b中 的分解率是反应器a中分解率的3倍,则
的分解率是反应器a中分解率的3倍,则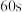 时容器a与容器b中
时容器a与容器b中 的物质的量之比为
的物质的量之比为