反应I:


反应II:


已知:①平衡状态下,甲醛选择性
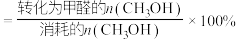 ;甲醛的收率
;甲醛的收率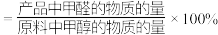 。
。②几种物质的燃烧热
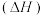 如下表:
如下表:| 物质 |  |  |  |  |
燃烧热 | -725.8 | -563.6 | -283.0 | -285.8 |
(1)

(2)反应I、反应II的反应历程可表示为:
历程i:……
历程ii:
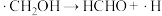
历程iii:

历程iv:
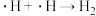
写出历程i的反应方程式:
(3)将
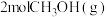 加入容积为2L的刚性密闭容器中,温度对平衡状态下
加入容积为2L的刚性密闭容器中,温度对平衡状态下 的选择性和收率的影响如图所示:
的选择性和收率的影响如图所示: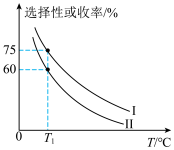
②
 ℃,反应进行到10min时达到平衡,此时
℃,反应进行到10min时达到平衡,此时 的转化率为
的转化率为

 。
。

 ,若起始时向密闭容器中加入2molCO(g)和
,若起始时向密闭容器中加入2molCO(g)和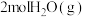 ,充分反应,5min时达到平衡,
,充分反应,5min时达到平衡, 和
和 的质量之和占混合气体总质量的40%,下列说法正确的是
的质量之和占混合气体总质量的40%,下列说法正确的是| A.达到平衡时,CO(g)的转化率为40% |
B.0~5min内,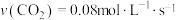 |
| C.达到平衡后,升高温度,平衡常数增大 |
| D.恒容时,增大CO(g)的浓度能增加单位体积内的活化分子百分数 |
3 . 甲基叔戊基醚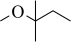 (TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇
(TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇 (简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应(B为2-甲基-1-丁烯的简写,不考虑其他副反应):
(简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应(B为2-甲基-1-丁烯的简写,不考虑其他副反应):


反应ⅱ:
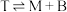

反应ⅲ:

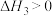
(1)磷钼酸(
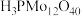 )可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第ⅥB族,核外电子排布与Cr相似。基态钼原子的价层电子排布式为
)可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第ⅥB族,核外电子排布与Cr相似。基态钼原子的价层电子排布式为(2)比较

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)我国学者团队对制备TAME反应的催化剂进行了研究。研究表明:用不同浓度(1~3%)的磷钼酸浸渍催化剂,浓度越大催化剂催化活性越好。用浓度分别为1%、2%、3%的磷钼酸浸渍催化剂进行了三组实验,得到
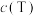 随时间的变化曲线如图所示。
随时间的变化曲线如图所示。
②下列说法正确的有
A.三组实验中,反应速率都随反应进程一直增大
B.平衡后加入惰性溶剂四氢呋喃稀释,
 减小
减小C.催化剂可加快化学反应速率,提高甲醇的平衡转化率
D.降低温度,反应ⅰ和ⅱ的正、逆反应速率都减小
E.达到平衡后,加入M,
 不变
不变(4)研究团队继续研究其他条件不变时,不同醇烯比
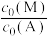 (甲醇M与烯烃A的起始物质的量浓度之比)对平衡的影响,当A起始浓度
(甲醇M与烯烃A的起始物质的量浓度之比)对平衡的影响,当A起始浓度 时,测得平衡时B和T的
时,测得平衡时B和T的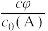 随
随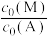 的变化曲线如图。
的变化曲线如图。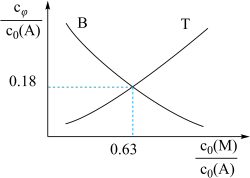
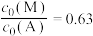 时,计算反应i的平衡常数
时,计算反应i的平衡常数 ,
, 。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中
。常温下,向一定体积的自来水中加入离子交换树脂(NaR),测得自来水中 变化如图所示。下列叙述正确的是
变化如图所示。下列叙述正确的是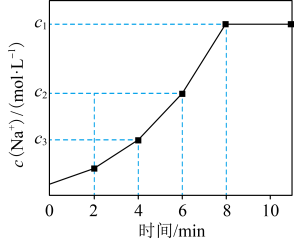
| A.反应达到平衡后,加入少量NaCl,离子交换反应的平衡常数减小 |
| B.6 min时的逆反应速率大于4 min时的逆反应速率 |
| C.其他条件不变时,10 min时离子交换反应已停止 |
D.4~8 min内平均反应速率: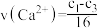 mol⋅L mol⋅L ⋅min ⋅min |
 在金表面分解的实验数据如下表。已知反应物消耗一半所需的时间
在金表面分解的实验数据如下表。已知反应物消耗一半所需的时间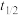 称为半衰期。下列说法错误的是
称为半衰期。下列说法错误的是 | 0 | 20 | 40 | 60 | 80 |
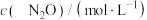 |  | 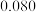 | 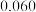 | 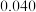 |  |
A. 消耗一半时的反应速率为 消耗一半时的反应速率为 |
B.100min时 消耗完全 消耗完全 |
C.该反应的速率与 的浓度有关 的浓度有关 |
D.该反应的半衰期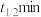 与起始浓度 与起始浓度 的关系满足 的关系满足 |
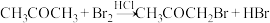 )的速率方程为:
)的速率方程为: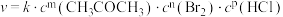 ,其中k为速率常数,与温度有关;“
,其中k为速率常数,与温度有关;“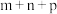 ”为反应级数。某温度时,获得如下实验数据:
”为反应级数。某温度时,获得如下实验数据:| 实验序号 | 初始浓度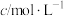 | 溴颜色消失所需时间t/s | ||
 | HCl |  | ||
| ① | 0.80 | 0.20 | 0.0010 | 200 |
| ② | 1.60 | 0.20 | 0.0010 | 100 |
| ③ | 0.80 | 0.40 | 0.0010 | 100 |
| ④ | 0.80 | 0.20 | 0.0020 | 400 |
A.增大 ,能延长溶液颜色消失的时间 ,能延长溶液颜色消失的时间 |
| B.实验②和③的平均速率相等 |
C.实验①在200s内的平均速率 |
| D.反应级数为2 |
7 . 为了消除含金硫精矿中硫对氰化浸出产生的不利影响,使被硫化物包裹的金得以解离,获得孔隙率较高的氧化焙烧渣,需对含金硫精矿进行氧化焙烧预处理。已知焙烧过程中发生的反应有:
反应1:
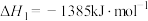
反应2:
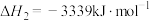
反应3: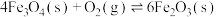

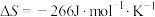
(1)
 分子的VSEPR模型为
分子的VSEPR模型为(2)

 。
。(3)焙烧温度和时间对硫的脱除率和金的浸出率的影响如图。
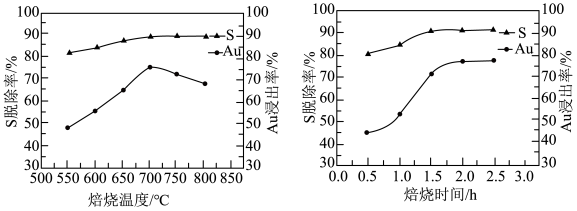
最佳的焙烧温度为
(4)在密闭容器中充入一定量的
 和
和 进行反应,测得平衡时
进行反应,测得平衡时 的体积分数随X的变化关系如图。
的体积分数随X的变化关系如图。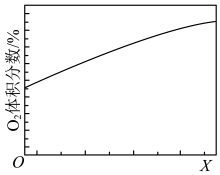
①X表示的是
②下列条件能判断反应1达到平衡状态的是
a. 的生成速率与
的生成速率与 的消耗速率相等 b.
的消耗速率相等 b. 和
和 浓度相等
浓度相等
c.容器中气体的平均摩尔质量不变 d. 的质量保持不变
的质量保持不变
(5)T℃下,在恒压密闭容器中充入1.5

 和3.5
和3.5
 进行反应,已知起始压强为140
进行反应,已知起始压强为140 ,经过10min达到平衡,测得生成
,经过10min达到平衡,测得生成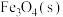 、
、 的物质的量均为0.2
的物质的量均为0.2 。
。①0~10min内, 分压的平均变化率为
分压的平均变化率为 。
。
②T℃下,反应1的压强平衡常数
 (
( 为用分压表示的平衡常数,分压=总压×物质的量分数,列计算式即可)。
为用分压表示的平衡常数,分压=总压×物质的量分数,列计算式即可)。
 既是化工原料,但也是空气污染物。回答下列问题:
既是化工原料,但也是空气污染物。回答下列问题:(1)已知反应:

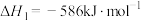 ;
;
 ;
;则反应
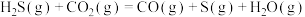 的
的
 。
。(2)
 与
与 在高温下发生反应:
在高温下发生反应: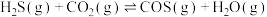
 。在610K时,将
。在610K时,将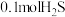 与
与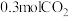 充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时
充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时 的物质的量分数为0.125,用
的物质的量分数为0.125,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
 的平衡转化率
的平衡转化率
(3)利用
 的热分解反应可生产
的热分解反应可生产 :
: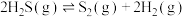 。现将
。现将 通入某恒压(压强
通入某恒压(压强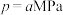 )密闭容器中,在不同温度下测得
)密闭容器中,在不同温度下测得 的平衡转化率如图所示。
的平衡转化率如图所示。
已知:对于气相反应,用某组分(B)的平衡分压(
 )代替物质的量浓度(
)代替物质的量浓度(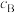 )也可表示平衡常数(
)也可表示平衡常数( )。(
)。(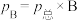 的物质的量分数,
的物质的量分数, 为平衡时气体总压强)。
为平衡时气体总压强)。温度升高时,混合气体的平均摩尔质量
 ℃时。该反应的平衡常数
℃时。该反应的平衡常数
(4)据预测,到2040年我国煤炭消费仍将占能源结构的三分之一左右。
 在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。
在催化活性炭(AC)表面的迁移,对煤的清洁和综合应用起了很大的促进作用,其机理如图所示,其中ad表示物种被吸附的状态。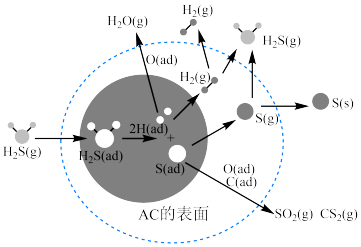
①
 、
、 、
、 的键角从小到大排列顺序为
的键角从小到大排列顺序为②下列有关叙述错误的是
A.图中阴影部分表示
 分子的吸附与解离
分子的吸附与解离B.AC表面的温度不同,
 的去除率不同
的去除率不同C.
 在AC表面作用生成的产物有
在AC表面作用生成的产物有 、
、 、S、
、S、 、
、 等
等D.图中反应过程中只有
 链的断裂。没有
链的断裂。没有 健的形成
健的形成

A.用H2的浓度变化表示0~t1时间内的反应速率v(H2)=0.02/t1mol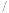 (L·min) (L·min) |
| B.混合气体的平均相对分子质量不再改变时,反应达平衡 |
| C.在该温度下的压强平衡常数为4800(kPa)2 |
| D.若t2时将容器体积迅速缩小至原来的一半,N2分压变化趋势的曲线是a |
 的密闭容器A(恒温)、B(绝热)中均加入
的密闭容器A(恒温)、B(绝热)中均加入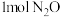 和
和 ,发生反应
,发生反应
 。已知:
。已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数,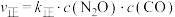 ,
,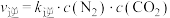 ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法中错误的是
的转化率随时间的变化关系如图所示。下列说法中错误的是
A.曲线M、N的平衡常数大小为: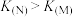 |
B. 与 与 浓度比为 浓度比为 且保持不变,不能说明反应达到平衡状态 且保持不变,不能说明反应达到平衡状态 |
C.T℃时,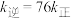 |
D.用CO的浓度变化表示曲线N在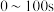 内的平均速率为 内的平均速率为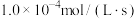 |



