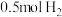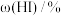名校
1 . 工业制氢,反应Ⅰ:
 ,
,
反应Ⅱ:
 。
。
维持T℃、560kPa不变,向容积可变的密闭容器中投入10mol 和10mol
和10mol  ,
, 、CO的转化率随时间的变化分别对应如图甲、乙曲线。下列说法错误的是
、CO的转化率随时间的变化分别对应如图甲、乙曲线。下列说法错误的是

 ,
,反应Ⅱ:

 。
。维持T℃、560kPa不变,向容积可变的密闭容器中投入10mol
 和10mol
和10mol  ,
, 、CO的转化率随时间的变化分别对应如图甲、乙曲线。下列说法错误的是
、CO的转化率随时间的变化分别对应如图甲、乙曲线。下列说法错误的是
A.开始时, 的分压 的分压 |
B.50min后反应到达平衡,平均反应速率可表达为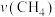 为2.24kPa/min 为2.24kPa/min |
C.保持温度不变,若增大压强, 的转化率变化曲线将是丙 的转化率变化曲线将是丙 |
| D.保持压强不变,若降低温度,CO的转化率变化曲线将是戊 |
您最近一年使用:0次
名校
2 . 过硫酸钠(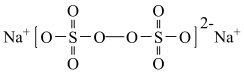 ),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对
),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对 制备和性质及用途进行探究。
制备和性质及用途进行探究。

工业制备过硫酸钠的反应原理:
主反应:

副反应:

实验室设计如图实验装置:
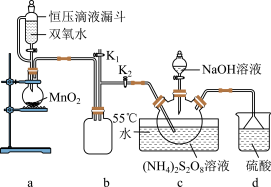
(2)装置b的作用是
(3)上述反应过程中,d装置中主要发生的化学反应方程式为
Ⅱ.探究
 的性质与用途
的性质与用途(4)
 用于废水中苯酚的降解
用于废水中苯酚的降解已知:a.
 具有强氧化性,
具有强氧化性, 浓度较高时会导致
浓度较高时会导致 淬灭。
淬灭。b.
 可将苯酚氧化,但反应速率较慢,加入
可将苯酚氧化,但反应速率较慢,加入 可加快反应。
可加快反应。过程为ⅰ.

ⅱ.
 将苯酚氧化为
将苯酚氧化为 气体
气体①
 氧化苯酚的离子方程式是
氧化苯酚的离子方程式是②将含
 的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。
的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。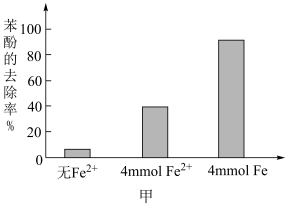
 ,可明显提高苯酚的降解率,主要原因是
,可明显提高苯酚的降解率,主要原因是(5)工业上利用
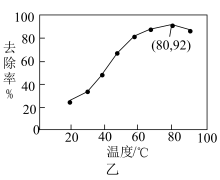
 能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含
能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含 的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为
的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为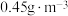 ,
, 达到最大去除率,NO去除的平均反应速率:
达到最大去除率,NO去除的平均反应速率:
 。
。
您最近一年使用:0次
名校
3 . 在不同温度下向容积为 的密闭容器中充入一定量
的密闭容器中充入一定量 ,发生反应
,发生反应
 。若在
。若在 时,通入
时,通入 ,
, 时达到平衡状态;
时达到平衡状态;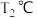 时,通入
时,通入 ,
, 时达到平衡状态。已知反应过程中有关物质的物质的量随时间的变化曲线如图所示。
时达到平衡状态。已知反应过程中有关物质的物质的量随时间的变化曲线如图所示。
 的密闭容器中充入一定量
的密闭容器中充入一定量 ,发生反应
,发生反应
 。若在
。若在 时,通入
时,通入 ,
, 时达到平衡状态;
时达到平衡状态;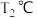 时,通入
时,通入 ,
, 时达到平衡状态。已知反应过程中有关物质的物质的量随时间的变化曲线如图所示。
时达到平衡状态。已知反应过程中有关物质的物质的量随时间的变化曲线如图所示。
A. |
B. 时, 时, 的平均反应速率为 的平均反应速率为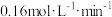 |
C.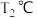 时, 时, 的平衡转化率约为 的平衡转化率约为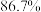 |
D. 时,该反应的平衡常数 时,该反应的平衡常数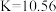 |
您最近一年使用:0次
名校
4 . 苯乙烯是合成树脂及合成橡胶等的重要单体,在催化剂作用下,可由乙苯直接脱氢制备: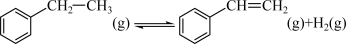 。在
。在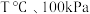 反应条件下,向甲、乙、丙三个容器中分别通入n(乙苯):
反应条件下,向甲、乙、丙三个容器中分别通入n(乙苯):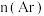 为
为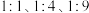 的混合气体,发生上述反应,测得乙苯转化率随时间变化如图所示。下列说法不正确的是
的混合气体,发生上述反应,测得乙苯转化率随时间变化如图所示。下列说法不正确的是

A. 时,该反应的 时,该反应的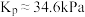 |
B.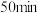 时,容器乙中的反应未达到平衡状态 时,容器乙中的反应未达到平衡状态 |
| C.保持其他条件不变,将甲变为恒容容器,则平衡转化率变小 |
D. 内,乙苯的平均反应速率 内,乙苯的平均反应速率 最大的容器是丙 最大的容器是丙 |
您最近一年使用:0次
名校
5 . 我国成功利用大功率运载火箭发射“天宫二号”空间实验室。火箭推进器中装有还原剂肼(N2H4)(液态)和强氧化剂过氧化氢(H2O2),请回答下列问题:
(1)肼又名联氨,其结构式为_____ 。
(2)液态肼与过氧化氢的反应属于_____ (填“吸热”或“放热”)反应。
(3)写出该火箭推进器中相关反应的化学方程式:_____ 。
(4)在一定温度下,向0.5L密闭容器中充入2molN2H4和2molO2发生如下反应:N2H4(g)+O2(g)⇌N2(g)+2H2O(g),其中有关物质的物质的量随时间变化的曲线如图所示,请回答下列问题:_____
②下列能说明该反应达到平衡状态的是_____ 。
A.υ正(N2)=2υ逆(H2O)
B.c(N2H4):c(O2):c(N2)=1:1:1
C.体系的压强不再发生变化
D.混合气体的密度不再发生变化
E.每断开1molO=O键,同时断开4molH-O键
③该反应达到平衡时,O2的体积百分数为_____ (结果保留一位小数)
④下列措施能够增大正反应的化学反应速率的有( )
A.升高反应温度 B.加入适当的催化剂C.向容器中加入氧气 D.向容器中加入氖气
(5)广泛应用的肼(N2H4)燃料电池属于环境友好型电池,该电池以空气中的氧气作氧化剂,氢氧化钠溶液作电解质,其负极的电极方程式:_____
(1)肼又名联氨,其结构式为
(2)液态肼与过氧化氢的反应属于
(3)写出该火箭推进器中相关反应的化学方程式:
(4)在一定温度下,向0.5L密闭容器中充入2molN2H4和2molO2发生如下反应:N2H4(g)+O2(g)⇌N2(g)+2H2O(g),其中有关物质的物质的量随时间变化的曲线如图所示,请回答下列问题:
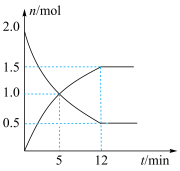
②下列能说明该反应达到平衡状态的是
A.υ正(N2)=2υ逆(H2O)
B.c(N2H4):c(O2):c(N2)=1:1:1
C.体系的压强不再发生变化
D.混合气体的密度不再发生变化
E.每断开1molO=O键,同时断开4molH-O键
③该反应达到平衡时,O2的体积百分数为
④下列措施能够增大正反应的化学反应速率的有
A.升高反应温度 B.加入适当的催化剂C.向容器中加入氧气 D.向容器中加入氖气
(5)广泛应用的肼(N2H4)燃料电池属于环境友好型电池,该电池以空气中的氧气作氧化剂,氢氧化钠溶液作电解质,其负极的电极方程式:
您最近一年使用:0次
名校
解题方法
6 . 研究发现燃煤脱硫过程中生成的 CaSO₄(s) 与 CO(g) 在密闭体系中将发生如下反应:
Ⅰ.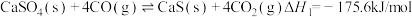
Ⅱ.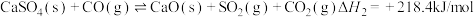
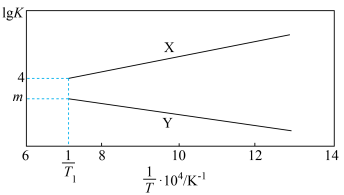
已知图为反应Ⅰ和反应Ⅱ的平衡常数(K) 与温度(T) 的变化关系。现维持温度为 T1,往某2L刚性密闭反应器中投入足量的CaSO4(s) 和1mol CO(g),经t小时反应体系达到平衡,此时体系压强为原来的1.4倍。下列说法正确的是
Ⅰ.
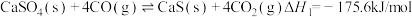
Ⅱ.
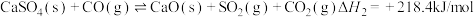
已知图为反应Ⅰ和反应Ⅱ的平衡常数(K) 与温度(T) 的变化关系。现维持温度为 T1,往某2L刚性密闭反应器中投入足量的CaSO4(s) 和1mol CO(g),经t小时反应体系达到平衡,此时体系压强为原来的1.4倍。下列说法正确的是

A.若用生石灰固硫的反应为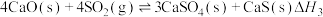 ,则 ,则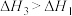 |
B.提高反应体系的温度能降低反应体系中 的生成量 的生成量 |
C.反应体系中 CO 的消耗速率为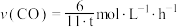 |
| D.m≈0.3 |
您最近一年使用:0次
名校
7 . CuBr2的分解反应为2CuBr2(s)=2CuBr(s)+Br2(g) ΔH=+105.4kJ/mol。起始状态Ⅰ中有CuBr2、CuBr和 Br2,经下列过程达到各平衡状态:

已知状态Ⅰ 和Ⅲ的固体质量相等,上述过程中Br2始终为气态。下列叙述正确的是

已知状态Ⅰ 和Ⅲ的固体质量相等,上述过程中Br2始终为气态。下列叙述正确的是
| A.从Ⅰ到Ⅱ的过程 ΔS<0 |
| B.平衡常数:K(Ⅱ)>K(Ⅳ) |
C.若体积V(Ⅰ)=2V(Ⅲ),则Q(Ⅰ)= K(Ⅲ) K(Ⅲ) |
| D.逆反应的速率:v(Ⅰ)>v(Ⅱ)=v(Ⅲ)>v(Ⅳ) |
您最近一年使用:0次
名校
解题方法
8 . 为了实现“碳中和”的目标,有多种方式,如节能减排,吸收储存,转化等。工业上用下列反应I将CO2进行加氢转化成甲醇,反应I: ,同时还伴有副反应II:
,同时还伴有副反应II: 。
。
(1)已知H2,CH3OH的燃烧热△H分别为-285.8kJ/mol,-726.5kJ/mol,水,甲醇的汽化热分别为44kJ/mol,39.4kJ/mol,则反应I的△H=___________ 。
(2)在一容器中以物质的量之比1:3的比例通入CO2和H2,并通入少量H2O(g)活化催化剂Cu/ZnO,得出的结果如下图所示,请选出最适宜的合成条件___________ (选择水蒸气含量和反应时间)。___________ 路径。(选“COOH*”或“HCOO*”)___________ ,甲醇的反应速率为___________ Pa/h(单位为Pa/h),反应II的Kp=___________ 。
(5)工业上还可用In2O3电极电化学还原CO2得到HCOO-,另一石墨电极得到产品CH3(CH2)6CN,写出阴极的电极反应:___________ ,当外电路转移1mol电子时,生成的产品CH3(CH2)6CN的物质的量为___________ 。
 ,同时还伴有副反应II:
,同时还伴有副反应II: 。
。(1)已知H2,CH3OH的燃烧热△H分别为-285.8kJ/mol,-726.5kJ/mol,水,甲醇的汽化热分别为44kJ/mol,39.4kJ/mol,则反应I的△H=
(2)在一容器中以物质的量之比1:3的比例通入CO2和H2,并通入少量H2O(g)活化催化剂Cu/ZnO,得出的结果如下图所示,请选出最适宜的合成条件


(5)工业上还可用In2O3电极电化学还原CO2得到HCOO-,另一石墨电极得到产品CH3(CH2)6CN,写出阴极的电极反应:

您最近一年使用:0次
名校
解题方法
9 . 甲醇(CH3OH)可以由碳的氧化物和氢气合成,主要反应包括:
a.
b.
c.
(1)
___________ 
(2)反应a的反应历程如下图所示,其中吸附在催化剂表面上的物种用(*)标注。

写出相对能量为-1.3eV时,对应物质M的化学式___________ ;该反应历程中决速步骤的能垒为___________ eV。
(3)在恒温(T/℃)容积可变的密闭容器中按体积比1∶3充入CO2和H2,若只发生反应b,反应达到平衡时,H2体积分数x随压强p的变化如图曲线a所示,则曲线___________ (填标号)表示了CH3OH的体积分数x随压强p的变化;点A、B均表示H2体积分数,则A点处v(正)___________ B点处v(逆)(填“>”、“<”或“=”)。

(4)在恒温恒容(2L)的密闭容器中充入CO、CO2各1mol和一定量的氢气发生上述a、b、c三个反应,10min达到平衡状态,生成(0.3molCH3OH和0.15molH2O。
①若升高温度,CO的平衡转化率___________ (填“增大”、“减小”、“不变”或“不能确定”)。
②0~10min内,平均每分钟生成甲醇(CH3OH)___________ mol/L;若c反应的平衡常数为K,则平衡时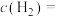
___________ (用含K的式子表达)。
a.

b.

c.

(1)


(2)反应a的反应历程如下图所示,其中吸附在催化剂表面上的物种用(*)标注。

写出相对能量为-1.3eV时,对应物质M的化学式
(3)在恒温(T/℃)容积可变的密闭容器中按体积比1∶3充入CO2和H2,若只发生反应b,反应达到平衡时,H2体积分数x随压强p的变化如图曲线a所示,则曲线

(4)在恒温恒容(2L)的密闭容器中充入CO、CO2各1mol和一定量的氢气发生上述a、b、c三个反应,10min达到平衡状态,生成(0.3molCH3OH和0.15molH2O。
①若升高温度,CO的平衡转化率
②0~10min内,平均每分钟生成甲醇(CH3OH)
您最近一年使用:0次
2023-11-11更新
|
309次组卷
|
2卷引用:西南大学附属中学校2023-2024学年高二上学期期中考试化学试题
10 . 体积均为 的密闭容器中进行如下实验,在温度为
的密闭容器中进行如下实验,在温度为 时测得气体混合物中碘化氢的物质的量分数
时测得气体混合物中碘化氢的物质的量分数 与反应时间
与反应时间 的关系如表:
的关系如表:
上述反应中 (正)
(正) ,
, (逆)
(逆)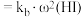 ,其中
,其中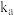 、
、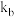 为常数。下列说法正确的是
为常数。下列说法正确的是
 的密闭容器中进行如下实验,在温度为
的密闭容器中进行如下实验,在温度为 时测得气体混合物中碘化氢的物质的量分数
时测得气体混合物中碘化氢的物质的量分数 与反应时间
与反应时间 的关系如表:
的关系如表:容器编号 | 起始物质 |
| 0 | 20 | 40 | 60 | 80 | 100 |
I |
|
| 0 | 50 | 68 | 76 | 80 | 80 |
II |
|
| 100 | 91 | 84 | 81 | 80 | 80 |
 (正)
(正) ,
, (逆)
(逆)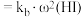 ,其中
,其中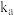 、
、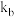 为常数。下列说法正确的是
为常数。下列说法正确的是A.温度为 时该反应的 时该反应的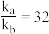 |
B.容器I中前 的平均速率 的平均速率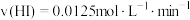 |
C. 的值一定为1 的值一定为1 |
| D.容器Ⅱ中达到平衡时的转化率为20% |
您最近一年使用:0次


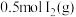 、
、