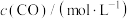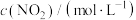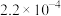2024高三·全国·专题练习
解题方法
1 . 二甲醚是重要的有机合成原料,工业上常用合成气(主要成分为CO、H2)制备二甲醚,其主要反应如下。
反应ⅰ:CO(g)+2H2(g) CH3OH(g);
CH3OH(g);
反应ⅱ:2CH3OH(g) CH3OCH3(g)+H2O(g);
CH3OCH3(g)+H2O(g);
反应ⅲ:CO(g)+H2O(g) CO2(g)+H2(g)。
CO2(g)+H2(g)。
(1)一定温度下,在体积为2 L的刚性容器中充入4 mol CO(g)和8 mol H2(g)制备二甲醚,4 min时达到平衡,平衡时CO(g)的转化率为80%,c(H2)=1.4 mol·L-1,且c(CH3OH)=2c(CH3OCH3)。反应ⅲ的平衡常数Kc=_______ (保留三位有效数字)。
(2)实际工业生产中,需要在260 ℃、压强恒为4.0 MPa的反应釜中进行上述反应。初始时向反应釜中加入0.01 mol CO(g)和0.02 mol H2(g),为确保反应的连续性,需向反应釜中以n(CO)∶n(H2)=1∶2、进气流量0.03 mol·min-1持续通入原料,同时控制出气流量。①已知出气流量为0.02 mol·min-1,单位时间内CO(g)的转化率为60%,则流出气体中CO2(g)的百分含量为_______ 。②需控制出气流量小于进气流量的原因为_______ 。
(3)在ZnxO催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。______________ 。
②在合成甲醇过程中,需要不断分离出甲醇的原因为_______ 。
反应ⅰ:CO(g)+2H2(g)
 CH3OH(g);
CH3OH(g);反应ⅱ:2CH3OH(g)
 CH3OCH3(g)+H2O(g);
CH3OCH3(g)+H2O(g);反应ⅲ:CO(g)+H2O(g)
 CO2(g)+H2(g)。
CO2(g)+H2(g)。(1)一定温度下,在体积为2 L的刚性容器中充入4 mol CO(g)和8 mol H2(g)制备二甲醚,4 min时达到平衡,平衡时CO(g)的转化率为80%,c(H2)=1.4 mol·L-1,且c(CH3OH)=2c(CH3OCH3)。反应ⅲ的平衡常数Kc=
(2)实际工业生产中,需要在260 ℃、压强恒为4.0 MPa的反应釜中进行上述反应。初始时向反应釜中加入0.01 mol CO(g)和0.02 mol H2(g),为确保反应的连续性,需向反应釜中以n(CO)∶n(H2)=1∶2、进气流量0.03 mol·min-1持续通入原料,同时控制出气流量。①已知出气流量为0.02 mol·min-1,单位时间内CO(g)的转化率为60%,则流出气体中CO2(g)的百分含量为
(3)在ZnxO催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
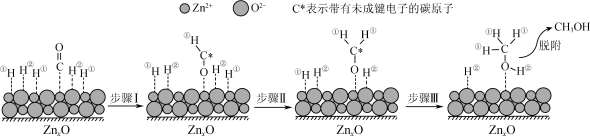
②在合成甲醇过程中,需要不断分离出甲醇的原因为
您最近一年使用:0次
2024·广东·一模
2 . 工业合成氨是人类科学技术的一项重大突破,选择高效催化剂实现降能提效是目前研究的重点。回答下列问题:
(1)合成氨反应为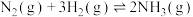
 ,理论上
,理论上___________ (填“高”或“低”,下同)温有利于提高反应速率,___________ 温有利于提高平衡转化率。
(2)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:
①写出 参与化学吸附的反应方程式:
参与化学吸附的反应方程式:___________ 。
②以上历程须克服的最大能垒为___________ eV。
(3)在t℃、压强为0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示: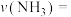
___________  ,该反应的
,该反应的
___________ (用数字表达式表示, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
②下列叙述能说明该条件下反应达到平衡状态的是___________ (填标号)。
a.氨气的体积分数保持不变 b.容器中氢氮比保持不变
c. 和
和 的平均反应速率之比为1∶2 d.气体密度保持不变
的平均反应速率之比为1∶2 d.气体密度保持不变
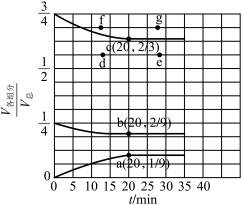
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中___________ (填“d”“e”“f”或“g”)点。
(1)合成氨反应为
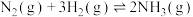
 ,理论上
,理论上(2)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:
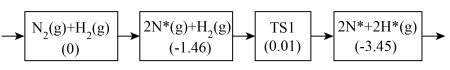
①写出
 参与化学吸附的反应方程式:
参与化学吸附的反应方程式:②以上历程须克服的最大能垒为
(3)在t℃、压强为0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示:
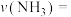
 ,该反应的
,该反应的
 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。②下列叙述能说明该条件下反应达到平衡状态的是
a.氨气的体积分数保持不变 b.容器中氢氮比保持不变
c.
 和
和 的平均反应速率之比为1∶2 d.气体密度保持不变
的平均反应速率之比为1∶2 d.气体密度保持不变③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中
您最近一年使用:0次
名校
解题方法
3 . 根据化学反应速率和化学反应限度的知识回答下列问题:
Ⅰ.某温度时,在2 L容器中发生A、B两种物质间的转化反应,AB物质的量随时间变化的曲线如图所示:___________ 。
(2)反应开始至4 min时,A的平均反应速率为___________ 。
(3)4 min时,反应是否达平衡状态?___________ (填“是”或“否”),8 min时,v正___________ v逆。(填“>”“<”或“=”)
Ⅱ.氢气是合成氨的重要原料,合成氨反应的化学方程式为N2(g)+3H2(g) ⇌2NH3(g),该反应为放热反应,且每生成2 mol NH3,放出92.4 kJ的热量。当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。___________ 。
(5)在一定温度下,向一个容积为1 L的容器中通入2 mol氮气和
8 mol氢气及固体催化剂,使之反应。已知平衡时容器内气体的压强为起始时的80%。
①N2的转化率为___________ 。
②反应达到平衡时,放出的热量___________ (填字母,下同)。
A.小于92.4 kJ B.等于92.4 kJ
C.大于92.4 kJ D.可能大于、小于或等于92.4 kJ
(6)若该反应在绝热条件下进行,下列能证明反应已达化学平衡的为___________ 。
A.混合气体的平均相对分子质量
B.体系的温度不变
C.N2、H2、NH3的分子数之比为1:3:2
D.混合气体的密度不变
E.断开3 mol H-H键的同时断开2 mol N-H键
(7)反应达到平衡后,保持其他条件不变,t0时刻升高温度,请在图中画出 改变条件后至达到新平衡时v正、v逆的变化曲线并注明v正、v逆(在答题卡做答)__________
Ⅰ.某温度时,在2 L容器中发生A、B两种物质间的转化反应,AB物质的量随时间变化的曲线如图所示:
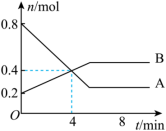
(2)反应开始至4 min时,A的平均反应速率为
(3)4 min时,反应是否达平衡状态?
Ⅱ.氢气是合成氨的重要原料,合成氨反应的化学方程式为N2(g)+3H2(g) ⇌2NH3(g),该反应为放热反应,且每生成2 mol NH3,放出92.4 kJ的热量。当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。

(5)在一定温度下,向一个容积为1 L的容器中通入2 mol氮气和
8 mol氢气及固体催化剂,使之反应。已知平衡时容器内气体的压强为起始时的80%。
①N2的转化率为
②反应达到平衡时,放出的热量
A.小于92.4 kJ B.等于92.4 kJ
C.大于92.4 kJ D.可能大于、小于或等于92.4 kJ
(6)若该反应在绝热条件下进行,下列能证明反应已达化学平衡的为
A.混合气体的平均相对分子质量
B.体系的温度不变
C.N2、H2、NH3的分子数之比为1:3:2
D.混合气体的密度不变
E.断开3 mol H-H键的同时断开2 mol N-H键
(7)反应达到平衡后,保持其他条件不变,t0时刻升高温度,请在图中画出 改变条件后至达到新平衡时v正、v逆的变化曲线并注明v正、v逆(在答题卡做答)

您最近一年使用:0次
2024-04-30更新
|
279次组卷
|
2卷引用:名校期中好题汇编-化学反应与能量(非选择题)
4 . Ⅰ.甲醇是一种理想的储氢载体,我国科学家研发的全球首套太阳能燃料合成项目被称为“液态阳光”计划,可利用太阳能电解水产生H2,再将CO2与H2转化为甲醇,以实现碳中和。
(1)下列关于甲醇(CH3OH)的说法中,正确的是___________
Ⅱ.已知,CO2生产甲醇过程主要发生以下反应:
反应Ⅰ.CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ∆H1= −48.97kJ·mol−1
CH3OH(g) + H2O(g) ∆H1= −48.97kJ·mol−1
反应Ⅱ.CO2(g) + H2(g) CO(g) + H2O(g) ∆H2= +41.17 kJ·mol−1
CO(g) + H2O(g) ∆H2= +41.17 kJ·mol−1
反应Ⅲ.CO(g) + 2H2(g) CH3OH(g) ∆H3
CH3OH(g) ∆H3
(2)反应Ⅲ中,①活化能E(正)___________ E (逆) (填“>”、“<”或“=”);
②该反应在___________ 条件下能自发进行;
A.在高温条件下自发进行 B.在低温条件下自发进行
C.在任何条件下都能自发进行 D.在任何条件下都不能自发进行
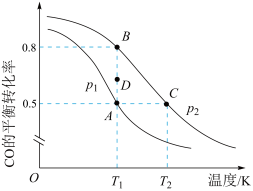
(3)反应III中,CO的平衡转化率与温度的关系如图所示:___________ 。T1时,由D点到B点过程中,正、逆反应速率之间的关系:v正 ___________ v逆。(填“>”、“<”或“=”)
②向某恒温恒压密闭 容器中充入1mol CO(g)和2mol H2(g),下列能说明反应III达到平衡的是___________ ;
A.容器内混合气体的密度不再改变
B.容器内混合气体的平均相对分子质量不再改变
C.两种反应物转化率的比值不再改变
D.v正(CO)=2 v逆(H2)
③在2L恒容密闭 容器中充入2mol CO和4mol H2,在p2和T1条件下经10min达到平衡状态。在该条件下,v(H2)=___________ mol·L−1·min−1。
(4)在CO2加氢合成甲醇的体系中,①下列说法不正确的是___________ ;
A.若在绝热恒容 容器,反应I的平衡常数K保持不变,说明反应I、II都已达平衡
B.若气体的平均相对分子质量不变,说明反应I、II都已达平衡
C.体系达平衡后,若压缩体积,反应I平衡正向移动,反应II平衡不移动
D.选用合适的催化剂可以提高甲醇在单位时间内的产量
②已知:CH3OH的选择性=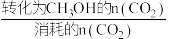 ×100%,不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是
×100%,不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是___________ ,并说明其原因
A.高温高压 B.高温低压 C.低温低压 D.低温高压
原因:___________
(5)我国科学家设计了离子液体电还原CO2合成CH3OH工艺,写出碱性条件下CO2生成甲醇的电极反应式___________ 。
(1)下列关于甲醇(CH3OH)的说法中,正确的是___________
| A.甲醇在一定条件下可被氧化生成CO2 | B.甲醇储氢符合“相似相溶”原理 |
C.甲醇官能团的电子式: | D.甲醇分子是含有极性键的非极性分子 |
Ⅱ.已知,CO2生产甲醇过程主要发生以下反应:
反应Ⅰ.CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) ∆H1= −48.97kJ·mol−1
CH3OH(g) + H2O(g) ∆H1= −48.97kJ·mol−1 反应Ⅱ.CO2(g) + H2(g)
 CO(g) + H2O(g) ∆H2= +41.17 kJ·mol−1
CO(g) + H2O(g) ∆H2= +41.17 kJ·mol−1反应Ⅲ.CO(g) + 2H2(g)
 CH3OH(g) ∆H3
CH3OH(g) ∆H3(2)反应Ⅲ中,①活化能E(正)
②该反应在
A.在高温条件下自发进行 B.在低温条件下自发进行
C.在任何条件下都能自发进行 D.在任何条件下都不能自发进行
(3)反应III中,CO的平衡转化率与温度的关系如图所示:
②向某
A.容器内混合气体的密度不再改变
B.容器内混合气体的平均相对分子质量不再改变
C.两种反应物转化率的比值不再改变
D.v正(CO)=2 v逆(H2)
③在2L
(4)在CO2加氢合成甲醇的体系中,①下列说法不正确的是
A.若在
B.若气体的平均相对分子质量不变,说明反应I、II都已达平衡
C.体系达平衡后,若压缩体积,反应I平衡正向移动,反应II平衡不移动
D.选用合适的催化剂可以提高甲醇在单位时间内的产量
②已知:CH3OH的选择性=
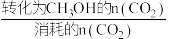 ×100%,不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是
×100%,不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是A.高温高压 B.高温低压 C.低温低压 D.低温高压
原因:
(5)我国科学家设计了离子液体电还原CO2合成CH3OH工艺,写出碱性条件下CO2生成甲醇的电极反应式
您最近一年使用:0次
名校
5 . 汽车尾气净化反应2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=-746.8 kJ/mol,ΔS=-197.5J/(mol·K)。为了探究其转化效率,某小组利用传感器测定一定温度下投入
N2(g)+2CO2(g) ΔH=-746.8 kJ/mol,ΔS=-197.5J/(mol·K)。为了探究其转化效率,某小组利用传感器测定一定温度下投入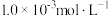 NO、
NO、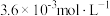 CO的物质的量浓度与时间关系如图所示:
CO的物质的量浓度与时间关系如图所示:
 N2(g)+2CO2(g) ΔH=-746.8 kJ/mol,ΔS=-197.5J/(mol·K)。为了探究其转化效率,某小组利用传感器测定一定温度下投入
N2(g)+2CO2(g) ΔH=-746.8 kJ/mol,ΔS=-197.5J/(mol·K)。为了探究其转化效率,某小组利用传感器测定一定温度下投入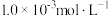 NO、
NO、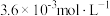 CO的物质的量浓度与时间关系如图所示:
CO的物质的量浓度与时间关系如图所示:
| A.上述正反应在较高温度下能自发进行 |
| B.b→c段反应速率v(NO)=0.1 mol/(L·s) |
| C.单位时间内消耗NO和消耗CO2浓度相等时达到平衡状态 |
| D.该温度下,上述反应的平衡常数K=500 |
您最近一年使用:0次
2024-03-18更新
|
494次组卷
|
4卷引用:河北省2023-2024学年高三下学期3月省级联测化学试题
河北省2023-2024学年高三下学期3月省级联测化学试题(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)江西省宜春市宜丰中学2023-2024学年高二下学期3月月考化学试题湖南省衡阳市衡阳县第一中学2023-2024学年高三下学期4月月考化学试题
名校
解题方法
6 . 汞及其化合物广泛应用于医药、冶金及其他精密高新科技领域。
(1)干燥的 固体上通入
固体上通入 可反应制得
可反应制得 和
和 ,反应的化学方程式为
,反应的化学方程式为___________ 。该反应中氧化产物是___________ 。
(2)富氧燃烧烟气中 的脱除主要是通过与
的脱除主要是通过与 反应实现,反应的化学方程式为
反应实现,反应的化学方程式为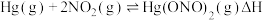
根据实验结果,有研究组提出了 与
与 的可能反应机理:
的可能反应机理:

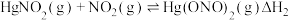

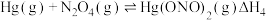
①根据盖斯定律,
___________ (写出一个代数式即可)。
②上述反应体系在一定条件下建立平衡后,下列说法正确的是___________ 。
A.增大 的浓度,可提高
的浓度,可提高 的平衡脱除率
的平衡脱除率
B.升高温度,正反应速率增大,逆反应速率减小
C.恒温恒压下充入 ,可提高原料的平衡转化率
,可提高原料的平衡转化率
D.加入催化剂,可降低反应活化能,提高脱除速率
③在常压、温度范围为15~60℃条件下,将浓度为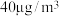 汞蒸气和
汞蒸气和 的
的 气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。
气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。 的平均脱除反应速率为
的平均脱除反应速率为___________ 
ⅱ)
___________ 0(填“>”或“<”)
④富氧燃烧烟气中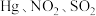 等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于
等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于 转化为
转化为 而脱除,但随着循环水量的增大,
而脱除,但随着循环水量的增大, 的去除率下降,其原因可能是
的去除率下降,其原因可能是___________ 。 溶液可用于手术刀消毒。
溶液可用于手术刀消毒。 与
与 的混合溶液中主要存在平衡:
的混合溶液中主要存在平衡:

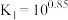
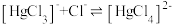
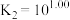
 的
的 溶液中加入
溶液中加入 固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数
固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数 随
随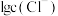 的变化如图所示
的变化如图所示 ]。
]。
①熔融状态的 不能导电,
不能导电, 是
是___________ (填“共价”或“离子”)化合物。
②A点溶液中
___________  。
。
③A点溶液中 的转化率为
的转化率为___________ (列出计算式)。
(1)干燥的
 固体上通入
固体上通入 可反应制得
可反应制得 和
和 ,反应的化学方程式为
,反应的化学方程式为(2)富氧燃烧烟气中
 的脱除主要是通过与
的脱除主要是通过与 反应实现,反应的化学方程式为
反应实现,反应的化学方程式为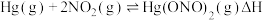
根据实验结果,有研究组提出了
 与
与 的可能反应机理:
的可能反应机理:
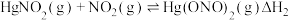

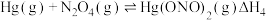
①根据盖斯定律,

②上述反应体系在一定条件下建立平衡后,下列说法正确的是
A.增大
 的浓度,可提高
的浓度,可提高 的平衡脱除率
的平衡脱除率B.升高温度,正反应速率增大,逆反应速率减小
C.恒温恒压下充入
 ,可提高原料的平衡转化率
,可提高原料的平衡转化率D.加入催化剂,可降低反应活化能,提高脱除速率
③在常压、温度范围为15~60℃条件下,将浓度为
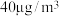 汞蒸气和
汞蒸气和 的
的 气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。
气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。
 的平均脱除反应速率为
的平均脱除反应速率为
ⅱ)

④富氧燃烧烟气中
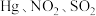 等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于
等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于 转化为
转化为 而脱除,但随着循环水量的增大,
而脱除,但随着循环水量的增大, 的去除率下降,其原因可能是
的去除率下降,其原因可能是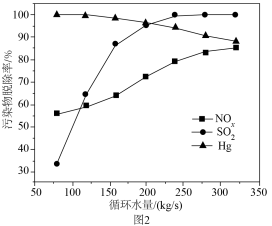
 溶液可用于手术刀消毒。
溶液可用于手术刀消毒。 与
与 的混合溶液中主要存在平衡:
的混合溶液中主要存在平衡:
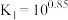
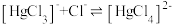
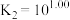
 的
的 溶液中加入
溶液中加入 固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数
固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数 随
随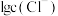 的变化如图所示
的变化如图所示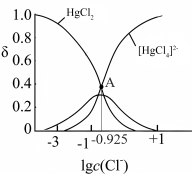
 ]。
]。①熔融状态的
 不能导电,
不能导电, 是
是②A点溶液中

 。
。③A点溶液中
 的转化率为
的转化率为
您最近一年使用:0次
7 .  是重要的化工原料,合理使用
是重要的化工原料,合理使用 能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
(1)已知下列反应的热化学方程式:
①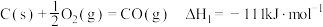
②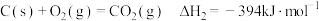
计算 燃烧生成
燃烧生成 反应③
反应③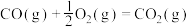 的
的
__________  。
。
(2)已知下列键能数据,结合反应③数据,计算 的键能是
的键能是____________  。
。
(3)650K时,某研究小组测得反应i: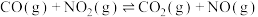 的浓度、速率数据如下:
的浓度、速率数据如下:
已知k为速率常数,一般情况下只与温度有关,实验测得
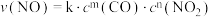 ,通过以上实验数据可知
,通过以上实验数据可知
_________ ,
_______ ;650K时,若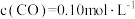 ,
,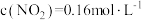 ,
,
________  。
。
(4)在上述实验过程中,同时发生了如下副反应ii: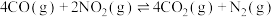 ,650K时,向容积为2L的密闭容器中通入
,650K时,向容积为2L的密闭容器中通入 和
和 ,10min 后体系达到平衡,此时
,10min 后体系达到平衡,此时 、
、 的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为
的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为____________ 。
(5)已知CO是常见配体,配位时简单认为1个CO提供2个电子,EAN规则认为金属的价电子数加上配体提供的电子数等于18时,配位化合物一般较稳定,下列结构能够稳定存在的有__________。
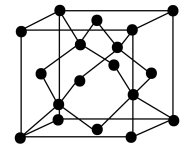
(6)CO可以用于生产多晶金刚石箔,将一氧化碳和氢气混合,在高温高压下通过催化剂使之沉积在金属基底上,形成金刚石晶体。金刚石的晶胞如图,晶胞参数为bnm,晶胞中C与C间的最大距离为__________ nm,晶体密度为____________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 是重要的化工原料,合理使用
是重要的化工原料,合理使用 能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
能发挥其在工业生产、物质合成、速率分析等领域的重要作用。(1)已知下列反应的热化学方程式:
①
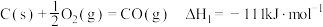
②
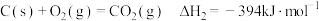
计算
 燃烧生成
燃烧生成 反应③
反应③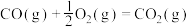 的
的
 。
。(2)已知下列键能数据,结合反应③数据,计算
 的键能是
的键能是 。
。化学键 |
|
|
键能 | 496 | 799 |
(3)650K时,某研究小组测得反应i:
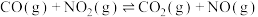 的浓度、速率数据如下:
的浓度、速率数据如下:实验编号 |
|
|
|
① | 0.025 | 0.040 |
|
② | 0.050 | 0.040 |
|
③ | 0.025 | 0.120 |
|
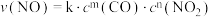 ,通过以上实验数据可知
,通过以上实验数据可知

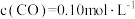 ,
,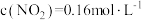 ,
,
 。
。(4)在上述实验过程中,同时发生了如下副反应ii:
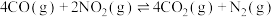 ,650K时,向容积为2L的密闭容器中通入
,650K时,向容积为2L的密闭容器中通入 和
和 ,10min 后体系达到平衡,此时
,10min 后体系达到平衡,此时 、
、 的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为
的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为(5)已知CO是常见配体,配位时简单认为1个CO提供2个电子,EAN规则认为金属的价电子数加上配体提供的电子数等于18时,配位化合物一般较稳定,下列结构能够稳定存在的有__________。
A.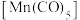 | B.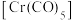 | C.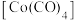 | D.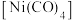 |
(6)CO可以用于生产多晶金刚石箔,将一氧化碳和氢气混合,在高温高压下通过催化剂使之沉积在金属基底上,形成金刚石晶体。金刚石的晶胞如图,晶胞参数为bnm,晶胞中C与C间的最大距离为
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
名校
8 . 在起始温度均为T℃.容积均为 的密闭容器A(恒温)、B(绝热)中均加入
的密闭容器A(恒温)、B(绝热)中均加入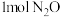 和
和 ,发生反应
,发生反应
 。已知:
。已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数,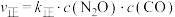 ,
,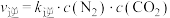 ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法中错误的是
的转化率随时间的变化关系如图所示。下列说法中错误的是
 的密闭容器A(恒温)、B(绝热)中均加入
的密闭容器A(恒温)、B(绝热)中均加入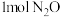 和
和 ,发生反应
,发生反应
 。已知:
。已知: 、
、 分别是正、逆反应速率常数,
分别是正、逆反应速率常数,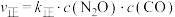 ,
,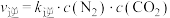 ,A、B容器中
,A、B容器中 的转化率随时间的变化关系如图所示。下列说法中错误的是
的转化率随时间的变化关系如图所示。下列说法中错误的是
A.曲线M、N的平衡常数大小为: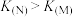 |
B. 与 与 浓度比为 浓度比为 且保持不变,不能说明反应达到平衡状态 且保持不变,不能说明反应达到平衡状态 |
C.T℃时,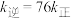 |
D.用CO的浓度变化表示曲线N在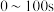 内的平均速率为 内的平均速率为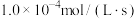 |
您最近一年使用:0次
解题方法
9 . T℃时,向容积为2L的刚性容器中充入1molCO2和一定量的H2发生反应:CO2(g)+2H2(g) HCHO(g)+H20(g),达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始
HCHO(g)+H20(g),达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始 的关系如图所示。已知:初始加入2molH2时,容器内气体的总压强为1.2pkPa。下列说法正确的是
的关系如图所示。已知:初始加入2molH2时,容器内气体的总压强为1.2pkPa。下列说法正确的是
 HCHO(g)+H20(g),达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始
HCHO(g)+H20(g),达到平衡时,HCHO的分压(分压=总压×物质的量分数)与起始 的关系如图所示。已知:初始加入2molH2时,容器内气体的总压强为1.2pkPa。下列说法正确的是
的关系如图所示。已知:初始加入2molH2时,容器内气体的总压强为1.2pkPa。下列说法正确的是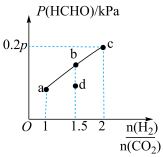
A.a点时反应的平衡常数Kp=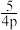 kPa-1 kPa-1 |
| B.d点:v正<v逆 |
| C.10min时反应到达c点,则0~10min用CO2表示的平均反应速率为0.05mol/(L·min) |
| D.c点时,再加入CO2(g)和H2O(g),使二者分压均增大0.1pkPa,平衡正向移动 |
您最近一年使用:0次
名校
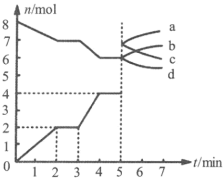
10 . 工业上生产CO的反应原理为
 。一定条件下,将足量焦炭和一定量
。一定条件下,将足量焦炭和一定量 放入体积为2L的恒容密闭容器中发生反应,
放入体积为2L的恒容密闭容器中发生反应, 和CO的物质的量n随时间t的变化关系如图。下列说法正确的是
和CO的物质的量n随时间t的变化关系如图。下列说法正确的是

 。一定条件下,将足量焦炭和一定量
。一定条件下,将足量焦炭和一定量 放入体积为2L的恒容密闭容器中发生反应,
放入体积为2L的恒容密闭容器中发生反应, 和CO的物质的量n随时间t的变化关系如图。下列说法正确的是
和CO的物质的量n随时间t的变化关系如图。下列说法正确的是
A.0~2min,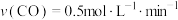 ;2~3min, ;2~3min, |
B.当容器内的气体密度( )不变时,反应一定达到平衡状态,且 )不变时,反应一定达到平衡状态,且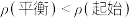 |
C.3min时温度由 升高到 升高到 ,则 ,则 ,平衡常数 ,平衡常数 |
D.5min时再充入一定量的CO,a、d曲线分别表示 、 、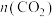 的变化 的变化 |
您最近一年使用:0次
2024-01-13更新
|
410次组卷
|
3卷引用:辽宁省锦州市2023-2024学年高三上学期1月期末化学试题
辽宁省锦州市2023-2024学年高三上学期1月期末化学试题(已下线)题型12 化学平衡图表分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)山东省青岛第五十八中学2023-2024学年高二下学期期初考试化学试卷