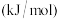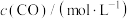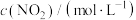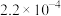名校
解题方法
1 .  催化加氢有利于实现碳的循环利用,在催化剂的作用下可发生如下反应:
催化加氢有利于实现碳的循环利用,在催化剂的作用下可发生如下反应:
① ;
;
② ;
;
③ 。
。
回答下列问题:
(1)已知相关化学键键能如表所示:
根据表中键能数据计算出
_______  (用字母表示)。
(用字母表示)。
(2)已知反应③的速率方程为 、
、 ,其中
,其中 、
、 分别为正、逆反应的速率常数。
分别为正、逆反应的速率常数。
①如图所示( 表示速率常数的对数,
表示速率常数的对数, 表示温度的倒数)
表示温度的倒数) 、
、 、
、 、
、 四条斜线中有两条分别表示
四条斜线中有两条分别表示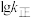 、
、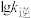 随
随 的变化关系曲线,其中能表示
的变化关系曲线,其中能表示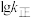 随
随 变化关系的是斜线
变化关系的是斜线_______ (填图中字母)。 减小的是
减小的是_______ (填选项字母)。
A.减小压强 B.减小温度 C.减小 的浓度 D.更换成负催化剂
的浓度 D.更换成负催化剂
(3)在 恒温恒容有某催化剂的密闭容器中充入
恒温恒容有某催化剂的密闭容器中充入 和
和 ,发生上述三个反应。该温度下反应均达平衡时,测得
,发生上述三个反应。该温度下反应均达平衡时,测得 为
为 、
、 为
为 、
、 为
为 ,则
,则 的选择性为
的选择性为
_______ ( 选择性=
选择性= );反应②的平衡常数为
);反应②的平衡常数为_______ (列出计算式即可)。
(4)若测得上述三个反应在不同温度下 的平衡转化率和甲醇的选择性如图所示:
的平衡转化率和甲醇的选择性如图所示:_______ (填选项字母)。
A.400℃ B.600℃ C.800℃ D.1000℃
高于800℃时, 转化率增大的主要原因是
转化率增大的主要原因是_______ 。
 催化加氢有利于实现碳的循环利用,在催化剂的作用下可发生如下反应:
催化加氢有利于实现碳的循环利用,在催化剂的作用下可发生如下反应:①
 ;
;②
 ;
;③
 。
。回答下列问题:
(1)已知相关化学键键能如表所示:
化学键 |
|
|
|
|
|
键能 | a | b | c | d | e |

 (用字母表示)。
(用字母表示)。(2)已知反应③的速率方程为
 、
、 ,其中
,其中 、
、 分别为正、逆反应的速率常数。
分别为正、逆反应的速率常数。①如图所示(
 表示速率常数的对数,
表示速率常数的对数, 表示温度的倒数)
表示温度的倒数) 、
、 、
、 、
、 四条斜线中有两条分别表示
四条斜线中有两条分别表示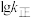 、
、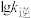 随
随 的变化关系曲线,其中能表示
的变化关系曲线,其中能表示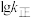 随
随 变化关系的是斜线
变化关系的是斜线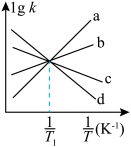
 减小的是
减小的是A.减小压强 B.减小温度 C.减小
 的浓度 D.更换成负催化剂
的浓度 D.更换成负催化剂(3)在
 恒温恒容有某催化剂的密闭容器中充入
恒温恒容有某催化剂的密闭容器中充入 和
和 ,发生上述三个反应。该温度下反应均达平衡时,测得
,发生上述三个反应。该温度下反应均达平衡时,测得 为
为 、
、 为
为 、
、 为
为 ,则
,则 的选择性为
的选择性为
 选择性=
选择性= );反应②的平衡常数为
);反应②的平衡常数为(4)若测得上述三个反应在不同温度下
 的平衡转化率和甲醇的选择性如图所示:
的平衡转化率和甲醇的选择性如图所示:
A.400℃ B.600℃ C.800℃ D.1000℃
高于800℃时,
 转化率增大的主要原因是
转化率增大的主要原因是
您最近一年使用:0次
名校
解题方法
2 . 在恒温恒压下,向密闭容器中充入4mol  和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是
 和2mol
和2mol  ,发生如下反应:
,发生如下反应: △H<0,2min后,反应达到平衡,生成
△H<0,2min后,反应达到平衡,生成 为1.4mol,同时放出热量Q kJ。则下列分析正确的是
为1.4mol,同时放出热量Q kJ。则下列分析正确的是A.若反应开始时容器体积为2L,则 |
B.若把条件“恒温恒压”改为“恒压恒容”,则平衡后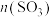 大于1.4mol 大于1.4mol |
C.2min后,向容器中再通入一定量的 气体,重新达到平衡时 气体,重新达到平衡时 的含量变小 的含量变小 |
| D.若把条件“恒温恒压”改为“恒温恒容”,则平衡时放出热量小于Q kJ |
您最近一年使用:0次
23-24高三下·上海·开学考试
名校
3 . Ⅰ.亚硫酰氯( )又称氯化亚砜,沸点
)又称氯化亚砜,沸点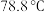 ,遇水强烈水解,是一种重要的脱水剂。
,遇水强烈水解,是一种重要的脱水剂。
(1) 属于___________。
属于___________。
(2)已知 分子中S为中心原子,其中心原子的杂化方式和分子结构分别为___________。
分子中S为中心原子,其中心原子的杂化方式和分子结构分别为___________。
(3) 的两种水解产物均是有刺激性气味的气体,其中一种产物属于强电解质。写出该产物分子的电子式
的两种水解产物均是有刺激性气味的气体,其中一种产物属于强电解质。写出该产物分子的电子式___________ 。检验另一产物的实验方法为___________ 。
(4) 作脱水剂时可使含结晶水的盐变成无水盐。设计简单实验证明其脱水性
作脱水剂时可使含结晶水的盐变成无水盐。设计简单实验证明其脱水性___________ 。
Ⅱ.工业上利用尾气 与
与 、反应合成氯化亚砜。发生如下反应:
、反应合成氯化亚砜。发生如下反应:
 反应①
反应①
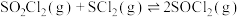 反应②
反应②
 时,在
时,在 密闭容器中,充入一定量的、
密闭容器中,充入一定量的、 和
和 ,测得初始压强为p0,反应过程中容器内总压强(p)随时间(t)变化如下图所示,起始各组分及达平衡时
,测得初始压强为p0,反应过程中容器内总压强(p)随时间(t)变化如下图所示,起始各组分及达平衡时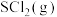 的物质的量如下表。
的物质的量如下表。
(5) 内,二氯亚砜的平均反应速率
内,二氯亚砜的平均反应速率
___________  。
。 时
时 的转化率为
的转化率为___________ 。
(6) 时,上述反应②的
时,上述反应②的
___________ 。
 )又称氯化亚砜,沸点
)又称氯化亚砜,沸点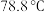 ,遇水强烈水解,是一种重要的脱水剂。
,遇水强烈水解,是一种重要的脱水剂。(1)
 属于___________。
属于___________。| A.分子晶体 | B.离子晶体 | C.共价晶体 | D.金属晶体 |
 分子中S为中心原子,其中心原子的杂化方式和分子结构分别为___________。
分子中S为中心原子,其中心原子的杂化方式和分子结构分别为___________。A. ,角形 ,角形 | B. ,三角锥形 ,三角锥形 |
C. ,平面三角形 ,平面三角形 | D. ,四面体形 ,四面体形 |
 的两种水解产物均是有刺激性气味的气体,其中一种产物属于强电解质。写出该产物分子的电子式
的两种水解产物均是有刺激性气味的气体,其中一种产物属于强电解质。写出该产物分子的电子式(4)
 作脱水剂时可使含结晶水的盐变成无水盐。设计简单实验证明其脱水性
作脱水剂时可使含结晶水的盐变成无水盐。设计简单实验证明其脱水性Ⅱ.工业上利用尾气
 与
与 、反应合成氯化亚砜。发生如下反应:
、反应合成氯化亚砜。发生如下反应: 反应①
反应①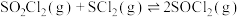 反应②
反应② 时,在
时,在 密闭容器中,充入一定量的、
密闭容器中,充入一定量的、 和
和 ,测得初始压强为p0,反应过程中容器内总压强(p)随时间(t)变化如下图所示,起始各组分及达平衡时
,测得初始压强为p0,反应过程中容器内总压强(p)随时间(t)变化如下图所示,起始各组分及达平衡时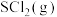 的物质的量如下表。
的物质的量如下表。
| 物质 |  |  | 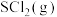 | 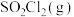 |  |
起始 |  |  |  | 0 | 0 |
平衡 | 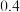 |
 内,二氯亚砜的平均反应速率
内,二氯亚砜的平均反应速率
 。
。 时
时 的转化率为
的转化率为(6)
 时,上述反应②的
时,上述反应②的
您最近一年使用:0次
名校
解题方法
4 . 利用甲醇 催化脱氢法制备甲酸甲酯
催化脱氢法制备甲酸甲酯 涉及到如下化学反应:
涉及到如下化学反应:
反应Ⅰ: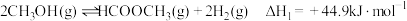
反应Ⅱ: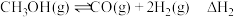
反应Ⅲ:
回答下列问题:
(1)
___________  。
。
(2) ,向密闭容器中通入
,向密闭容器中通入 ,恒压条件下进行反应Ⅰ。
,恒压条件下进行反应Ⅰ。
①下列有关说法正确是___________ (填标号)。
A.高温有利于反应Ⅰ自发
B. 说明该反应体系达到平衡状态
说明该反应体系达到平衡状态
C.温度升高有利于提高 的转化率
的转化率
D.通过减小 分压可以提高
分压可以提高 的平衡产率
的平衡产率
②要缩短达到平衡的时间,可采取的措施有___________ 。
③ ,测得体系中反应Ⅰ的平衡转化率和进料时甲醇的分压
,测得体系中反应Ⅰ的平衡转化率和进料时甲醇的分压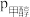 (分压=总压×物质的量分数)关系如图.M点
(分压=总压×物质的量分数)关系如图.M点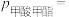
___________  ;该反应的平衡常数
;该反应的平衡常数
___________  (
( 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。 上高度分散的铜颗粒催化剂
上高度分散的铜颗粒催化剂 制备方法如下.
制备方法如下.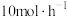 的流速通过负载
的流速通过负载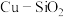 的催化反应器,甲醇转化率和甲酸甲酯选择性随
的催化反应器,甲醇转化率和甲酸甲酯选择性随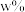 、反应温度的变化如图.
、反应温度的变化如图. 时,生成甲酸甲酯的反应速率为
时,生成甲酸甲酯的反应速率为___________ 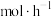 。
。
②最适合的反应温度为___________ (填标号)。
A.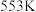 B.
B. C.
C. D.
D.
③图2中当温度高于 时,甲酸甲酯选择性下降的可能原因为
时,甲酸甲酯选择性下降的可能原因为___________ 。
 催化脱氢法制备甲酸甲酯
催化脱氢法制备甲酸甲酯 涉及到如下化学反应:
涉及到如下化学反应:反应Ⅰ:
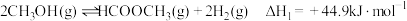
反应Ⅱ:
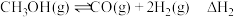
反应Ⅲ:

回答下列问题:
(1)

 。
。(2)
 ,向密闭容器中通入
,向密闭容器中通入 ,恒压条件下进行反应Ⅰ。
,恒压条件下进行反应Ⅰ。①下列有关说法正确是
A.高温有利于反应Ⅰ自发
B.
 说明该反应体系达到平衡状态
说明该反应体系达到平衡状态C.温度升高有利于提高
 的转化率
的转化率D.通过减小
 分压可以提高
分压可以提高 的平衡产率
的平衡产率②要缩短达到平衡的时间,可采取的措施有
③
 ,测得体系中反应Ⅰ的平衡转化率和进料时甲醇的分压
,测得体系中反应Ⅰ的平衡转化率和进料时甲醇的分压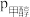 (分压=总压×物质的量分数)关系如图.M点
(分压=总压×物质的量分数)关系如图.M点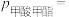
 ;该反应的平衡常数
;该反应的平衡常数
 (
( 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。
 上高度分散的铜颗粒催化剂
上高度分散的铜颗粒催化剂 制备方法如下.
制备方法如下.
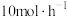 的流速通过负载
的流速通过负载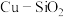 的催化反应器,甲醇转化率和甲酸甲酯选择性随
的催化反应器,甲醇转化率和甲酸甲酯选择性随 、反应温度的变化如图.
、反应温度的变化如图.
 时,生成甲酸甲酯的反应速率为
时,生成甲酸甲酯的反应速率为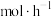 。
。②最适合的反应温度为
A.
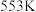 B.
B. C.
C. D.
D.
③图2中当温度高于
 时,甲酸甲酯选择性下降的可能原因为
时,甲酸甲酯选择性下降的可能原因为
您最近一年使用:0次
2024-02-27更新
|
136次组卷
|
3卷引用:安徽省芜湖市安徽师范大学附属中学2023-2024学年高二下学期2月月考化学试题
5 .  是重要的化工原料,合理使用
是重要的化工原料,合理使用 能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
(1)已知下列反应的热化学方程式:
①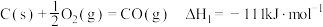
②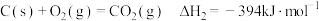
计算 燃烧生成
燃烧生成 反应③
反应③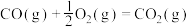 的
的
__________  。
。
(2)已知下列键能数据,结合反应③数据,计算 的键能是
的键能是____________  。
。
(3)650K时,某研究小组测得反应i: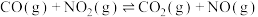 的浓度、速率数据如下:
的浓度、速率数据如下:
已知k为速率常数,一般情况下只与温度有关,实验测得
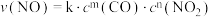 ,通过以上实验数据可知
,通过以上实验数据可知
_________ ,
_______ ;650K时,若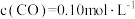 ,
,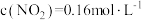 ,
,
________  。
。
(4)在上述实验过程中,同时发生了如下副反应ii: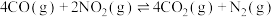 ,650K时,向容积为2L的密闭容器中通入
,650K时,向容积为2L的密闭容器中通入 和
和 ,10min 后体系达到平衡,此时
,10min 后体系达到平衡,此时 、
、 的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为
的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为____________ 。
(5)已知CO是常见配体,配位时简单认为1个CO提供2个电子,EAN规则认为金属的价电子数加上配体提供的电子数等于18时,配位化合物一般较稳定,下列结构能够稳定存在的有__________。
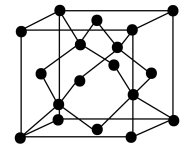
(6)CO可以用于生产多晶金刚石箔,将一氧化碳和氢气混合,在高温高压下通过催化剂使之沉积在金属基底上,形成金刚石晶体。金刚石的晶胞如图,晶胞参数为bnm,晶胞中C与C间的最大距离为__________ nm,晶体密度为____________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 是重要的化工原料,合理使用
是重要的化工原料,合理使用 能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
能发挥其在工业生产、物质合成、速率分析等领域的重要作用。(1)已知下列反应的热化学方程式:
①
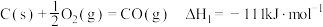
②
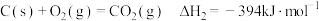
计算
 燃烧生成
燃烧生成 反应③
反应③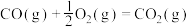 的
的
 。
。(2)已知下列键能数据,结合反应③数据,计算
 的键能是
的键能是 。
。化学键 |
|
|
键能 | 496 | 799 |
(3)650K时,某研究小组测得反应i:
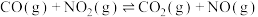 的浓度、速率数据如下:
的浓度、速率数据如下:实验编号 |
|
|
|
① | 0.025 | 0.040 |
|
② | 0.050 | 0.040 |
|
③ | 0.025 | 0.120 |
|
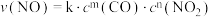 ,通过以上实验数据可知
,通过以上实验数据可知

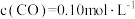 ,
,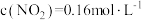 ,
,
 。
。(4)在上述实验过程中,同时发生了如下副反应ii:
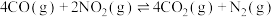 ,650K时,向容积为2L的密闭容器中通入
,650K时,向容积为2L的密闭容器中通入 和
和 ,10min 后体系达到平衡,此时
,10min 后体系达到平衡,此时 、
、 的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为
的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为(5)已知CO是常见配体,配位时简单认为1个CO提供2个电子,EAN规则认为金属的价电子数加上配体提供的电子数等于18时,配位化合物一般较稳定,下列结构能够稳定存在的有__________。
A.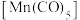 | B.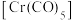 | C.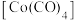 | D.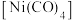 |
(6)CO可以用于生产多晶金刚石箔,将一氧化碳和氢气混合,在高温高压下通过催化剂使之沉积在金属基底上,形成金刚石晶体。金刚石的晶胞如图,晶胞参数为bnm,晶胞中C与C间的最大距离为
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
名校
解题方法
6 . 将 和
和 重整转化为合成气一直是减少温室气体排放的研究方向之一,涉及如下反应:
重整转化为合成气一直是减少温室气体排放的研究方向之一,涉及如下反应:
主反应:

副反应: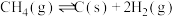
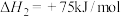
回答下列问题:
(1)已知: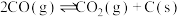
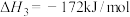 ,则
,则
_______  。
。
(2)恒温恒容密闭容器中仅发生主反应,能说明反应达到平衡状态的是_______(填标号)。
(3)在体积为 恒容密闭容器中充入
恒容密闭容器中充入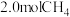 和
和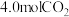 ,
, 下仅发生主反应,
下仅发生主反应, 、
、 的物质的量随时间变化如下表所示:
的物质的量随时间变化如下表所示:
① 在
在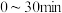 内的平均反应速率
内的平均反应速率
_______ 。
②若在 时再充入
时再充入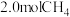 ,达到新平衡后
,达到新平衡后 的转化率
的转化率_______ (填“增大”、“减小”或“不变”,下同),此时平衡常数
_______ 。
③若相同条件下改为充入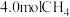 和
和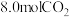 反应,平衡后
反应,平衡后 的转化率
的转化率_______  (填“<”、“=”或“>”)。
(填“<”、“=”或“>”)。
(4) 催化加
催化加 可以制备
可以制备 ,保持反应气中
,保持反应气中 与
与 的体积比为
的体积比为 ,以
,以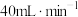 的流速通过催化剂,甲烷化过程中,含碳产物
的流速通过催化剂,甲烷化过程中,含碳产物 的物质的量百分数
的物质的量百分数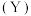 及
及 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。 时
时 反应速率为
反应速率为_______  。
。

 和
和 重整转化为合成气一直是减少温室气体排放的研究方向之一,涉及如下反应:
重整转化为合成气一直是减少温室气体排放的研究方向之一,涉及如下反应:主反应:


副反应:
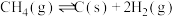
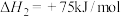
回答下列问题:
(1)已知:
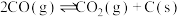
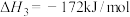 ,则
,则
 。
。(2)恒温恒容密闭容器中仅发生主反应,能说明反应达到平衡状态的是_______(填标号)。
| A.容器内的压强不变 |
B. |
| C.混合气体的密度不再变化 |
D.断开 键同时断开 键同时断开 键 键 |
(3)在体积为
 恒容密闭容器中充入
恒容密闭容器中充入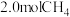 和
和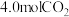 ,
, 下仅发生主反应,
下仅发生主反应, 、
、 的物质的量随时间变化如下表所示:
的物质的量随时间变化如下表所示:时间/min 反应物 | 0 | 15 | 30 | 45 | 60 | 75 |
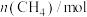 | 2.0 | 1.3 | 0.8 | 0.4 | 0.2 | 0.2 |
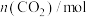 | 4.0 | 3.3 | 2.8 | 2.4 | 2.2 | 2.2 |
 在
在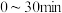 内的平均反应速率
内的平均反应速率
②若在
 时再充入
时再充入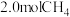 ,达到新平衡后
,达到新平衡后 的转化率
的转化率
③若相同条件下改为充入
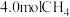 和
和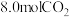 反应,平衡后
反应,平衡后 的转化率
的转化率 (填“<”、“=”或“>”)。
(填“<”、“=”或“>”)。(4)
 催化加
催化加 可以制备
可以制备 ,保持反应气中
,保持反应气中 与
与 的体积比为
的体积比为 ,以
,以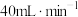 的流速通过催化剂,甲烷化过程中,含碳产物
的流速通过催化剂,甲烷化过程中,含碳产物 的物质的量百分数
的物质的量百分数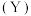 及
及 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。 时
时 反应速率为
反应速率为 。
。
您最近一年使用:0次
名校
解题方法
7 . 甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都有着重要的用途和应用前景。工业上用 和
和 反应生产甲醇、乙醇。回答下列问题:
反应生产甲醇、乙醇。回答下列问题:
(1)已知: 的燃烧热为285.8
的燃烧热为285.8 ,
, (l)的燃烧热为725.8
(l)的燃烧热为725.8 ,
,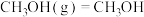
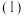
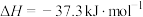 ,则
,则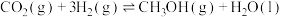

______  。
。
(2)为探究用 生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1mol
生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1mol 和3.25mol
和3.25mol 在一定条件下发生反应,测得
在一定条件下发生反应,测得 、
、 (g)和
(g)和 (g)的物质的量(n)随时间的变化如图1所示:
(g)的物质的量(n)随时间的变化如图1所示:
______ ( 。
。
②下列措施能使 的平衡转化率增大的是
的平衡转化率增大的是______ (填字母)。
A.在原容器中再充入1mol B.在原容器中再充入1mol
B.在原容器中再充入1mol
C.在原容器中充入1mol氦气 D.使用更有效的催化剂
(3) 也可通过催化加氢合成乙醇,其反应原理为
也可通过催化加氢合成乙醇,其反应原理为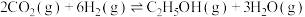 △H<0.设m为起始时的投料比,即
△H<0.设m为起始时的投料比,即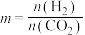 。通过实验得到如图2所示图像:
。通过实验得到如图2所示图像:______ 。
②乙中 、
、 、
、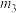 从大到小的顺序为
从大到小的顺序为______ 。
③丙表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系,曲线a表示的物质是______ (填化学式), 温度时,该反应压强平衡常数
温度时,该反应压强平衡常数 的计算式为
的计算式为____________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,代入数据,不用计算)。
 和
和 反应生产甲醇、乙醇。回答下列问题:
反应生产甲醇、乙醇。回答下列问题:(1)已知:
 的燃烧热为285.8
的燃烧热为285.8 ,
, (l)的燃烧热为725.8
(l)的燃烧热为725.8 ,
,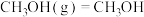
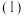
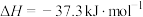 ,则
,则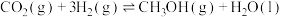

 。
。(2)为探究用
 生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1mol
生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1mol 和3.25mol
和3.25mol 在一定条件下发生反应,测得
在一定条件下发生反应,测得 、
、 (g)和
(g)和 (g)的物质的量(n)随时间的变化如图1所示:
(g)的物质的量(n)随时间的变化如图1所示:

 。
。②下列措施能使
 的平衡转化率增大的是
的平衡转化率增大的是A.在原容器中再充入1mol
 B.在原容器中再充入1mol
B.在原容器中再充入1mol
C.在原容器中充入1mol氦气 D.使用更有效的催化剂
(3)
 也可通过催化加氢合成乙醇,其反应原理为
也可通过催化加氢合成乙醇,其反应原理为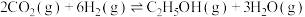 △H<0.设m为起始时的投料比,即
△H<0.设m为起始时的投料比,即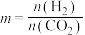 。通过实验得到如图2所示图像:
。通过实验得到如图2所示图像: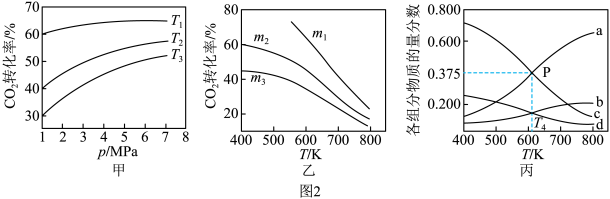
②乙中
 、
、 、
、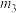 从大到小的顺序为
从大到小的顺序为③丙表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系,曲线a表示的物质是
 温度时,该反应压强平衡常数
温度时,该反应压强平衡常数 的计算式为
的计算式为
您最近一年使用:0次
2024-01-09更新
|
147次组卷
|
2卷引用:安徽省合肥市一中2023-2024学年高三上学期第二次教学质量检测化学试题
名校
解题方法
8 . 某温度下,在2L恒容密闭容器中4.0molX发生反应 ,有关数据如下:
,有关数据如下:
下列说法正确的是
 ,有关数据如下:
,有关数据如下:| 时间段/min | 产物Z的平均生成速率/ |
| 0~2 | 0.20 |
| 0~4 | 0.15 |
| 0~6 | 0.10 |
A.0~2min内,X平均反应速率为 |
B.2min时,加入0.40molZ,此时 |
| C.当Z的气体体积分数约为66.7%,说明反应一定处于平衡状态 |
| D.5min时,Y的物质的量为0.3mol |
您最近一年使用:0次
名校
解题方法
9 . 恒温恒容的密闭容器中,某催化剂表面发生氨的分解反应: ,测得不同起始浓度和催化剂表面积下氨的浓度随时间的变化
,测得不同起始浓度和催化剂表面积下氨的浓度随时间的变化
下列说法不正确的是
 ,测得不同起始浓度和催化剂表面积下氨的浓度随时间的变化
,测得不同起始浓度和催化剂表面积下氨的浓度随时间的变化| 编号 | 时间/min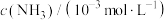 表面积/cm  | 0 | 20 | 40 | 60 | 80 |
| ① | a | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| ② | a | 1.20 | 0.80 | 0.40 | x | |
| ③ | 2a | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
A.实验①,0∼40min,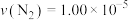 mol⋅L mol⋅L ∙min ∙min |
| B.相同条件下,增加氨气的浓度,反应速率增大 |
| C.相同条件下,增加催化剂的表面积,反应速率增大 |
D.实验②,60min时处于平衡状态, |
您最近一年使用:0次
2023-11-23更新
|
79次组卷
|
31卷引用:安徽省合肥一六八中学2022-2023学年高二上学期化学学科学情调研试题
安徽省合肥一六八中学2022-2023学年高二上学期化学学科学情调研试题安徽省六安第一中学2022-2023学年高二上学期期末考试化学试题安徽省淮北市树人高级中学2023-2024学年高二下学期开学考试化学试题(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)黑龙江省双鸭山市第一中学2021-2022学年高一下学期期末考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高一下学期期末考试化学试题(已下线)第16练 化学反应的速率与限度-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第20讲 化学反应速率(练)-2023年高考化学一轮复习讲练测(全国通用)浙江省浙里卷天下2022-2023学年高三8月开学测试化学试题江西省新余市第一中学2022-2023学年高二上学期开学考试化学试题辽宁省朝阳市建平县实验中学2022-2023学年高二上学期第一次月考化学试题(已下线)第19讲 化学平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题(已下线)易错点22 化学反应平衡和移动-备战2023年高考化学考试易错题天津市五校(杨村宝坻蓟州芦台静海一中)2022-2023学年高二上学期期中考试化学试题黑龙江省佳木斯市第一中学2022-2023学年高三上学期第三次调研化学试题(已下线)2023年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷A(已下线)化学预测卷(五)-预测卷(浙江专版)(已下线)专题09 化学反应速率与化学平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)辽宁省营口市2022-2023学年高三上学期期末考试化学试题上海市奉贤区2022-2023学年高三上学期一模练习卷化学试题(已下线)第13练 化学反应速率与化学平衡的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点21 化学反应速率(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)第二章 章末训练(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)河南省周口恒大中学2023-2024学年高二上学期11月期中考试化学试题北京师范大学附属中学2022-2023学年高二上学期10月月考化学试题吉林省长春市第二实验中学2023-2024学年高二上学期10月月考化学试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)上海市建平世纪中学2023-2024学年高二上学期阶段练习二 化学(等级)试题
解题方法
10 . “碳中和”是国家战略目标,其目的是实现 的排放量和利用量达到相等,将
的排放量和利用量达到相等,将 资源化是实现“碳中和”目标的重要手段。回答下列问题:
资源化是实现“碳中和”目标的重要手段。回答下列问题:
(1)下列措施有利于“碳中和”的是___________(填标号)。
(2) 和
和 在催化剂作用下发生反应可合成清洁能源甲醇:
在催化剂作用下发生反应可合成清洁能源甲醇: 。
。
①断开(或形成) 化学键的能量变化数据如表中所示,该反应每生成
化学键的能量变化数据如表中所示,该反应每生成 甲醇,需要
甲醇,需要___________ (填“吸收”或“放出”)___________  的热量。
的热量。
②已知该反应的正反应速率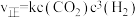 (k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中a=
(k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中a=___________ 。
(3)若 和
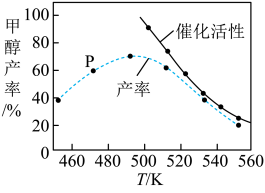
和 按一定比例反应
按一定比例反应 ,一定时间内甲醇的产率和催化剂的催化活性与温度的关系如图所示。当温度为470K时,图中P点
,一定时间内甲醇的产率和催化剂的催化活性与温度的关系如图所示。当温度为470K时,图中P点___________ (填“是”或“不是”)处于平衡状态,说出理由:___________ ;490K之后,甲醇产率下降,请分析其变化产生的原因:___________ 。
 的排放量和利用量达到相等,将
的排放量和利用量达到相等,将 资源化是实现“碳中和”目标的重要手段。回答下列问题:
资源化是实现“碳中和”目标的重要手段。回答下列问题:(1)下列措施有利于“碳中和”的是___________(填标号)。
| A.植树造林,发展绿色经济 | B.通过裂化将重油转化为汽油 |
C.在燃煤中添加 或 或 | D.大力开采和使用可燃冰 |
 和
和 在催化剂作用下发生反应可合成清洁能源甲醇:
在催化剂作用下发生反应可合成清洁能源甲醇: 。
。①断开(或形成)
 化学键的能量变化数据如表中所示,该反应每生成
化学键的能量变化数据如表中所示,该反应每生成 甲醇,需要
甲醇,需要 的热量。
的热量。| 化学键 | H-H | C-O | C=O | O-H | C-H |
键能/ | 436 | 326 | 803 | 464 | 414 |
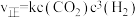 (k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中a=
(k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中a=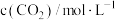 | 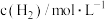 | 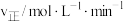 | |
| 1 | 0.02 | 0.01 |  |
| 2 | 0.02 | 0.02 | a |
 和
和 按一定比例反应
按一定比例反应 ,一定时间内甲醇的产率和催化剂的催化活性与温度的关系如图所示。当温度为470K时,图中P点
,一定时间内甲醇的产率和催化剂的催化活性与温度的关系如图所示。当温度为470K时,图中P点
您最近一年使用:0次