名校
1 . 对于反应2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是
 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是| A.反应的ΔS>0 |
B.反应的平衡常数可表示为K= |
| C.增大体系的压强能提高SO2的反应速率和转化率 |
| D.使用催化剂能改变反应路径,提高反应的活化能 |
您最近一年使用:0次
2021-10-18更新
|
599次组卷
|
7卷引用:湖北省新高考联考协作体2021-2022学年高二3月考试化学试题
湖北省新高考联考协作体2021-2022学年高二3月考试化学试题江苏省徐州市第三中学2021-2022学年高二上学期10月月考化学试题湖南省衡阳市田家炳实验中学2021-2022学年高二上学期期中考试化学试题黑龙江省佳木斯市实验中学2021-2022学年高二上学期期末考试化学试题江苏省南通市通州区金沙中学2021-2022学年高二上学期第二次调研考试化学试题(已下线)专题06 化学反应的方向及调控【考点清单】(讲+练)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)广西百色市德保高中2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
2 . 下列反应在任何温度下均能自发进行的是
A. △H<0 △H<0 |
B.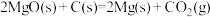 △H>0 △H>0 |
C. △H<0 △H<0 |
D.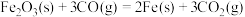 △H>0 △H>0 |
您最近一年使用:0次
2021-09-20更新
|
628次组卷
|
7卷引用:湖北省黄冈市麻城二中2021-2022学年高二上学期10月月考化学试题
湖北省黄冈市麻城二中2021-2022学年高二上学期10月月考化学试题浙江省嘉兴市2022届高三上学期9月基础测试化学试题(已下线)2022年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷B云南昆明师范专科学校附属中学2021-2022学年高二上学期期中考试化学试题(已下线)解密09 化学反应速率与化学平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)一轮巩固卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(浙江专用)浙江省宁波效实中学2022-2023学年高一下学期期中考试化学(选考班)试题
14-15高二上·山西·期中
名校
3 . 闪电时空气中的N2和O2会发生反应:N2(g)+2O2(g)=2NO2(g) ΔH=+180.50 kJ·mol-1,ΔS=247.3 J·mol-1·K-1,若不考虑温度对该反应焓变的影响,则下列说法中正确的是
| A.在1 000 ℃时,此反应能自发进行 |
| B.在1 000 ℃时,此反应不能自发进行 |
| C.该反应能自发进行的最低温度约为730℃ |
| D.该反应能自发进行的最高温度约为730 K |
您最近一年使用:0次
2021-08-25更新
|
781次组卷
|
13卷引用:湖北省恩施咸丰春晖学校2021-2022学年高二上学期第一次月考化学试题
湖北省恩施咸丰春晖学校2021-2022学年高二上学期第一次月考化学试题(已下线)2014-2015学年山西省山大附中高二上学期期中化学试卷湖南省浏阳一中、醴陵一中、南方中学2017-2018学年高二12月联考化学试题湖南省浏阳一中、醴陵一中、南方中学2017-2018学年高二12月联考化学试题(实验班)山西省平遥中学2017-2018学年高二上学期期中考试化学试题(已下线)2.3 化学反应的方向-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)2.2.1 化学反应的方向-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题(已下线)必考点04 化学反应的方向和调控-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)(已下线)2.1 化学反应的方向-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第2章能力提升测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)甘肃省兰州第一中学2022-2023学年高二上学期期中考试化学试题上海市上海中学2022-2023学年高一下学期期末考试化学试题
4 . 某反应过程中的能量变化如图所示。下列叙述正确的是
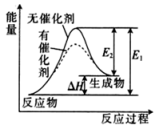

A.该反应的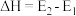 |
| B.该反应的能量变化与合成氨反应的能量变化相同 |
C.加入催化剂既能减小反应的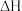 ,又能加快反应速率 ,又能加快反应速率 |
D.若该反应常温下能自发进行,则反应的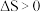 |
您最近一年使用:0次
2021-08-25更新
|
293次组卷
|
3卷引用:湖北省公安县第三中学2020-2021学年高三上学期10月月考化学试题
湖北省公安县第三中学2020-2021学年高三上学期10月月考化学试题湖北省阳新高中2021-2022学年高二上学期9月月考化学试题(已下线)2.2.1 化学反应的方向-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)
5 . 氮气是空气的重要组成气体,氮气的综合利用在农业和国防中有着重要意义。
(1)合成氨从实验室研究到实现工业生产,大约经历了150 年。
①写出工业合成氨的化学方程式___________
②已知该反应的ΔH= -92.4 kJ/mol, ΔS (T =298K) =- 198.76 J·mol -1·K-1,试判断室温(即298K) 下,合成氨的反应能否自发进行?___________ (填“能”或“否”)
(2) NH3和CO2在120 °C,催化剂作用下可以合成尿素。
①写出该反应的化学方程式___________
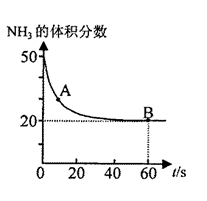
②混合气体中NH3 的含量变化关系如图所示(该条件下尿素为固体)。则A点的正反应速率v正 (CO2)___________ B点的逆反应速率为v逆(CO2) (填“大于”、“小于”或“等于”),NH3的平衡转化率为___________
(3) NH3可用工业上生产硝酸,其尾气中的NO2可用氨水吸收生成NH4NO3.25 °C时,将a mol NH4NO3溶于水,溶液显酸性,其原因是___________ (用离子方程式表示)向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将___________ (填 “正向”、“不”或“逆向”移动,所滴加氨水的浓度为___________ mol·L-1(25 °C时,NH3·H2O 的电离平衡常数取Kb= 2 ×10-5 mol·L-1)
(1)合成氨从实验室研究到实现工业生产,大约经历了150 年。
①写出工业合成氨的化学方程式
②已知该反应的ΔH= -92.4 kJ/mol, ΔS (T =298K) =- 198.76 J·mol -1·K-1,试判断室温(即298K) 下,合成氨的反应能否自发进行?
(2) NH3和CO2在120 °C,催化剂作用下可以合成尿素。
①写出该反应的化学方程式
②混合气体中NH3 的含量变化关系如图所示(该条件下尿素为固体)。则A点的正反应速率v正 (CO2)

(3) NH3可用工业上生产硝酸,其尾气中的NO2可用氨水吸收生成NH4NO3.25 °C时,将a mol NH4NO3溶于水,溶液显酸性,其原因是
您最近一年使用:0次
名校
6 . 关于反应CH3COOH(l)+C2H5OH(l) ⇌CH3COOC2H5(l)+H2O(1) ΔH=-2.7 kJ mol-1,下列说法正确的是
mol-1,下列说法正确的是
 mol-1,下列说法正确的是
mol-1,下列说法正确的是| A.因为化学反应方程式前后物质的化学计量数之和相等,所以反应的ΔS等于0 |
| B.加入高效吸水剂有利于平衡正向移动,该反应平衡常数增大 |
C.该反应的平衡常数为:K= |
| D.因为反应的ΔH接近于0,所以温度变化对平衡转化率的影响不大 |
您最近一年使用:0次
2021-05-24更新
|
437次组卷
|
7卷引用:湖北省罗田县第一中学2020-2021学年高二下学期第一次月考化学试题
湖北省罗田县第一中学2020-2021学年高二下学期第一次月考化学试题浙江省名校协作体2021届高三下学期开学联考化学试题(已下线)【浙江新东方】高中化学20210513-013【2021】【高二下】(已下线)【浙江新东方】双师274高二下(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)
解题方法
7 . 根据反应情况不同,反应热可分为多种,例如燃烧热、中和热、溶解热等,下列关于燃烧热的说法不正确的是
| A.已知:S(s)+O2 (g)=SO2 (g) ΔH1=—Q1 kJ•mol-1,S(g)+O2 (g)=SO2 (g) ΔH2=—Q2 kJ•mol-1,则Q1<Q2 |
| B.已知反应C(s)+CO2 (g)= 2CO(g)的ΔH>0,则该反应在高温下能自发进行 |
C.500℃、30MPa下,将0.5mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3,放出的热量为19.3 kJ,其热化学方程式为N2 (g)+3H2 (g)  2NH3 (g) ΔH=—Q kJ·mol-1则Q>38.6 2NH3 (g) ΔH=—Q kJ·mol-1则Q>38.6 |
| D.已知中和热为—57.3 kJ•mol-1,若将含0.5 mol H2 SO4的稀溶液与含0.5 mol Ba(OH)2的稀溶液混合,放出的热量等于57.3 kJ |
您最近一年使用:0次
解题方法
8 . 下列关于化学反应方向的说法正确的是
| A.凡是放热反应都是自发反应 | B.凡是熵增大的反应都是自发反应 |
| C.凡是吸热反应都不是自发反应 | D.反应是否自发,需要综合考虑反应焓变和熵变 |
您最近一年使用:0次
2021-02-20更新
|
187次组卷
|
2卷引用:湖北省武汉市青山区2021-2022学年高二上学期期末考试化学试题
9 . 氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法一定正确的是
| A.氢氧燃料电池的负极反应为:O2+2H2O+4e −= 4OH− |
| B.一定温度下,反应2H2(g)+O2(g)=2H2O(g)能自发进行,该反应的ΔH<0 |
| C.常温常压,氢氧燃料电池放电过程中转移电子的数目6.02×1023时,消耗 H2 11.2 L |
| D.反应2H2(g)+O2(g)=2H2O(g)的ΔH可通过下式估算:ΔH=反应中形成新共价键的键能之和−反应中断裂旧共价键的键能之和 |
您最近一年使用:0次
解题方法
10 . (1)用太阳能分解水制备 是一项新技术,其过程如下。
是一项新技术,其过程如下。

已知: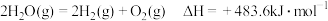
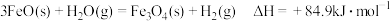
过程I的热化学方程式是_______
(2)已知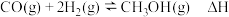 ,经测定不同温度下反应的化学平衡常数如下:
,经测定不同温度下反应的化学平衡常数如下:
①该反应在_______ 条件下易自发。(填“高温”或“低温”)
②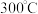 ,某时刻
,某时刻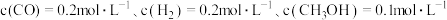 ,此时
,此时 正
正_______  逆(填“>”、“<”或“=”)
逆(填“>”、“<”或“=”)
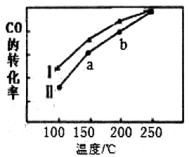
③其他条件不变,在不同催化剂(Ⅰ、Ⅱ)作用下,反应 进行相同时间后,
进行相同时间后, 的转化率随反应温度的变化如图所示。b点
的转化率随反应温度的变化如图所示。b点 的转化率高于a点,原因是
的转化率高于a点,原因是_______
(3)在一体积为 密闭容器中,加入催化剂并加热到一定温度时,使其发生反应
密闭容器中,加入催化剂并加热到一定温度时,使其发生反应 ,起始
,起始 和
和 的物质的量分别为
的物质的量分别为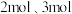 :
:
①达到平衡后测得体系压强是起始时的0.6倍,则该反应的平衡常数
_______ 
②一氧化碳催化加氢合成甲醇反应往往伴随着副反应,生成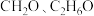 等有机物。一定温度和压强条件下,为了提高反应速率和合成甲醇的选择性,应当
等有机物。一定温度和压强条件下,为了提高反应速率和合成甲醇的选择性,应当_______ 。
(4)在不同的电压下,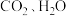 混合电解转化为
混合电解转化为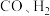 的电流效率如图所示
的电流效率如图所示
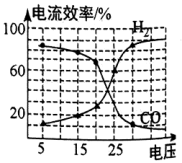
(注: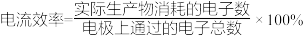 )
)
①由图可知生成 和
和 有相互
有相互_______ (填“促进”、“抑制”或“无影响”)作用。
②用此法生产的 和
和 合成
合成 ,为使利用率最高,电解时应控制电压在
,为使利用率最高,电解时应控制电压在_______ V左右(选填5、15、25)
 是一项新技术,其过程如下。
是一项新技术,其过程如下。
已知:
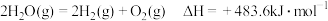
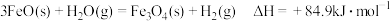
过程I的热化学方程式是
(2)已知
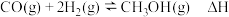 ,经测定不同温度下反应的化学平衡常数如下:
,经测定不同温度下反应的化学平衡常数如下:温度 | 250 | 300 | 350 |
| K | 2.04 | 0.27 | 0.012 |
①该反应在
②
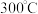 ,某时刻
,某时刻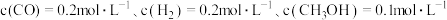 ,此时
,此时 正
正 逆(填“>”、“<”或“=”)
逆(填“>”、“<”或“=”)③其他条件不变,在不同催化剂(Ⅰ、Ⅱ)作用下,反应
 进行相同时间后,
进行相同时间后, 的转化率随反应温度的变化如图所示。b点
的转化率随反应温度的变化如图所示。b点 的转化率高于a点,原因是
的转化率高于a点,原因是
(3)在一体积为
 密闭容器中,加入催化剂并加热到一定温度时,使其发生反应
密闭容器中,加入催化剂并加热到一定温度时,使其发生反应 ,起始
,起始 和
和 的物质的量分别为
的物质的量分别为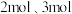 :
:①达到平衡后测得体系压强是起始时的0.6倍,则该反应的平衡常数


②一氧化碳催化加氢合成甲醇反应往往伴随着副反应,生成
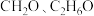 等有机物。一定温度和压强条件下,为了提高反应速率和合成甲醇的选择性,应当
等有机物。一定温度和压强条件下,为了提高反应速率和合成甲醇的选择性,应当(4)在不同的电压下,
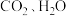 混合电解转化为
混合电解转化为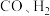 的电流效率如图所示
的电流效率如图所示
(注:
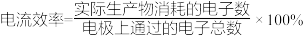 )
)①由图可知生成
 和
和 有相互
有相互②用此法生产的
 和
和 合成
合成 ,为使利用率最高,电解时应控制电压在
,为使利用率最高,电解时应控制电压在
您最近一年使用:0次



