| A.混乱度减小的吸热反应一定不能自发进行 |
| B.碳酸氢钠加热可以分解,因为升高温度利于熵增的方向自发进行 |
C.在温度、压强一定条件下,自发反应总是向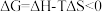 的方向进行 的方向进行 |
| D.水结冰的过程不能自发进行的原因是熵减的过程,改变条件也不可能自发进行 |
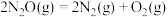
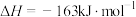 ,下列说法正确的是
,下列说法正确的是| A.高温下自发 | B.低温下自发 | C.任何温度均自发 | D.任何温度不自发 |
| A.已知:S(s)+O2 (g)=SO2 (g) ΔH1=—Q1 kJ•mol-1,S(g)+O2 (g)=SO2 (g) ΔH2=—Q2 kJ•mol-1,则Q1<Q2 |
| B.已知反应C(s)+CO2 (g)= 2CO(g)的ΔH>0,则该反应在高温下能自发进行 |
C.500℃、30MPa下,将0.5mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3,放出的热量为19.3 kJ,其热化学方程式为N2 (g)+3H2 (g)  2NH3 (g) ΔH=—Q kJ·mol-1则Q>38.6 2NH3 (g) ΔH=—Q kJ·mol-1则Q>38.6 |
| D.已知中和热为—57.3 kJ•mol-1,若将含0.5 mol H2 SO4的稀溶液与含0.5 mol Ba(OH)2的稀溶液混合,放出的热量等于57.3 kJ |
4 . (1)试运用盖斯定律回答下列问题:
(1)已知:H2O(g)===H2O(l) ΔH1= -Q1kJ·mol-1
C2H5OH(g)===C2H5OH(l) ΔH2= -Q2kJ·mol-1
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH3= -Q3kJ·mol-1
若使23 g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
(2)碳(s)在氧气供应不充分时,生成CO的同时还生成部分CO2,因此无法通过实验直接测得反应C(s)+ O2(g)=CO(g)的ΔH。但可设计实验,利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有
O2(g)=CO(g)的ΔH。但可设计实验,利用盖斯定律计算出该反应的ΔH,计算时需要测得的实验数据有
计算丙烷的燃烧热有两种途径:
途径Ⅰ:C3H8(g)+5O2(g)===3CO2(g)+4H2O(l) ΔH=-a kJ·mol-1。
途径Ⅱ:C3H8(g)===C3H6(g)+H2(g) ΔH=+b kJ·mol-1;
2C3H6(g)+9O2(g)===6CO2(g)+6H2O(l) ΔH=-c kJ·mol-1;
2H2(g)+O2(g)===2H2O(l) ΔH=-d kJ·mol-1(a、b、c、d均为正值)。
请回答下列问题:
(3)判断等量的丙烷通过两种途径放出的热量,途径Ⅰ放出的热量
(4)由于C3H8(g)=C3H6(g)+H2(g)的反应中,反应物具有的总能量
(5)b与a、c、d的数学关系式是
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。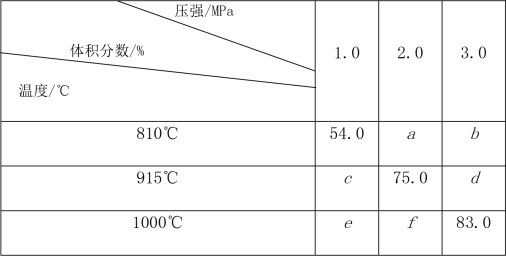
①b>f ②915℃,2.0MPa时E的转化率为60% ③该反应的ΔS<0 ④K(1000℃)<K(810℃)
上述①~④中正确的有( )
| A.4个 | B.3个 | C.2个 | D.1个 |
| A.常温下反应C(s)+CO2 (g)⇌2CO(g)不能自发进行,则该反应△H>0 |
| B.自发反应的熵一定增大,非自发反应的熵一定减小 |
| C.凡是放热反应都是自发的,凡是吸热反应都是非自发的 |
| D.反应2Mg(s)+CO2 (g)⇌C(s)+2MgO(s)能自发进行,则该反应△H>0 |



