1 . 下列实验事实引出的结论不正确的是
| 选项 | 事实 | 结论 |
| A | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸,比较析出沉淀所需时间 | 当其他条件不变时,反应物浓度增大,化学反应速率加快 |
| B | 向FeCl3溶液中加入几滴KSCN溶液,溶液变红,然后加入少量铁粉,红色变浅 | 铁粉与KSCN溶液反应,减少了FeCl3与KSCN的反应 |
| C | 往浅黄色固体难溶物AgBr中加水,振荡,静置。取上层清液,然后加入NaI固体,产生黄色沉淀 | 难溶物存在沉淀溶解平衡 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 . 甲醇( )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示:
 )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示: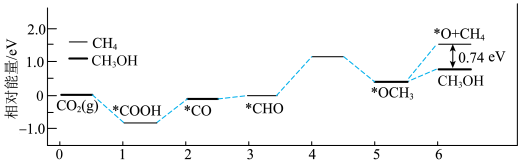
A.生成甲醇反应的决速步为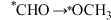 |
| B.两反应只涉及极性键的断裂和生成 |
| C.通过上图分析:甲烷比甲醇稳定 |
D.用 作催化剂可提高甲醇的选择性 作催化剂可提高甲醇的选择性 |
您最近半年使用:0次
名校
解题方法
3 . 卤代烃是重要的工业原料,同时对环境造成严重影响,如破坏臭氧层等,请回答下列问题:
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)
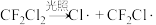 反应①
反应①
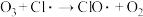 反应②
反应②
 反应③
反应③
(1)活性氯( )的作用是
)的作用是_____ 。
反应②和反应③的能量变化图如下所示
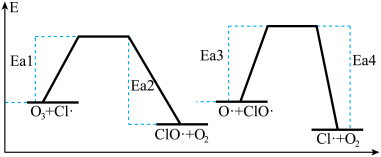
(2)利用上图数据计算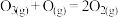 的
的
_____ 。
 破坏臭氧层的机理为(以下物质均为气态)
破坏臭氧层的机理为(以下物质均为气态)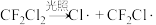 反应①
反应①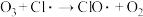 反应②
反应② 反应③
反应③(1)活性氯(
 )的作用是
)的作用是反应②和反应③的能量变化图如下所示

(2)利用上图数据计算
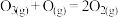 的
的
您最近半年使用:0次
名校
解题方法
4 . 通常在乙苯蒸汽中掺混水蒸气,控制温度600℃,并保持总压为常压。不同温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除 以外的产物中苯乙烯的物质的量分数)如图:
以外的产物中苯乙烯的物质的量分数)如图:
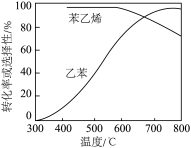
(1)掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实_____ 。
(2)控制反应温度为600℃的理由是_____ 。
(3)某机构用 代替水蒸气开发了乙苯-二氧化碳催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸气工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有
代替水蒸气开发了乙苯-二氧化碳催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸气工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有_____
①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利用CO2资源利用
 以外的产物中苯乙烯的物质的量分数)如图:
以外的产物中苯乙烯的物质的量分数)如图:
(1)掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实
(2)控制反应温度为600℃的理由是
(3)某机构用
 代替水蒸气开发了乙苯-二氧化碳催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸气工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有
代替水蒸气开发了乙苯-二氧化碳催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸气工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO。新工艺的特点有①CO2与H2反应,使乙苯脱氢反应的化学平衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利用CO2资源利用
您最近半年使用:0次
解题方法
5 . 下列实验操作及现象、得出的结论及解释,均正确的是
选项 | 实验操作及现象 | 结论及解释 |
A | 常温下,用胶头滴管将待测NaClO溶液滴在pH试纸上,与标准比色卡对照, | NaClO溶液显碱性 |
B | 在KSCN与 的混合液中再加入少量KCl固体,溶液颜色加深 的混合液中再加入少量KCl固体,溶液颜色加深 | 增大 浓度,平衡正向移动 浓度,平衡正向移动 |
C | 在相同条件下,向一支试管中加入2 mL 5% 溶液,向另一支试管中加入2 mL 5% 溶液,向另一支试管中加入2 mL 5% 溶液和1 mL 溶液和1 mL 溶液,可观察到后者产生气泡速率更快 溶液,可观察到后者产生气泡速率更快 |  可加快 可加快 分解速率 分解速率 |
D | 在室温下,用pH计分别测定 的 的 溶液、 溶液、 的 的 溶液的pH,前者大于后者 溶液的pH,前者大于后者 | 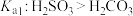 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-03-26更新
|
31次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
6 . 合成氨时采用400-500℃左右的温度进行,主要是因为在该温度时
| A.合成氨的化学反应限度最大 | B.N2的转化率最高 |
| C.催化剂的活性最大 | D.NH3在平衡混合气体中的体积分数最大 |
您最近半年使用:0次
解题方法
7 . 工业上利用黄铁矿(FeS2)制取硫酸,其反应流程如下:

| A.反应①矿石粉碎的目的是提高反应速率 |
| B.反应②中即使通入过量的氧气,也不能将SO2全部转化成SO3 |
| C.接触室选择500℃左右的温度是因为比常温更有利于合成SO3 |
| D.过量的氨水吸收SO2的化学方程式:2NH3·H2O+SO2=(NH4)2SO3+H2O |
您最近半年使用:0次
名校
8 . 资源化利用二氧化硫,一方面能保护环境,另一方面能提高经济效益,具有深远意义。钠碱法的启动吸收剂为 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。
(1)常温下进行“钠碱法”的模拟实验。用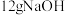 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为___________ L(折算成标准状况)。若实验时只吸收了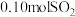 ,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为___________ 。
(2)当钠碱法的吸收液 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是___________ (填写化学式)。
(3)将 通入
通入 溶液时,得到一组
溶液时,得到一组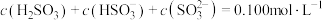 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
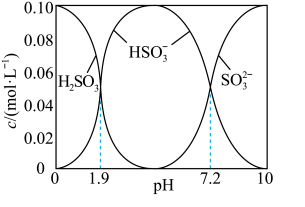
若溶液的 ,溶液中
,溶液中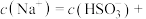
___________ 此时溶液中
___________  。(选填“>”、“<”或“=”)
。(选填“>”、“<”或“=”)
(4)亚硫酸为二元弱酸, 时,其电离常数
时,其电离常数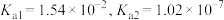 。请说明
。请说明 溶液呈酸性的理由。
溶液呈酸性的理由。___________ 。
(5)工业中可用含 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了
转化”工序。使用该装置实现了___________ (选填编号)。
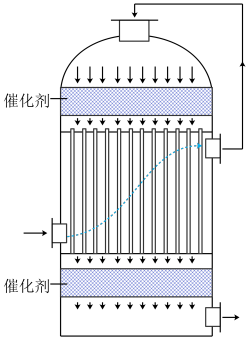
a.充分利用热能 b.防止形成酸雾 c.加速转化 d.获取纯净
d.获取纯净
 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。(1)常温下进行“钠碱法”的模拟实验。用
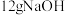 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为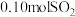 ,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为(2)当钠碱法的吸收液
 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是(3)将
 通入
通入 溶液时,得到一组
溶液时,得到一组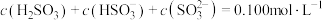 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
若溶液的
 ,溶液中
,溶液中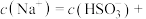

 。(选填“>”、“<”或“=”)
。(选填“>”、“<”或“=”)(4)亚硫酸为二元弱酸,
 时,其电离常数
时,其电离常数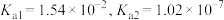 。请说明
。请说明 溶液呈酸性的理由。
溶液呈酸性的理由。(5)工业中可用含
 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了
转化”工序。使用该装置实现了
a.充分利用热能 b.防止形成酸雾 c.加速转化
 d.获取纯净
d.获取纯净
您最近半年使用:0次
解题方法
9 . 2007年2月,中国首条“生态马路”在上海复兴路隧道建成,它运用了“光触媒”技术,在路面涂上一种光催化剂涂料,可将汽车尾气中45%的NO和CO转化成N2和CO2。下列对此反应的叙述中正确的
| A.使用光催化剂不改变反应速率 |
| B.使用光催化剂能增大NO的转化率 |
| C.升高温度能加快反应速率 |
| D.改变压强对反应速率无影响 |
您最近半年使用:0次
名校
10 . 对于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.该反应的 |
B.反应的平衡常数可表示为 |
| C.使用高效催化剂能降低反应的焓变 |
D.其他条件相同,增大 的转化率下降 的转化率下降 |
您最近半年使用:0次
2024-02-29更新
|
35次组卷
|
2卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题



