名校
1 . 微生物燃料电池是利用微生物作为电池中的催化剂,将物质中的化学能直接转化成电能的装置。一种利用微生物燃料电池处理工业含氮废水和生活有机废水的装置如图甲所示,并利用此电池模拟粗铜的精炼,如图乙所示。
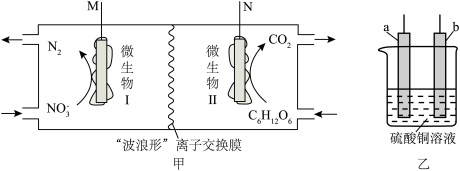
| A.图甲所示微生物燃料电池的电解质溶液为弱碱性 |
| B.增大两电极微生物的数量、采用“波浪形”离子交换膜,均可增大电池放电速率 |
C.处理废水过程中离子交换膜两侧溶液的 基本不变 基本不变 |
| D.若a为粗铜,b应与M相连 |
您最近半年使用:0次
名校
2 . 利用CO2合成二甲醚的原理为2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ∆H,其中投料比
CH3OCH3(g)+3H2O(g) ∆H,其中投料比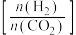 (取值为2、3、4)和温度与CO2的平衡转化率的关系如图所示
(取值为2、3、4)和温度与CO2的平衡转化率的关系如图所示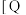 点c(CO2)= 0.2mol·L-1。下列说法正确的是
点c(CO2)= 0.2mol·L-1。下列说法正确的是
 CH3OCH3(g)+3H2O(g) ∆H,其中投料比
CH3OCH3(g)+3H2O(g) ∆H,其中投料比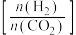 (取值为2、3、4)和温度与CO2的平衡转化率的关系如图所示
(取值为2、3、4)和温度与CO2的平衡转化率的关系如图所示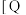 点c(CO2)= 0.2mol·L-1。下列说法正确的是
点c(CO2)= 0.2mol·L-1。下列说法正确的是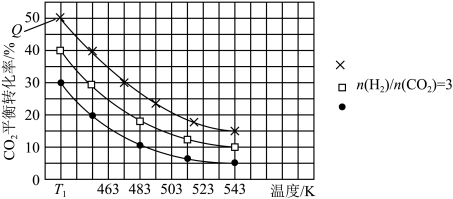
| A.T1K时,Kc=0.0675 | B.△H>0 |
C.X表示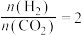 | D.催化剂可以改变CO2的平衡转化率 |
您最近半年使用:0次
名校
3 . 科学家提出在排气管内设置催化剂,使污染气体(CO、NO)转化为大气成分后再排出(反应过程如图)。下列说法错误的是


| A.NO可用排水法收集 |
| B.将燃油净化后使用,可减少NO的排放 |
| C.使用合适的催化剂能加快反应②的速率 |
D.反应②的化学方程式为 |
您最近半年使用:0次
名校
4 . 下列实验方案、现象和结论都正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 将 与 与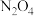 的混合气体通入密闭的注射器,压缩活塞 的混合气体通入密闭的注射器,压缩活塞 | 压缩后气体颜色变浅 | 增大压强会使化学平衡向气体体积缩小的方向移动 |
| B | 将乙醇在浓硫酸、 条件下产生的气体依次通过足量 条件下产生的气体依次通过足量 溶液,酸性高锰酸钾溶液 溶液,酸性高锰酸钾溶液 | 酸性高锰酸钾褪色 | 有乙烯生成 |
| C | 将某固体溶于水后,加足量稀盐酸酸化的 溶液 溶液 | 产生白色沉淀 | 该固体中一定含有 |
| D | 室温下向 两支试管中分别装入等体积的稀硫酸和浓硫酸,再加入表面积相等的铁片 两支试管中分别装入等体积的稀硫酸和浓硫酸,再加入表面积相等的铁片 | B试管中无明显现象 | 说明浓度越大反应速率越慢 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
5 . CI4分)某化学小组欲测定酸性条件下 溶液与
溶液与 溶液反应的化学反应速率,所用试剂为
溶液反应的化学反应速率,所用试剂为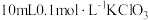 溶液和
溶液和 溶液,所得溶液中
溶液,所得溶液中 的浓度
的浓度 随时间变化的曲线如图1和
随时间变化的曲线如图1和 的速率
的速率 随时间的变化关系如图2:
随时间的变化关系如图2:_____ 。
 (已配平)
(已配平)
(2)根据实验数据可知,该反应在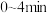 的平均反应速率
的平均反应速率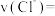
_____ 。
(3)下列说法正确的是_____
A.若纵坐标为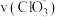 的
的 曲线与图2中的曲线不能重合
曲线与图2中的曲线不能重合
B.图中阴影部分的面积表示 时间内
时间内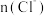 的增大
的增大
C.后期反应速率下降的主要原因是反应物浓度减少
(4)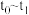 段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
已知: 对该反应无影响;
对该反应无影响;
可供选择的试剂有:A. 固体 B.
固体 B. 固体C.
固体C. D.
D.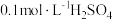 E.
E.
①方案I中所选试剂_____ ,方案Ⅱ中所选试剂_____ 。
②方案Ⅱ烧杯①中加入 水的作用是
水的作用是_____ 。
③除方案I和方案Ⅱ外,请再提出一种可能加快化学反应速率的假设_____ 。
 溶液与
溶液与 溶液反应的化学反应速率,所用试剂为
溶液反应的化学反应速率,所用试剂为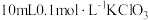 溶液和
溶液和 溶液,所得溶液中
溶液,所得溶液中 的浓度
的浓度 随时间变化的曲线如图1和
随时间变化的曲线如图1和 的速率
的速率 随时间的变化关系如图2:
随时间的变化关系如图2: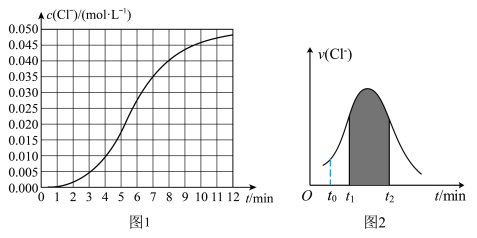
 (已配平)
(已配平)(2)根据实验数据可知,该反应在
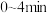 的平均反应速率
的平均反应速率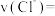
(3)下列说法正确的是
A.若纵坐标为
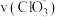 的
的 曲线与图2中的曲线不能重合
曲线与图2中的曲线不能重合B.图中阴影部分的面积表示
 时间内
时间内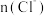 的增大
的增大C.后期反应速率下降的主要原因是反应物浓度减少
(4)
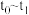 段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:已知:
 对该反应无影响;
对该反应无影响;可供选择的试剂有:A.
 固体 B.
固体 B. 固体C.
固体C. D.
D.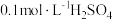 E.
E.
| 方案 | 假设 | 数据处理 | 具体实验操作 |
| I | 反应产物 对反应有催化作用,加快了化学反应速率 对反应有催化作用,加快了化学反应速率 | 取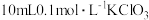 溶液于烧杯中,先加入_____(填字母),再加入 溶液于烧杯中,先加入_____(填字母),再加入 溶液。 溶液。 | 绘制溶液中 浓度 浓度 随时间变化的曲线与图1对比 随时间变化的曲线与图1对比 |
| Ⅱ | 反应中溶液酸性增强,加快了化学反应速率 | 分别向两个烧杯中加入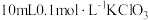 溶液。 溶液。烧杯①:加入  水: 水:烧杯②:加入  _____(填字母)。 _____(填字母)。再分别向两个烧杯中加入  溶液。 溶液。 |
②方案Ⅱ烧杯①中加入
 水的作用是
水的作用是③除方案I和方案Ⅱ外,请再提出一种可能加快化学反应速率的假设
您最近半年使用:0次
名校
6 .  和
和 在催化剂表面合成氨的微观历程及能量变化的示意图如下,用
在催化剂表面合成氨的微观历程及能量变化的示意图如下,用 、
、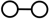 、
、 分别表示
分别表示 、
、 、
、 ,已知:
,已知: ,反应释放热量,下列说法正确的是
,反应释放热量,下列说法正确的是

| A.合成氨反应中,反应物断键吸收能量小于生成物形成新键释放的能量 |
B.②→③过程,是吸热过程且只有 键的断裂 键的断裂 |
C.③→④过程,N原子和H原子形成了含有非极性键的 |
D.使用催化剂,对生成 的速率没有影响 的速率没有影响 |
您最近半年使用:0次
名校
解题方法
7 . 某科研人员提出HCHO与 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
A.HAP降低了该反应的焓变( ) ) |
| B.反应过程中,发生了非极性键的断裂和生成 |
C.HCHO在反应过程中,无 键发生断裂 键发生断裂 |
D. 和 和 的中心原子上所含孤电子对数不同 的中心原子上所含孤电子对数不同 |
您最近半年使用:0次
7日内更新
|
265次组卷
|
4卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
名校
解题方法
8 .  (可表示为
(可表示为 )催化剂的催化原理如下图所示(
)催化剂的催化原理如下图所示( 为烃基)。
为烃基)。
 (可表示为
(可表示为 )催化剂的催化原理如下图所示(
)催化剂的催化原理如下图所示( 为烃基)。
为烃基)。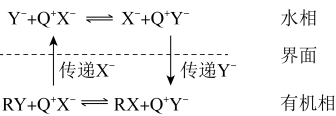
A.总反应为: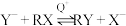 | B.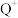 易溶于水相而难溶于有机相 易溶于水相而难溶于有机相 |
C.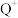 与 与 、 、 之间的离子键强度要适中 之间的离子键强度要适中 | D.PTC催化剂可用作相转移催化剂 |
您最近半年使用:0次
7日内更新
|
267次组卷
|
2卷引用:湖北省圆创联盟2024届高三三月联合测评(一模)化学试卷
名校
9 . 金表面发生分解反应: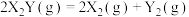 ,其速率方程为
,其速率方程为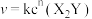 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
下列叙述不正确的是
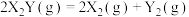 ,其速率方程为
,其速率方程为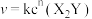 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示: | 0 | 20 | 40 | 60 | 80 | 100 |
 | 0.100 | 0.040 | 0.020 | 0 | ||
 | 0 | 0.020 | ||||
 | 0 | 0.020 |
| A.提高反应物浓度,反应速率不变 |
B. |
C.其他条件不变,若 起始浓度为 起始浓度为 ,则反应物浓度减半所需时间为 ,则反应物浓度减半所需时间为 |
D.当升高温度,反应 时 时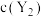 可能小于 可能小于 |
您最近半年使用:0次
10 . 我国丙烷储量丰富,将丙烷转化为具有高附加值的产品是提高丙烷利用效率.实现碳基能源高效利用的关键技术之一。传统利用丙烷:燃烧供能;理想利用丙烷:丙烷脱氢(PDH)制丙烯。下列叙述错误的是
| A.丙烷的燃烧反应一定是放热反应 |
B.丙烷的一氯代物 有2种结构 有2种结构 |
| C.丙烷与溴水在光照条件下容易发生取代反应 |
| D.工业选择合适的催化剂能提高PDH反应的生产效率 |
您最近半年使用:0次



