解题方法
1 . 乙烯氢化的化学方程式为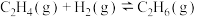
 ,使用不同含Au催化剂的反应进程如下图所示。下列说法
,使用不同含Au催化剂的反应进程如下图所示。下列说法不正确 的是
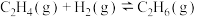
 ,使用不同含Au催化剂的反应进程如下图所示。下列说法
,使用不同含Au催化剂的反应进程如下图所示。下列说法
A.效果较好的催化剂是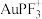 |
B.该反应的 |
| C.过渡态物质的稳定性:过渡态1>过渡态2 |
D.1mol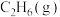 的能量小于1mol 的能量小于1mol 与1mol 与1mol 具有的能量之和 具有的能量之和 |
您最近半年使用:0次
2 . Ⅰ.工业上用CO生产燃料甲醇,一定条件下发生反应: 。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和
。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和 的浓度随时间变化。
的浓度随时间变化。
(1)在图1中,曲线________ (填“a”或“b”)表示使用了催化剂。
(2)该反应属于________ (填“吸热”或“放热”)反应。
(3)增大反应体系压强,则该反应化学平衡常数________ (填“增大”“减小”或“不变”)。根据图2计算该反应的化学平衡常数数值为K=________
Ⅱ.CuSO4溶液是一种重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是________ (填字母)。
a.溶液中Cu2+向阳极移动
b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)图中,A是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在B中实现铁上镀铜:________ (填“CH4”或“O2),a处的电极反应式为________ 。
②当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为________ 。
 。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和
。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和 的浓度随时间变化。
的浓度随时间变化。 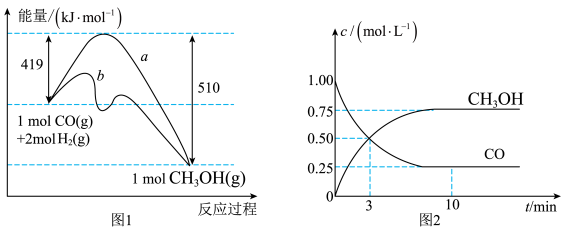
(1)在图1中,曲线
(2)该反应属于
(3)增大反应体系压强,则该反应化学平衡常数
Ⅱ.CuSO4溶液是一种重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.溶液中Cu2+向阳极移动
b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)图中,A是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在B中实现铁上镀铜:

②当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为
您最近半年使用:0次
真题
解题方法
3 . 工业上以硫黄为原料制备硫酸的原理示意图如下,其过程包括Ⅰ、Ⅱ、Ⅲ三个阶段。
(1)硫磺( )的晶体类型是
)的晶体类型是______ 。
(2)硫的燃烧应控制事宜温度。若进料温服超过硫的沸点,部分燃烧的硫以蒸汽的形式随SO2进入到下一阶段,会导致______ (填序号)。
a.硫的消耗量增加 b.SO2产率下降 c.生成较多SO3
(3)SO2(g)氧化生成80g SO3(g)放出热量98.3kJ,写出该反应的热化学方程式______ 。随温度升高,SO2的平衡转化率______ (填“升高”或“降低”)。
(4)从能量角度分析,钒催化剂在反应中的作用为______ 。
Ⅱ.一定条件下,钒催化剂的活性温度范围是450~600℃。为了兼顾转化率和反应速率,可采用四段转化工艺:预热后的SO2和O2通过第一段的钒催化剂层进行催化氧化,气体温度会迅速接近600℃,此时立即将气体通过热交换器,将热量传递给需要预热的SO2和O2,完成第一段转化。降温后的气体依次进行后三段转化,温度逐段降低,总转化率逐段提高,接近平衡转化率。最终反应在450℃左右时,SO2转化率达到97%。
(5)气体经过每段的钒催化剂层,温度都会升高,其原因是______ 。升高温度后的气体都需要降温,其目的是______ 。
(6)采用四段转化工艺可以实现______ (填序号)。
a.控制适宜的温度,尽量加快反应速率,尽可能提高SO2转化率
b.使反应达到平衡状态
c.节约能源
Ⅲ.工业上用浓硫酸吸收SO3。若用水吸收SO3会产生酸雾,导致吸收效率降低。
(7)SO3的吸收率与所用硫酸的浓度、温度的关系如图所示。______ ,温度______ 。
(8)用32吨含S 99%的硫磺为原料生成硫酸,假设硫在燃烧过程中损失2%,SO2生成SO3的转化率是97%,SO3吸收的损失忽略不计,最多可以生产98%的硫酸______ 吨。

(1)硫磺(
 )的晶体类型是
)的晶体类型是(2)硫的燃烧应控制事宜温度。若进料温服超过硫的沸点,部分燃烧的硫以蒸汽的形式随SO2进入到下一阶段,会导致
a.硫的消耗量增加 b.SO2产率下降 c.生成较多SO3
(3)SO2(g)氧化生成80g SO3(g)放出热量98.3kJ,写出该反应的热化学方程式
(4)从能量角度分析,钒催化剂在反应中的作用为
Ⅱ.一定条件下,钒催化剂的活性温度范围是450~600℃。为了兼顾转化率和反应速率,可采用四段转化工艺:预热后的SO2和O2通过第一段的钒催化剂层进行催化氧化,气体温度会迅速接近600℃,此时立即将气体通过热交换器,将热量传递给需要预热的SO2和O2,完成第一段转化。降温后的气体依次进行后三段转化,温度逐段降低,总转化率逐段提高,接近平衡转化率。最终反应在450℃左右时,SO2转化率达到97%。
(5)气体经过每段的钒催化剂层,温度都会升高,其原因是
(6)采用四段转化工艺可以实现
a.控制适宜的温度,尽量加快反应速率,尽可能提高SO2转化率
b.使反应达到平衡状态
c.节约能源
Ⅲ.工业上用浓硫酸吸收SO3。若用水吸收SO3会产生酸雾,导致吸收效率降低。
(7)SO3的吸收率与所用硫酸的浓度、温度的关系如图所示。
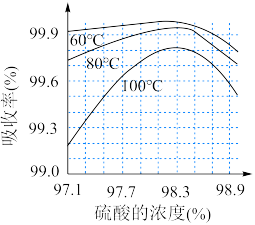
(8)用32吨含S 99%的硫磺为原料生成硫酸,假设硫在燃烧过程中损失2%,SO2生成SO3的转化率是97%,SO3吸收的损失忽略不计,最多可以生产98%的硫酸
您最近半年使用:0次
名校
4 . 下列所示装置或操作能达到实验目的的是
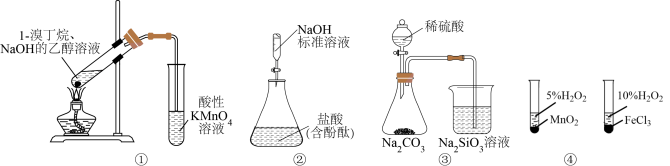

| A.图①:验证1-溴丁烷发生消去反应 |
B.图②: 标准溶液滴定盐酸 标准溶液滴定盐酸 |
| C.图③:比较硫、碳、硅三种元素的非金属性强弱 |
| D.图④:比较不同催化剂对反应速率的影响 |
您最近半年使用:0次
名校
解题方法
5 . 某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,其中不正确的是
A.可逆反应中反应物的转化率都小于 |
| B.使用催化剂既不会改变反应的限度也不会改变反应的焓变 |
| C.吸热反应就是反应物的总能量比生成物的总能量高 |
| D.金属的电化学腐蚀要比化学腐蚀的速率大得多 |
您最近半年使用:0次
名校
6 . 恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应: ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
 ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是| 编号 | 时间/min c(NH3)/(10-3mol/L) 表面积/cm2 | 0 | 20 | 40 | 60 | 80 |
| ① | a | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| ② | a | 1.20 | 0.80 | 0.40 | x | |
| ③ | 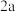 | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
A.相同条件下,增加 的浓度,反应速率增大 的浓度,反应速率增大 |
B.实验①, , ,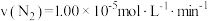 |
C.实验②, 时处于平衡状态, 时处于平衡状态, |
| D.相同条件下,增加催化剂的表面积,反应速率增大 |
您最近半年使用:0次
名校
7 . 反应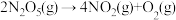 经历如下历程:
经历如下历程:
第一步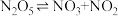 ,快速平衡;
,快速平衡;
第二步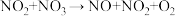 ,慢反应;
,慢反应;
第三步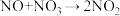 ,快反应。
,快反应。
其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是
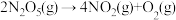 经历如下历程:
经历如下历程:第一步
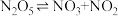 ,快速平衡;
,快速平衡;第二步
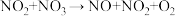 ,慢反应;
,慢反应;第三步
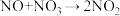 ,快反应。
,快反应。其中可近似认为第二步反应不影响第一步的平衡。下列表述正确的是
A. 此时第一步反应处于平衡状态 此时第一步反应处于平衡状态 | B.反应的中间产物只有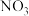 |
C.第二步中 与 与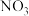 的碰撞仅部分有效 的碰撞仅部分有效 | D.第三步反应的活化能较高 |
您最近半年使用:0次
名校
解题方法
8 . 用下列实验装置进行相应实验,能达到实验目的的是
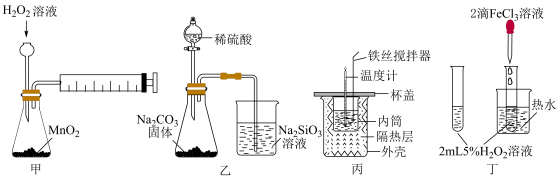

| A.用装置甲定量测定化学反应速率 |
| B.证明非金属性:S>C>Si |
| C.用装置丙准确测定中和反应的反应热 |
D.用装置丁验证 对 对 分解反应有催化作用 分解反应有催化作用 |
您最近半年使用:0次
解题方法
9 . Ⅰ.含硫化合物是实验室和工业上的常用化学品。请回答:
(1)实验室可用铜与浓硫酸反应制备少量 :
: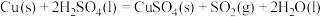
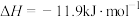 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由___________ 。
(2)已知
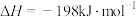 。850K时,在一恒容密闭反应器中充入一定量的
。850K时,在一恒容密闭反应器中充入一定量的 和
和 ,当反应达到平衡后测得
,当反应达到平衡后测得 、
、 和
和 的浓度分别为
的浓度分别为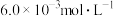 、
、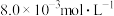 和
和 。
。
①该温度下反应的平衡常数为___________ 。
②平衡时 的转化率为
的转化率为___________ 。
(3)工业上主要采用接触法由含硫矿石制备硫酸。
①下列说法不正确的是___________ 。
A.须采用高温高压的反应条件使 氧化为
氧化为
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和 的转化率
的转化率
D.在吸收塔中宜采用水或稀硫酸吸收 以提高吸收速率
以提高吸收速率
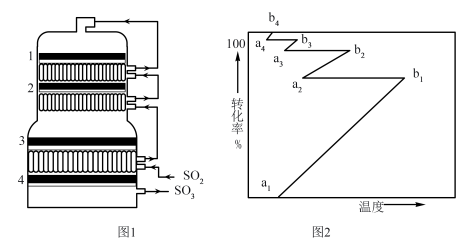
②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是___________ 。
A. B.
B. C.
C. D.
D. E.
E. F.
F. G.
G.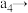
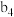
Ⅱ.一定条件下,用 、NiO或
、NiO或 作催化剂对燃煤烟气回收。反应为
作催化剂对燃煤烟气回收。反应为
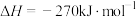 。
。
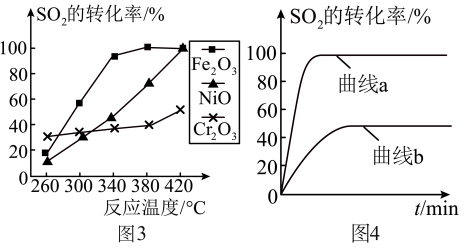
(4)其他条件相同、催化剂不同, 的转化率随反应温度的变化如图3,
的转化率随反应温度的变化如图3, 和NiO作催化剂均能使
和NiO作催化剂均能使 的转化率达到最高,不考虑催化剂价格因素,选择
的转化率达到最高,不考虑催化剂价格因素,选择 的主要优点是:
的主要优点是:___________ 。
(5)某科研小组用 作催化剂。在380℃时,分别研究了
作催化剂。在380℃时,分别研究了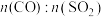 为1:1、3:1时
为1:1、3:1时 转化率的变化情况图4。则图4中表示
转化率的变化情况图4。则图4中表示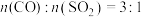 的变化曲线为
的变化曲线为___________ 。
(1)实验室可用铜与浓硫酸反应制备少量
 :
: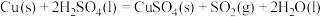
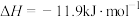 。判断该反应的自发性并说明理由
。判断该反应的自发性并说明理由(2)已知

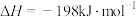 。850K时,在一恒容密闭反应器中充入一定量的
。850K时,在一恒容密闭反应器中充入一定量的 和
和 ,当反应达到平衡后测得
,当反应达到平衡后测得 、
、 和
和 的浓度分别为
的浓度分别为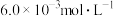 、
、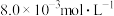 和
和 。
。①该温度下反应的平衡常数为
②平衡时
 的转化率为
的转化率为(3)工业上主要采用接触法由含硫矿石制备硫酸。
①下列说法不正确的是
A.须采用高温高压的反应条件使
 氧化为
氧化为
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和
 的转化率
的转化率D.在吸收塔中宜采用水或稀硫酸吸收
 以提高吸收速率
以提高吸收速率②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是

A.
 B.
B. C.
C. D.
D. E.
E. F.
F. G.
G.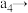
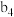
Ⅱ.一定条件下,用
 、NiO或
、NiO或 作催化剂对燃煤烟气回收。反应为
作催化剂对燃煤烟气回收。反应为
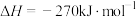 。
。(4)其他条件相同、催化剂不同,
 的转化率随反应温度的变化如图3,
的转化率随反应温度的变化如图3, 和NiO作催化剂均能使
和NiO作催化剂均能使 的转化率达到最高,不考虑催化剂价格因素,选择
的转化率达到最高,不考虑催化剂价格因素,选择 的主要优点是:
的主要优点是:(5)某科研小组用
 作催化剂。在380℃时,分别研究了
作催化剂。在380℃时,分别研究了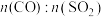 为1:1、3:1时
为1:1、3:1时 转化率的变化情况图4。则图4中表示
转化率的变化情况图4。则图4中表示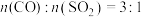 的变化曲线为
的变化曲线为
您最近半年使用:0次
名校
10 . 下列事实不能用勒夏特列原理解释的是
A.溴水中有下列平衡: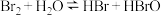 ,当加入少量AgNO3溶液后,溶液的颜色变浅 ,当加入少量AgNO3溶液后,溶液的颜色变浅 |
B.反应 △H<0,升高温度可使平衡向逆反应方向移动 △H<0,升高温度可使平衡向逆反应方向移动 |
| C.向双氧水中加入二氧化锰有利于氧气的生成 |
| D.对于合成NH3反应,为提高NH3的产率,理论上应采取低温措施 |
您最近半年使用:0次



