1 .  是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为
是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为 的7390倍。我国科学家用
的7390倍。我国科学家用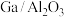 作为催化剂实现了
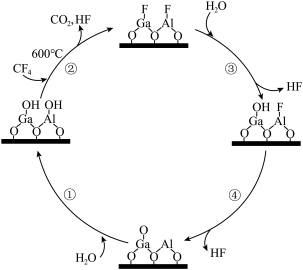
作为催化剂实现了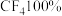 催化水解,其历程如图所示。下列说法错误的是
催化水解,其历程如图所示。下列说法错误的是
 是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为
是电解铝烟气的主要组分之一,属于强温室气体,其温室效应指数为 的7390倍。我国科学家用
的7390倍。我国科学家用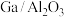 作为催化剂实现了
作为催化剂实现了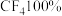 催化水解,其历程如图所示。下列说法错误的是
催化水解,其历程如图所示。下列说法错误的是
A.总反应为: |
B.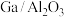 不能改变总反应的 不能改变总反应的 |
C.反应过程中,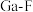 、 、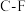 键既有断裂又有形成 键既有断裂又有形成 |
| D.反应过程中涉及的小分子都只含有极性键 |
您最近半年使用:0次
名校
2 . 杭州亚运会主火炬燃料是“零碳甲醇”,这是一种利用焦炉气中的 和工业废气捕获的
和工业废气捕获的 生产的绿色燃料。两者在适宜的过渡金属及其氧化物催化下发生反应:
生产的绿色燃料。两者在适宜的过渡金属及其氧化物催化下发生反应:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:
(1)
_______ 。
(2)在密闭容器中充有2molCO和 ,在催化剂作用下发生反应Ⅱ,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。
,在催化剂作用下发生反应Ⅱ,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。
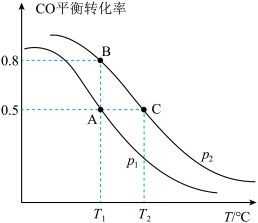
若达到平衡状态A时,容器的体积为2L,则在平衡状态B时容器的体积_______ (填“大于”、“=”或“小于”)2L。若反应进行1min达到平衡状态C,用CO的分压变化表示的平均反应速率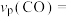
_______  ,此时的化学平衡常数
,此时的化学平衡常数
_______ [ 是用分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)]。
是用分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)]。
(3)不同压强下,按照 投料,实验测定
投料,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
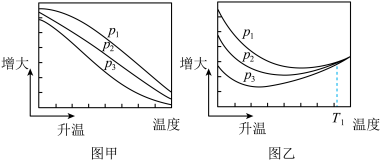
已知: 的平衡转化率
的平衡转化率
 的平衡产率
的平衡产率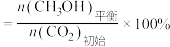
其中纵坐标表示 平衡转化率的是图
平衡转化率的是图_______ (填“甲”或“乙”);压强 、
、 、
、 由大到小的顺序为
由大到小的顺序为_______ ;图乙中 温度时,三条曲线几乎交于一点的原因是
温度时,三条曲线几乎交于一点的原因是_______ 。
(4)催化还原法
① 与丙烯通过金属杂多酸盐
与丙烯通过金属杂多酸盐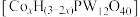 催化合成甲基丙烯酸。研究发现金属杂多酸盐中x对
催化合成甲基丙烯酸。研究发现金属杂多酸盐中x对 转化率的影响如图1所示,由图1得出催化效果最好的金属杂多酸盐化学式是
转化率的影响如图1所示,由图1得出催化效果最好的金属杂多酸盐化学式是_______ 。
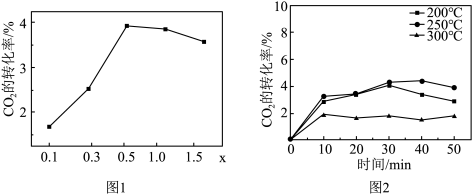
②催化剂在温度不同时对 转化率的影响如图2所示,300℃催化效果远不如200℃和250℃的原因
转化率的影响如图2所示,300℃催化效果远不如200℃和250℃的原因_______ 。
 和工业废气捕获的
和工业废气捕获的 生产的绿色燃料。两者在适宜的过渡金属及其氧化物催化下发生反应:
生产的绿色燃料。两者在适宜的过渡金属及其氧化物催化下发生反应:Ⅰ.


Ⅱ.


Ⅲ.


回答下列问题:
(1)

(2)在密闭容器中充有2molCO和
 ,在催化剂作用下发生反应Ⅱ,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。
,在催化剂作用下发生反应Ⅱ,改变条件,测得CO的平衡转化率与温度(T)、压强(p)的关系如图所示。
若达到平衡状态A时,容器的体积为2L,则在平衡状态B时容器的体积
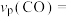
 ,此时的化学平衡常数
,此时的化学平衡常数
 是用分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)]。
是用分压表示的平衡常数,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)]。(3)不同压强下,按照
 投料,实验测定
投料,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图所示。
的平衡产率随温度的变化关系如下图所示。
已知:
 的平衡转化率
的平衡转化率
 的平衡产率
的平衡产率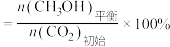
其中纵坐标表示
 平衡转化率的是图
平衡转化率的是图 、
、 、
、 由大到小的顺序为
由大到小的顺序为 温度时,三条曲线几乎交于一点的原因是
温度时,三条曲线几乎交于一点的原因是(4)催化还原法
①
 与丙烯通过金属杂多酸盐
与丙烯通过金属杂多酸盐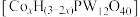 催化合成甲基丙烯酸。研究发现金属杂多酸盐中x对
催化合成甲基丙烯酸。研究发现金属杂多酸盐中x对 转化率的影响如图1所示,由图1得出催化效果最好的金属杂多酸盐化学式是
转化率的影响如图1所示,由图1得出催化效果最好的金属杂多酸盐化学式是
②催化剂在温度不同时对
 转化率的影响如图2所示,300℃催化效果远不如200℃和250℃的原因
转化率的影响如图2所示,300℃催化效果远不如200℃和250℃的原因
您最近半年使用:0次
解题方法
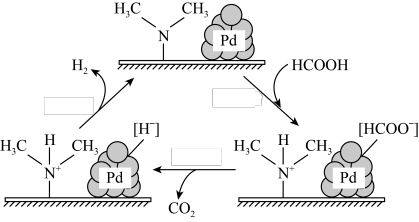
3 . 在催化剂作用下,HCOOH分解生成 和
和 可能的反应机理如图所示。下列说法不正确的是
可能的反应机理如图所示。下列说法不正确的是
 和
和 可能的反应机理如图所示。下列说法不正确的是
可能的反应机理如图所示。下列说法不正确的是
A.该反应的总反应为 |
| B.其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳 |
| C.改变催化剂的用量和表面积,可改变化学反应速率 |
D.HCOOD在催化剂作用下可释放出 |
您最近半年使用:0次
4 . 甲醇是重要的化工原料,可以使用多种方法制备甲醇。
I.利用反应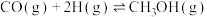
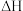 ,若在体积一定的密闭容器中按物质的量之比1:2充入CO和
,若在体积一定的密闭容器中按物质的量之比1:2充入CO和 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如如图所示。
的体积分数在不同压强下随温度的变化情况如如图所示。
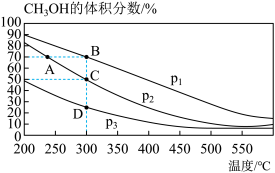
(1)该反应的
______ 0(填“>”“<”或“=”)
(2)达到平衡时,反应速率:A点____ B点(填“>”“<”或“=”)。在C点时,CO的转化率为____ 。
(3)要提高CO的平衡转化率,可以采取的措施是______ (填字母)。
A.加入催化剂 B.增大CO的浓度 C.通入 D.通入惰性气体 E.分离出甲醇
D.通入惰性气体 E.分离出甲醇
(4)关于该反应,下列说法正确的是___________(填字母)。
Ⅱ.利用 与在催化剂的作用下合成甲醇。主反应:
与在催化剂的作用下合成甲醇。主反应: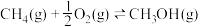 ,在温度为 T℃、压强为
,在温度为 T℃、压强为 条件下,向容器中充入
条件下,向容器中充入 、
、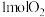 ,充分反应达平衡时
,充分反应达平衡时 的转化率为
的转化率为 。
。
(5)求平衡时 的物质的量为
的物质的量为______ 。
(6)主反应的相对压力平衡常数
___________ ( 表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。用含p的式子表示)。
表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。用含p的式子表示)。
I.利用反应
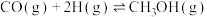
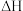 ,若在体积一定的密闭容器中按物质的量之比1:2充入CO和
,若在体积一定的密闭容器中按物质的量之比1:2充入CO和 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如如图所示。
的体积分数在不同压强下随温度的变化情况如如图所示。
(1)该反应的

(2)达到平衡时,反应速率:A点
(3)要提高CO的平衡转化率,可以采取的措施是
A.加入催化剂 B.增大CO的浓度 C.通入
 D.通入惰性气体 E.分离出甲醇
D.通入惰性气体 E.分离出甲醇(4)关于该反应,下列说法正确的是___________(填字母)。
| A.该反应在任何温度下都能自发进行 | B.使用催化剂,不能提高CO的平衡转化率 |
| C.升高温度,正反应速率增大,逆反应速率减小 | D.增大压强,该反应的化学平衡常数不变 |
Ⅱ.利用
 与在催化剂的作用下合成甲醇。主反应:
与在催化剂的作用下合成甲醇。主反应: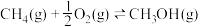 ,在温度为 T℃、压强为
,在温度为 T℃、压强为 条件下,向容器中充入
条件下,向容器中充入 、
、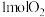 ,充分反应达平衡时
,充分反应达平衡时 的转化率为
的转化率为 。
。(5)求平衡时
 的物质的量为
的物质的量为(6)主反应的相对压力平衡常数

 表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。用含p的式子表示)。
表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。用含p的式子表示)。
您最近半年使用:0次
2023-12-23更新
|
52次组卷
|
2卷引用:内蒙古自治区赤峰市红山区校级联考2023-2024学年高三上学期12月期中理科综合试题
名校
5 . 活泼自由基与氧气的反应一直是关注的热点。HNO自由基与 反应过程的能量变化如图所示,下列说法不正确的是
反应过程的能量变化如图所示,下列说法不正确的是
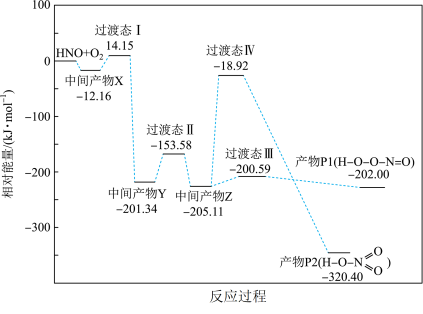
 反应过程的能量变化如图所示,下列说法不正确的是
反应过程的能量变化如图所示,下列说法不正确的是
| A.总反应为放热反应 |
| B.稳定性:产物P1<产物P2 |
| C.相同条件下,由中间产物Z转化为产物反应速率:v(产物P1)<v(产物P2) |
D.该历程中最小正反应的活化能 kJ·mol kJ·mol |
您最近半年使用:0次
名校
6 . 下列事实中,不能用勒夏特列原理解释的是
| A.用排饱和食盐水法收集氯气 | B.使用催化剂可加快 转化为 转化为 的速率 的速率 |
| C.打开可乐饮料后会产生大量气泡 | D.90℃纯水的 |
您最近半年使用:0次
2023-12-06更新
|
97次组卷
|
3卷引用:内蒙古自治区优质高中联考2023-2024学年高二上学期11月期中化学试题
7 . 在恒温恒容的密闭容器中发生 △H<0,T℃时,平衡常数为K,下列说法正确的是
△H<0,T℃时,平衡常数为K,下列说法正确的是
 △H<0,T℃时,平衡常数为K,下列说法正确的是
△H<0,T℃时,平衡常数为K,下列说法正确的是| A.该反应在任何温度下都可自发进行 |
B.T℃时,若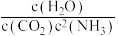 <K时,则V正<V逆 <K时,则V正<V逆 |
| C.若容器内气体压强保持不变,该可逆反应达到化学平衡状态 |
| D.选择高效催化剂可以提高活化分子百分数,提高CO(NH2)2平衡产率 |
您最近半年使用:0次
2023-08-14更新
|
679次组卷
|
4卷引用:内蒙古赤峰二中2023-2024学年高二上学期第二次月考化学试题
8 . 甲烷可在铑/铈氧化物的催化下与过氧化氢反应,转化为甲醇和甲基过氧化氢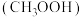 ,实现了天然气的高效利用,其原理如图所示,下列说法错误的是
,实现了天然气的高效利用,其原理如图所示,下列说法错误的是

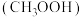 ,实现了天然气的高效利用,其原理如图所示,下列说法错误的是
,实现了天然气的高效利用,其原理如图所示,下列说法错误的是
| A.反应③有极性键的断裂与生成 |
| B.反应⑤中,Ce的化合价升高 |
C.铑/铈氧化物改变了 和 和 的反应历程,降低了反应的活化能 的反应历程,降低了反应的活化能 |
D.若用 作反应物,一段时间后只有 作反应物,一段时间后只有 、 、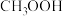 中含有 中含有 |
您最近半年使用:0次
2023-03-24更新
|
370次组卷
|
3卷引用:内蒙古赤峰市2024届高三一模理科综合-化学试题
内蒙古赤峰市2024届高三一模理科综合-化学试题湖南省郴州市2023届高三下学期第三次教学质量监测化学试题(已下线)化学(九省联考考后提升卷,河南卷)-2024年1月“九省联考”真题完全解读与考后提升
解题方法
9 . 我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下,下列说法正确的是
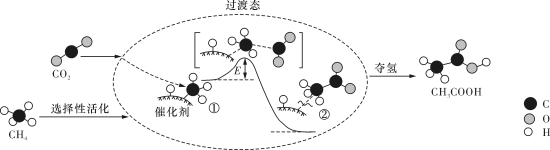

| A.①→②吸收能量并形成了碳碳单键 |
| B.反应中催化剂有效改变反应的反应热 |
| C.CH4→CH3COOH过程中,有极性键的断裂和非极性键的形成 |
| D.生成CH3COOH总反应的原子利用率小于100% |
您最近半年使用:0次
10 . 在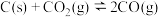 反应中,下列措施能使化学反应速率增大的是
反应中,下列措施能使化学反应速率增大的是
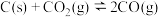 反应中,下列措施能使化学反应速率增大的是
反应中,下列措施能使化学反应速率增大的是| A.将碳粉改为块状碳 | B.减少 的浓度 的浓度 |
| C.降低温度 | D.使用合适的催化剂 |
您最近半年使用:0次



