1 . 图为某反应的“能量—反应过程”图,下列有关说法正确的是

A.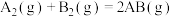 是放热反应 是放热反应 |
| B.形成2mol AB的化学键需要吸收b kJ的能量 |
| C.加入催化剂对a和b的值没有影响 |
| D.若白磷转化成红磷的反应和上述过程能量变化相反,则等质量的红磷更加稳定 |
您最近半年使用:0次
2 . 下列关于有效碰撞理论与影响速率因素之间关系正确的是
| A.增大反应物浓度,可以提高活化分子百分数,从而提高反应速率 |
| B.对于气体反应来说,通过压缩体积增大压强,可以提高单位体积内活化分子数,从而提高反应速率 |
| C.温度升高,反应所需活化能减少,反应速率增大 |
| D.选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 |
您最近半年使用:0次
3 . 下图是我国科研工作者研究MgO(s)与CH4(g)作用最终生成Mg(s)与CH3OH (g)的物质相对能量-反应进程曲线。下列叙述错误的是
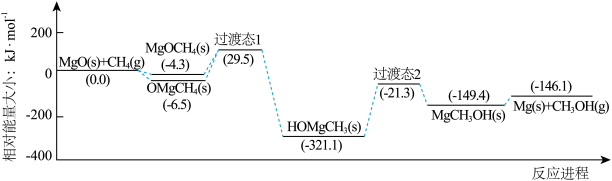

| A.中间体OMgCH4(s)比MgOCH4(s)更稳定 |
| B.MgCH3OH(s)→Mg(s)+CH3OH(g)的速率决定总反应的速率 |
| C.生成HOMgCH3(s)的过程中有极性键的断裂和形成 |
| D.总反应的热化学方程式为MgO(s)+CH4(g)=Mg(s)+CH3OH (g) ΔH= -146.1kJ·mol-1 |
您最近半年使用:0次
名校
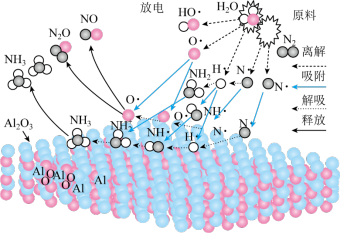
4 . 科学家利用等离子结合 催化剂一步法直接从湿空气
催化剂一步法直接从湿空气 合成氨,原理如下图所示。已知:
合成氨,原理如下图所示。已知: 的结构式为
的结构式为 。下列叙述错误的是
。下列叙述错误的是
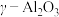 催化剂一步法直接从湿空气
催化剂一步法直接从湿空气 合成氨,原理如下图所示。已知:
合成氨,原理如下图所示。已知: 的结构式为
的结构式为 。下列叙述错误的是
。下列叙述错误的是
A. 能提高 能提高 和 和 活化分子百分率 活化分子百分率 |
B.上述利用湿空气和氮气合成氨反应的原子利用率为 |
C. 的键角大于 的键角大于 的键角 的键角 |
| D.上述转化中有非极性键断裂和形成 |
您最近半年使用:0次
5 . 制造水煤气时发生可逆反应C(s)+H2O(g) CO(g)+H2(g) ΔH >0,下列措施既能提高化学反应速率,又能提高平衡转化率的是
CO(g)+H2(g) ΔH >0,下列措施既能提高化学反应速率,又能提高平衡转化率的是
 CO(g)+H2(g) ΔH >0,下列措施既能提高化学反应速率,又能提高平衡转化率的是
CO(g)+H2(g) ΔH >0,下列措施既能提高化学反应速率,又能提高平衡转化率的是| A.增大压强 | B.升高温度 | C.增大C的用量 | D.加入催化剂 |
您最近半年使用:0次
解题方法
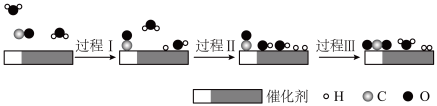
6 . 中国学者在水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]中突破了低温下高转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化实现的,反应过程示意图如下:
下列说法正确 的是

下列说法
| A.过程Ⅰ和过程Ⅲ均为放热过程 |
| B.图示过程中的3个过程都涉及到了H2O |
| C.过程Ⅲ生成了具有极性共价键的H2、CO2 |
| D.使用催化剂缩小反应物和生成物的能量差 |
您最近半年使用:0次
2023高三·全国·专题练习
解题方法
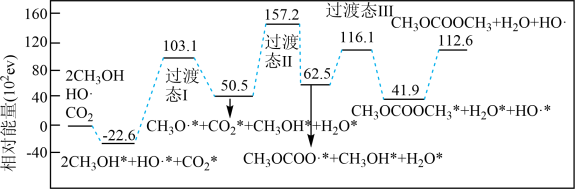
7 . 碳酸二甲酯DMC( )是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
)是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
下列说法错误的是
 )是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
)是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
下列说法错误的是
| A.HO·提高了反应的活化能 |
| B.过程CH3OH*+HO·*=CH3O·*+H2O*是该反应的决速步骤 |
| C.过程中既有H-O键的断裂,又有H-O键的形成 |
| D.吸附和脱附过程中共吸收1.126×104 eV的能量 |
您最近半年使用:0次
23-24高三上·浙江·阶段练习
8 . 一定条件下,丙烯与 反应生成
反应生成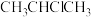 和
和 的反应历程如图所示。下列说法不正确的是
的反应历程如图所示。下列说法不正确的是
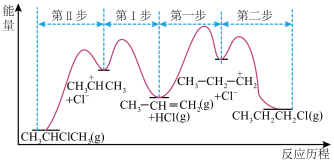
 反应生成
反应生成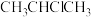 和
和 的反应历程如图所示。下列说法不正确的是
的反应历程如图所示。下列说法不正确的是
A.合成 的反应中,第一步为反应的决速步 的反应中,第一步为反应的决速步 |
B.其他条件不变,适当升高温度可以提高加成产物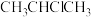 的比例 的比例 |
C.根据该反应推测,丙烯与 加成的主要产物为2-溴丙烷 加成的主要产物为2-溴丙烷 |
D.反应的主要产物为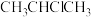 ,是由于活性中间体 ,是由于活性中间体 比 比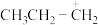 更稳定,所需活化能更低 更稳定,所需活化能更低 |
您最近半年使用:0次
9 . 皓矾( )在生活中主要用作材料防腐剂和医疗消毒剂。以闪锌矿(主要成分为
)在生活中主要用作材料防腐剂和医疗消毒剂。以闪锌矿(主要成分为 ,含有少量
,含有少量 、
、 、
、 、
、 、
、 等杂质)为主要原料制备皓矾的工艺流程如图(已知:“滤渣1”含有硫等)。
等杂质)为主要原料制备皓矾的工艺流程如图(已知:“滤渣1”含有硫等)。

回答下列问题:
(1)基态锌原子价层电子排布式为___________ ;S、O、Si三种元素中,第一电离能最大的是___________ 。
(2)“酸浸”时, 和
和 反应的离子方程式为
反应的离子方程式为___________ 。
(3)“氧化”时,双氧水实际消耗量远大于理论计算值,除温度因素外,可能的原因是___________ 。
(4)“滤渣2”为黄钠铁矾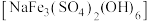 沉淀,产生该沉淀的离子方程式为
沉淀,产生该沉淀的离子方程式为___________ 。
(5)若“净化”时,将除去 和
和 的反应设计成原电池,正极生成的物质是
的反应设计成原电池,正极生成的物质是___________ (填化学式)。
(6)该工艺产生的废液中含有 ,需要先处理后排放。向废液中加入由
,需要先处理后排放。向废液中加入由 和
和 组成的缓冲溶液调节pH,再通入
组成的缓冲溶液调节pH,再通入 发生反应:
发生反应: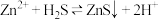 。
。
处理后的废液中部分微粒浓度如下:
则a=___________ ,该废水___________ (填“能”或“不能”)排放。
已知:常温下, ,
,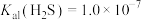 ,
, ,
, 。当c(Zn2+)≤1.0×10-5mol/L时认为废水可以排放。
。当c(Zn2+)≤1.0×10-5mol/L时认为废水可以排放。
 )在生活中主要用作材料防腐剂和医疗消毒剂。以闪锌矿(主要成分为
)在生活中主要用作材料防腐剂和医疗消毒剂。以闪锌矿(主要成分为 ,含有少量
,含有少量 、
、 、
、 、
、 、
、 等杂质)为主要原料制备皓矾的工艺流程如图(已知:“滤渣1”含有硫等)。
等杂质)为主要原料制备皓矾的工艺流程如图(已知:“滤渣1”含有硫等)。
回答下列问题:
(1)基态锌原子价层电子排布式为
(2)“酸浸”时,
 和
和 反应的离子方程式为
反应的离子方程式为(3)“氧化”时,双氧水实际消耗量远大于理论计算值,除温度因素外,可能的原因是
(4)“滤渣2”为黄钠铁矾
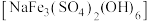 沉淀,产生该沉淀的离子方程式为
沉淀,产生该沉淀的离子方程式为(5)若“净化”时,将除去
 和
和 的反应设计成原电池,正极生成的物质是
的反应设计成原电池,正极生成的物质是(6)该工艺产生的废液中含有
 ,需要先处理后排放。向废液中加入由
,需要先处理后排放。向废液中加入由 和
和 组成的缓冲溶液调节pH,再通入
组成的缓冲溶液调节pH,再通入 发生反应:
发生反应: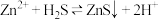 。
。处理后的废液中部分微粒浓度如下:
| 微粒 |  |  |  |  |
| 浓度/(mol/L) | 0.2 | 0.1 | 0.2 | a |
已知:常温下,
 ,
, ,
, ,
, 。当c(Zn2+)≤1.0×10-5mol/L时认为废水可以排放。
。当c(Zn2+)≤1.0×10-5mol/L时认为废水可以排放。
您最近半年使用:0次
名校
10 . “肼合成酶”以其中的 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼(
转化为肼(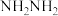 ),其反应历程如下所示。
),其反应历程如下所示。
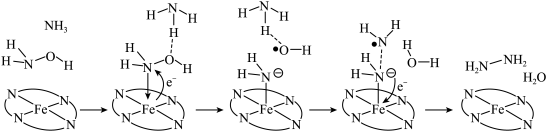
下列说法正确的是
 配合物为催化中心,可将
配合物为催化中心,可将 与
与 转化为肼(
转化为肼(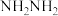 ),其反应历程如下所示。
),其反应历程如下所示。
下列说法正确的是
A. 、 、 、 、 均为极性分子 均为极性分子 |
| B.反应涉及N-H、N-O键断裂、不涉及N-N键生成 |
C.催化中心的 被还原为 被还原为 ,后又被氧化为 ,后又被氧化为 |
D.将 替换为 替换为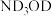 ,反应可得 ,反应可得 |
您最近半年使用:0次



